Circulation 中国科学技术大学单革课题组发现线粒体编码的环RNA快速降解机制及其在治疗心力衰竭中的应用
时间:2025-02-24 12:08:43 热度:37.1℃ 作者:网络
环RNA (circular RNA, circRNA)是一大类共价闭环的单链RNA分子。近年来的研究表明,circRNA具有重要的调控功能并在多种疾病发生发展中起着重要作用。目前已知动物细胞中的circRNA大部分由细胞核基因组编码;研究人员对核基因组编码的circRNA的生成、降解、功能和机制已有较多的认知。单革实验室前期发现并报道了线粒体DNA也可以编码circRNA,并且将其命名为线粒体编码的环RNA (mitochondria-encoded circRNA, mecciRNA)(Science China Life Sciences, 2020)。
线粒体对于极度耗能的器官,尤其是心脏,至关重要。心肌细胞中线粒体功能紊乱与心力衰竭(心衰)的发生发展密切相关。心衰具有高发病率、高致死率,治疗费用昂贵,是我国及全球的严重临床和公共健康问题。据统计,我国35岁以上人群的心衰患病率已达1.3%,心衰患者五年内的死亡率高达50%。心衰目前无法治愈,现有的治疗策略主要集中在缓解症状和延缓病程;目前迫切需要研发基于心衰疾病发生发展的病理而保护和恢复心肌细胞功能的治疗性药物。
2025年2月20日,中国科学技术大学生命科学与医学部单革教授团队在Circulation在线发表题为“Fast Degradation of MecciRNAs by SUPV3L1/ELAC2 Provides a Novel Opportunity to Tackle Heart Failure with Exogenous MecciRNA”的研究论文。该研究揭示了动物中保守存在的由RNA解旋酶SUPV3L1和内切酶ELAC2形成的复合物介导的mecciRNA快速降解机制。研究发现在心衰病人以及小鼠心衰模型中,心肌细胞中mecciRNA降解进一步加快。而mecciRNA可以抑制线粒体中有害活性氧(ROS)的释放;在两种不同的小鼠心衰模型中,给予外源mecciRNA药物均能够减少有害线粒体ROS释放,保护心肌细胞、进而延缓心衰的发展进程。

研究人员在小鼠和人的细胞系以及模式动物秀丽线虫中通过高通量测序和实验验证发现,相对于较高稳定性的核基因组编码的circRNA,mecciRNA会被快速降解。通过一系列生化和分子实验证明,SUPV3L1和ELAC2形成复合物介导mecciRNA降解。研究人员利用co-IP、蛋白质谱、RIP-seq等手段,对降解复合物进一步的研究发现,SUPV3L1与线粒体膜通透性转换孔(mitochondrial permeability transition pore,mPTP)的组分ATP5B及其调控因子TRAP1和CypD具有相互作用,并且TRAP1与ATP5B均能够结合mecciRNA。线粒体是细胞内ROS的主要来源,线粒体mPTP负责线粒体ROS的释放;而TRAP1抑制mPTP开放,CypD促进其开放。在SUPV3L1不足的细胞中,mecciRNA表达水平明显升高,同时,线粒体中的TRAP1含量上升,CypD含量下降。向细胞中转染体外合成的、与TRAP1结合的一个mecciRNA mecciND2,发现其能够在胞质溶胶(cytosol)中与TRAP1结合,促进TRAP1转运进入线粒体、并导致线粒体中TRAP1水平升高;而胞质溶胶和线粒体中CypD水平均降低,最终抑制mPTP对线粒体有害ROS的释放。
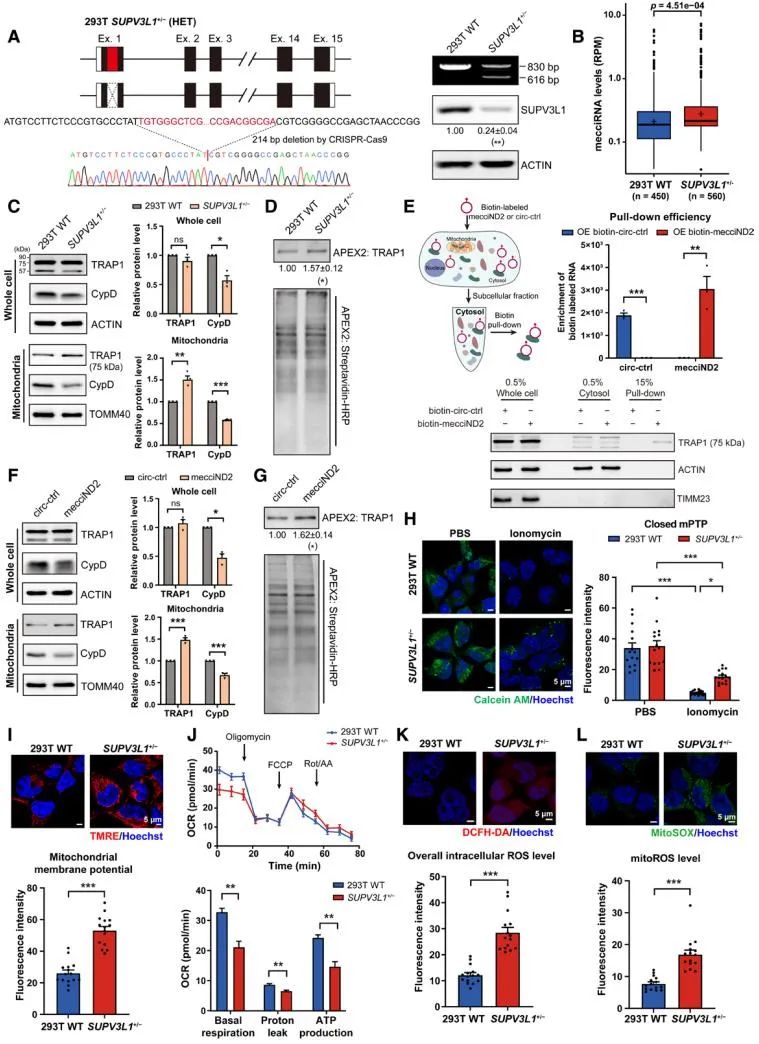
一些原因引起的缺氧低氧以及某些药物,如癌症化疗药物阿霉素(DOX)产生的心脏毒性,能引起或加重心衰。心衰心脏的能量供需失衡,线粒体的功能障碍引发ROS的过度生成和过量释放,导致心肌细胞受损推动了心衰的发生发展。研究人员通过分析人和小鼠心脏的RNA高通量测序数据发现,心衰的心脏组织中,mecciRNA整体含量减少。mecciNd2是在小鼠心衰心脏中显著减少的mecciRNA,体外合成的mecciNd2转染到DOX或低氧处理的小鼠HL-1心肌细胞中,能够显著抑制mPTP过度开放、阻止线粒体膜电位降低以及线粒体ROS释放。体外合成的mecciND2在人诱导多能干细胞分化而来的心肌细胞(hiPSC-CM细胞)中也起到了相似的效果。接下来研究人员利用两种小鼠心衰模型探究了mecciNd2对心衰的治疗作用。一种是压力过载(主动脉弓缩窄术,TAC)诱导的小鼠心衰模型,另一种是DOX产生的心脏毒性诱导的小鼠心衰模型。这两种小鼠模型的心脏中mecciRNAs (包括mecciNd2)水平降低,同时SUPV3L1和ELAC2水平较高。将体外合成的mecciNd2用脂质体包裹后,通过静脉注射的方式递送到小鼠体内,RT-qPCR及单分子荧光原位杂交技术(smFISH)结果显示,小鼠心脏中的mecciNd2水平显著升高。心脏超声结果表明,mecciNd2药物的注射有效保护了心脏功能。在DOX模型中,减轻了DOX引起的左心室壁变薄和心室扩张等病理变化。心脏组织切片染色发现,mecciNd2缓解了DOX诱导的心脏纤维化,降低了心肌细胞凋亡。在TAC模型中,由于左心室后负荷的增加,心脏经历了从代偿期到失代偿期的病理性转变。该过程伴随着左心室重塑,初期表现为向心性肥厚,随后转变为离心性肥厚。TAC手术后5周,注射对照circRNA的小鼠心脏收缩功能受损,表现出离心性肥厚的失代偿状态;而mecciNd2注射的小鼠心脏功能接近假手术对照组水平,超声测量结果表明心脏仍处于向心性肥厚阶段。此外,与对照circRNA组相比,mecciNd2组处理的TAC小鼠显示出较小的心肌细胞增大和较少的纤维化区域。这些结果显示mecciNd2延长了代偿期。进一步分析发现,mecciNd2的注射在DOX和TAC诱导的小鼠中均维持了心肌细胞中线粒体TRAP1(使其没有下降)和CypD(使其未发生上升)的水平以及线粒体功能。DOX和TAC导致小鼠心肌细胞线粒体外膜蛋白TOMM20水平下降,而mecciNd2的注射维持了TOMM20的水平。这些结果表明,mecciNd2药物具有针对心衰病理机制的心脏保护作用,显著延缓了心衰进程。

综上所述,研究人员发现mecciRNA通过保守的SUPV3L1/ELAC2复合物被快速降解,并且mecciRNA水平调控mPTP的开放和线粒体内有害ROS的释放。通过一系列证据表明,利用mecciRNA的降解机制及与TRAP1相互作用的mecciRNA (如mecciND2),可以有效抑制mPTP的过度开放和线粒体ROS的过量释放,从而为心力衰竭的治疗提供新的策略。
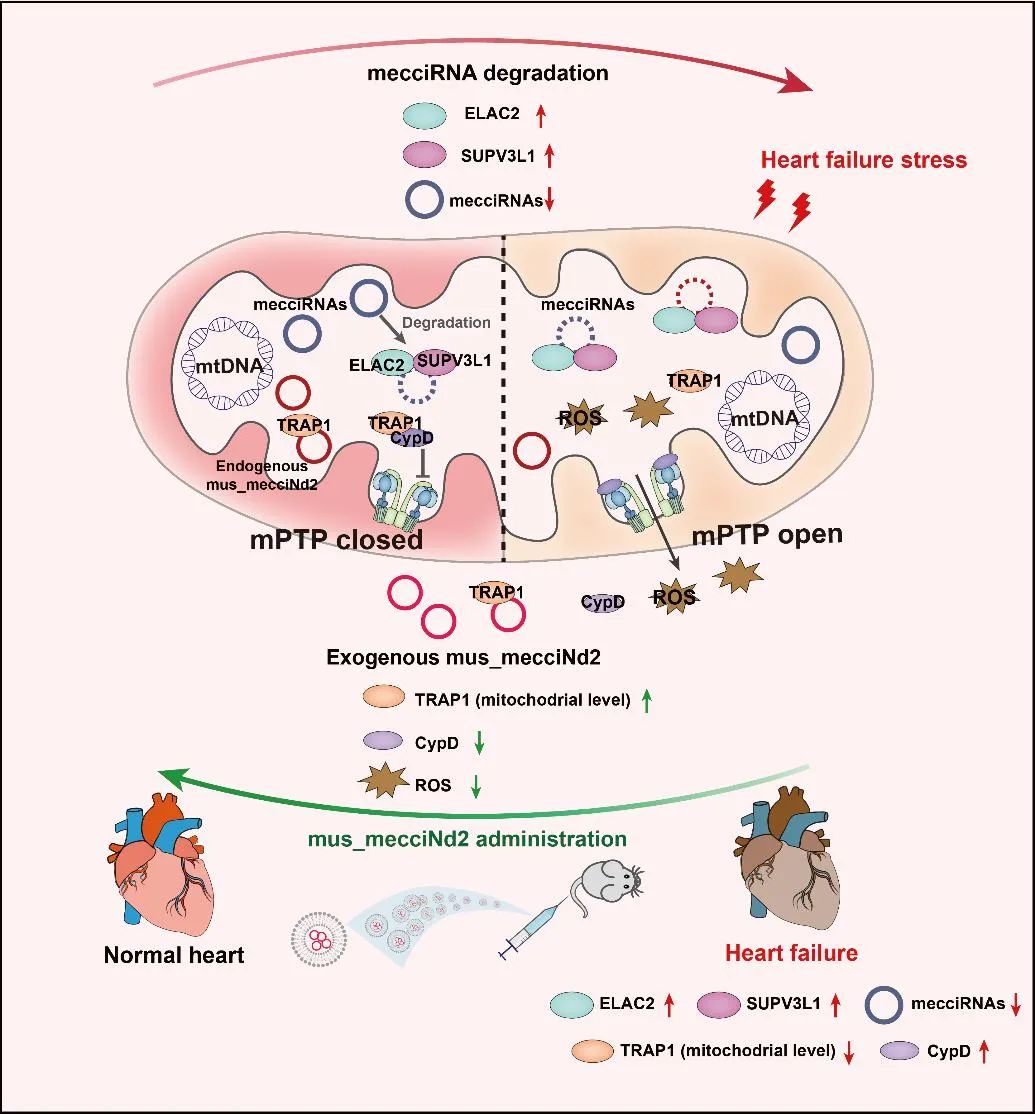
mecciRNA降解及外源性mecciND2在心力衰竭治疗中的作用机制示意图
中国科学技术大学生命科学与医学部特任副研究员刘旭与博士生汪沁维为该论文共同第一作者,单革教授为通讯作者。研究成果是在中国科学技术大学附属第一医院(安徽省立医院)心内科马礼坤主任、陈亮研究员、李新亚博士后协作下取得。研究得到了科技部、国家基金委、安徽省、中国科学技术大学、以及合肥综合性国家科学中心前沿交叉科学与生物医学研究所的基金项目资助。
原文链接:
https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.124.070840


