Cardiovasc Diabetol 西苑医院刘玥团队首次构建跨器官血管单细胞图谱,解码糖尿病泛血管并发症心肾共病机制
时间:2025-03-03 12:16:04 热度:37.1℃ 作者:网络
糖尿病泛血管疾病(Diabetic Panvascular Disease, DPD)是糖尿病最严重的并发症之一,表现为全身血管内皮功能失调、炎症反应加剧及纤维化进程加速,最终导致心肌梗死、肾功能衰竭等终末期疾病。然而,传统研究多聚焦单一器官或细胞类型,难以解析跨器官血管网络的动态协作机制,尤其是糖尿病环境下血管细胞间的异常“通信”模式。近年来,单细胞测序技术为解析复杂疾病提供了革命性工具,但现有研究多集中于分子特征或基因表达谱分析,缺乏对血管细胞间通信网络的系统性探索。作为循环系统与各器官环境之间的关键界面,血管网络的信号交互(如ECs与免疫细胞、平滑肌细胞的通信)尚未被系统解析。揭示正常和病理状态下血管通信的通用模式及其分子机制,将为开发针对DPD的精准治疗策略提供重要依据。

2025年2月26日,中国中医科学院西苑医院心血管病中心(国家中医心血管病临床医学研究中心)刘玥主任医师团队在心血管内分泌领域的国际知名期刊Cardiovascular Diabetology杂志上发表了题为“Cellular crosstalk in organotypic vasculature: mechanisms of diabetic cardiorenal complications and SGLT2i responses”的研究成果,研究团队通过整合8个组织的单细胞RNA测序数据,构建了首个器官型血管系统单细胞图谱,并系统解析了血管细胞间通信(CCI)的特征。基于频率的数学模型揭示了高频受体-配体对在器官功能特异性及多器官共病机制中的关键作用。研究进一步明确了内皮细胞(ECs)在血管网络中的核心功能。以心脏和肾脏为例,研究发现BMP6通过促进心肌纤维化及肾小球硬化介导糖尿病心肾并发症,并揭示了目前治疗糖尿病心肾并发症的“明星药物”SGLT2i通过靶向调控BMP6信号通路发挥保护作用的分子机制。这些发现为解析糖尿病泛血管疾病(DPD)的共病机制及SGLT2i的药理作用提供了科学证据。
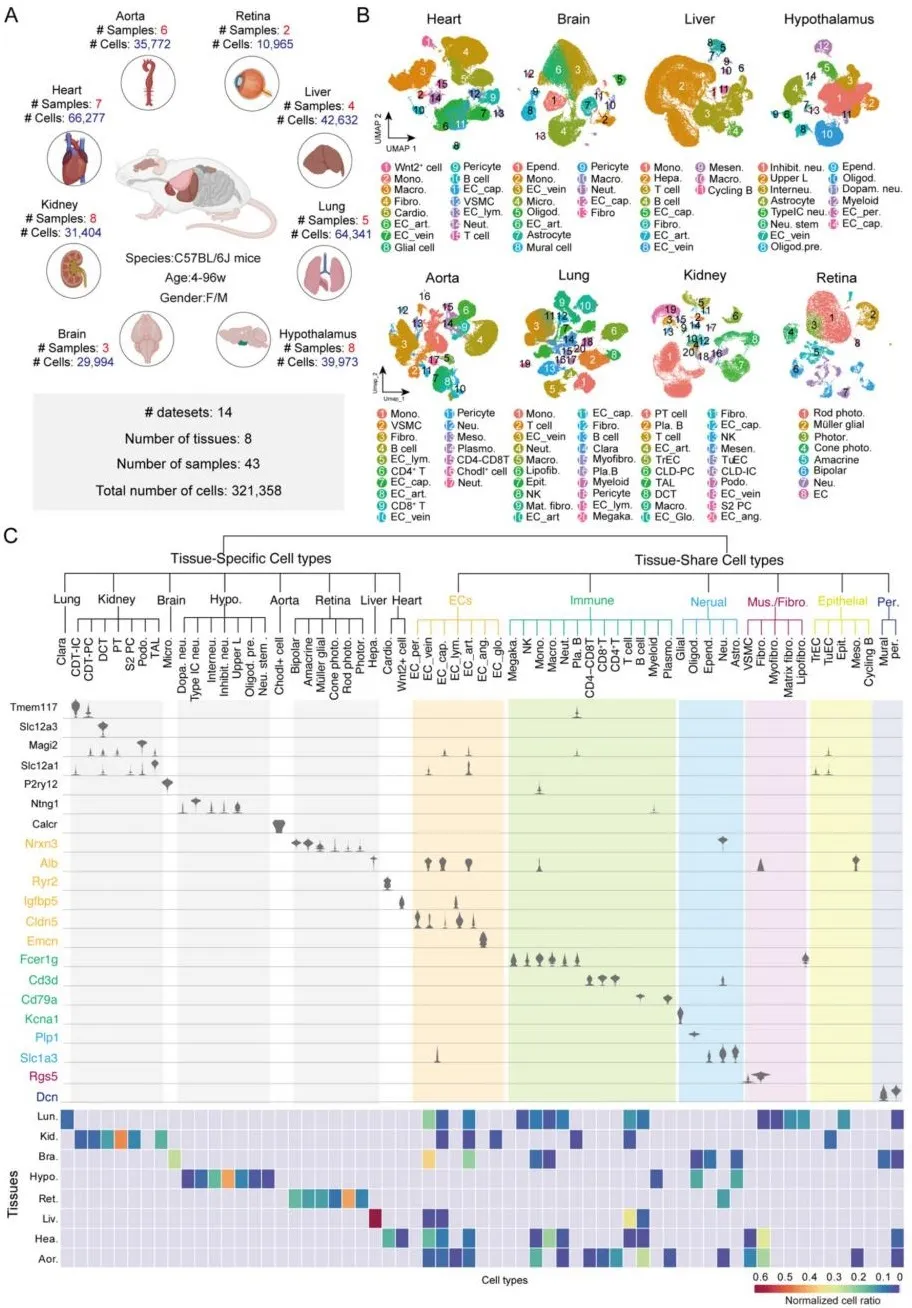
图1. 研究构建的单细胞分辨率的多血管器官型图谱
本研究的主要核心发现体现在以下四个方面:一是首次构建器官型血管系统单细胞图谱。研究整合了8个组织(心、脑、肾、肺、肝、视网膜、主动脉、下丘脑)的14个单细胞转录组数据,构建了包含63种细胞类型的器官型血管系统单细胞图谱。其中,血管内皮细胞(ECs)被鉴定为核心细胞类型,进一步细分为动脉EC、静脉EC、毛细血管EC等亚型,揭示了不同器官中ECs的高度异质性及其组织特异性分布规律。二是系统性解析细胞间通讯(CCI)网络。①ECs的核心作用:ECs是血管内最主要的通讯细胞,通过配体-受体相互作用(如LAMININ、COLLAGEN、JAM等信号通路)与免疫细胞、成纤维细胞、平滑肌细胞等交互,调控干细胞分化、免疫应答及血管稳态;②高频与低频通讯通路的分层:研究发现,仅8条通讯通路(如ANGPT、CDH、COLLAGEN等)在所有8个组织中共享,而多数通路具有组织特异性。高频通路主要参与基础生理功能(如发育、分化),低频通路则与免疫调节相关;③跨器官通讯特征识别:各器官功能发挥主要依赖于高频受配体对,而低频受配体对可能在特定的病理条件下或特殊生理事件中起到作用。相对而言,在疾病状态下,高频受配体对可能是多器官共病的关键靶点。三是阐明糖尿病对心脏与肾脏通讯网络的扰动机制。糖尿病显著改变心肌细胞、巨噬细胞与成纤维细胞间的通讯强度,尤其是与炎症和纤维化相关的通路(如MIF-CD74_Cxcr4、Spp1-Itga9_Itga1)下调。糖尿病增强了不同EC亚型间的通讯(如Col4a3-Cd44、Col4a3-Itga1_Itgb1),促进胶原合成与肾脏纤维化。26条在心脏与肾脏中均异常的通讯通路被锁定,其中BMP信号通路成为核心节点,相关分子BMP6、Bmpr1a可能是糖尿病心肾并发症的治疗靶标。四是揭示SGLT2i作用于糖尿病心肾并发症的靶向机制。snRNA-seq分析显示,SGLT2i(达格列净)有效改善了糖尿病介导的心脏异常通讯,通过抑制BMP6及其受体表达,显著改善糖尿病模型小鼠的心脏与肾脏病理损伤。
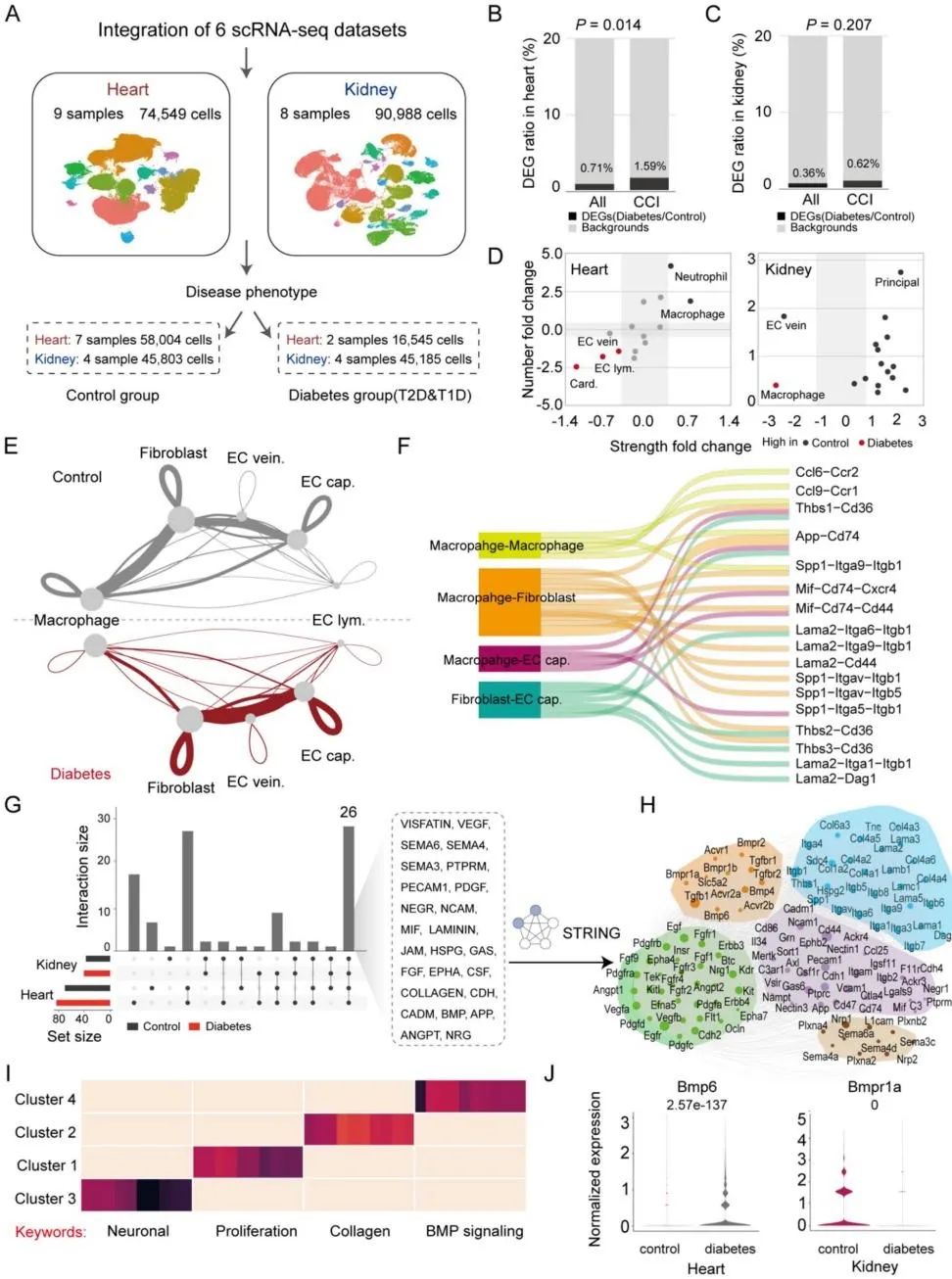
图2. 糖尿病心肾共病状态下CCI的变化
本研究创新性地绘制了跨器官血管系统的细胞通讯网络,发现内皮细胞(ECs)是血管系统细胞间通讯(CCI)的核心枢纽,其配体通过与多种细胞受体互作调控干细胞分化、免疫调节等关键生物学过程。研究从细胞通讯角度揭示了不同EC亚型的功能异质性—动脉EC通过BMP/JAM信号调控血管生成,而淋巴EC则通过IL2/RELN通路参与免疫调节,这为理解血管细胞的功能分化和组织特异性损伤机制提供了新视角。针对糖尿病心肾并发症这一临床难题,研究通过跨器官CCI分析发现BMP信号通路是介导糖尿病心肾损伤的关键通路,其中BMP6及其受体Bmpr1a在糖尿病心肾组织显著上调,而SGLT2抑制剂可通过调控BMP6表达改善器官损伤,这为糖尿病并发症的精准治疗提供了全新靶点。研究还揭示了糖尿病状态下心肾器官间通讯的病理重构特征:心脏中巨噬细胞-成纤维细胞互作减弱而内皮-成纤维细胞胶原信号增强,肾脏中不同EC亚型间胶原信号异常活化,这些发现系统阐释了糖尿病导致多器官纤维化的细胞互作机制。
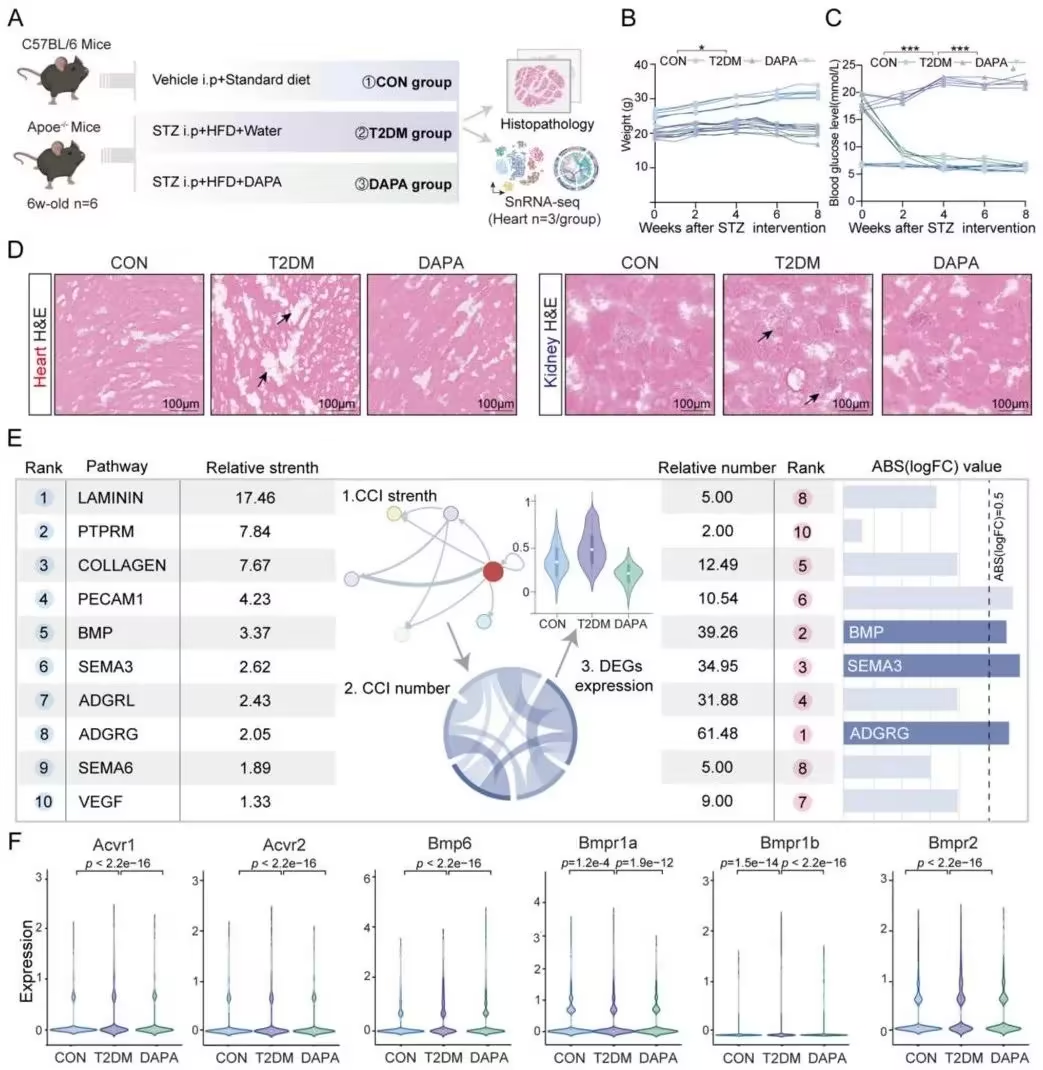
图3. 糖尿病及治疗过程中CCI网络的变化
本研究不仅首次从单细胞层面解析了器官特异性血管系统的细胞通讯规律,更重要的是建立了糖尿病多器官并发症的细胞互作理论框架,为DPD的早期预警、靶向干预及SGLT2抑制剂的机制研究提供了重要的科学依据,对推动糖尿病泛血管并发症的精准防治具有重要临床意义。
中国中医科学院西苑医院博士研究生王文婷和综合内科主治医师刘艳飞为该项研究的共同第一作者,刘玥主任医师为独立通讯作者,本研究得到中国中医科学院卓越青年科技人才专项、国家自然科学基金项目及中国中医科学院西苑医院高水平临床研究和成果转化能力试点建设项目的资助。
原文链接:
https://doi.org/10.1186/s12933-025-02655-2


