Lancet:这种微创消融法,有望实现高血压和原发性醛固酮增多症临床治愈
时间:2025-02-16 12:08:30 热度:37.1℃ 作者:网络
原发性醛固酮增多症是最常见的继发性高血压,与原发性高血压患者相比,心脑肾等靶器官受损更为严重。原发性醛固酮增多症肾上腺皮质自主分泌醛固酮,导致体内潴钠排钾,血容量增多,肾素-血管紧张素系统活性受抑制,临床主要表现为高血压和低血钾。过去,原发性醛固酮增多症的治疗方式仍以盐皮质激素受体拮抗剂和全肾上腺切除术为主。然而,通过药物治疗患者耐受性差,手术治疗则属侵入性治疗,且依从性差。
内窥镜超声引导射频消融术(EUS-RFA)一种简单、微创的靶向热疗法,该疗法有望作为全肾上腺切除术替代方案,治疗单侧分泌醛固酮腺瘤。近期,发表在Lancet杂志的一项题为“Endoscopic, ultrasound-guided, radiofrequency ablation of aldosterone-producing adenomas (FABULAS): a UK, multicentre, prospective, proof-of-concept trial”的研究,旨在确定EUS-RFA治疗单侧分泌醛固酮腺瘤的安全性和疗效。

在这项研究中,研究人员在英国的三个中心开展了一项可行性研究,将 EUS-RFA 作为左侧分泌醛固酮腺瘤的一种非手术保肾上腺治疗方法。符合条件的参与者为 18 岁或以上患者,根据内分泌学会的标准确诊为原发性醛固酮增多症,并通过 AVS 或 PET-CT 确诊为左侧分泌醛固酮腺瘤。
患者招募分为三个阶段,在先前招募的小组中前4名患者的数据由独立的安全委员会审查后才继续进行。研究人员对患者进行了两次分子影像学检查,第一次是诊断和定位左侧分泌醛固酮腺瘤,第二次是量化可消融程度。在进行细针活检以确认左侧分泌醛固酮腺瘤后,研究人员使用内镜超声(EUS)技术精确定位肾上腺腺瘤,并通过射频消融(RFA)进行高温(约90°C)消融,以破坏腺瘤细胞,同时尽可能保留正常的肾上腺组织。
术后,研究主要终点为患者安全性,以消融术后 24 小时或 48 小时内发生预先指定的重大事件(胃和肾上腺穿刺:穿孔、大出血或主要器官梗塞)来判断。次要终点为3个月和6个月时对患者进行随访,评估其生化和临床改善情况。生化治愈的标准是患者的醛固酮-肾素比值显著下降,而临床治愈则主要体现在血压水平的降低或降压药物剂量的减少。
结果显示,从2018年2月21日至2023年2月10日,共筛选出44名患者,招募了28名参与者,其中75%男性,25%女性,平均年龄为57.7岁 ,57%白人,39%黑人,4%亚裔。在28名患者中,21名患者接受了EUS-RFA,7名患者因首次术后3个月经PET-CT检查发现分泌醛固酮腺瘤的消融率低于25%,而接受了第二次微创消融。在分泌醛固酮腺瘤的不同部位均可观察到治疗痕迹,每次治疗持续时间5~20秒不等。
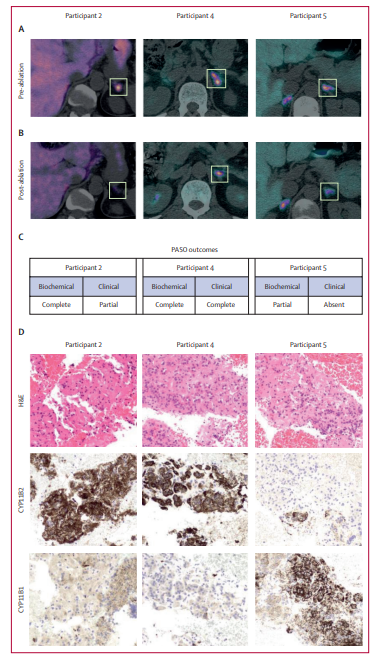
所有PET-CT阳性的结节均通过内镜超声探头识别,并成功通过活检和消融导管穿透。没有患者发生预先设定的主要风险,包括器官穿孔、出血或梗死等事件。微创消融后3个月,PET-CT阳性APA局部放射性示踪剂摄取量的减少与21名患者(75% [95% CI 55–91])的生化完全或部分缓解相关,并与12名患者的高血压完全或部分治愈(临床治愈)相关。
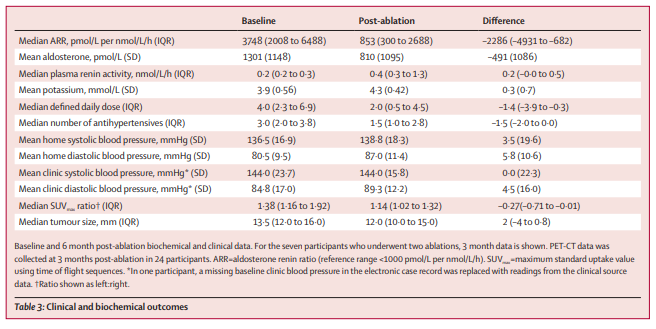
在术后6个月时,43%的患者达到了部分或完全的临床治愈标准,表现为血压显著下降,部分患者已无需继续服用降压药物。在4名患者中,影像学检查未能检测到残存的肾上腺腺瘤,并且他们在停用所有降压药后,收缩压稳定在135 mmHg以下,舒张压维持在85 mmHg以下。
总之,在左侧分泌醛固酮腺瘤(APA)的治疗中,内镜超声引导下的射频消融(EUS-RFA)作为一种微创治疗方法,显示了其在实现生化和临床治愈方面的潜力。通过EUS-RFA技术,可以精准地定位并消融大部分APA组织,从而有效控制甚至可能彻底治愈APA以及相关的高血压问题。
原始出处
Argentesi G, Wu X, Ney A, et al. Endoscopic, ultrasound-guided, radiofrequency ablation of aldosterone-producing adenomas (FABULAS): a UK, multicentre, prospective, proof-of-concept trial. Lancet. 2025 Feb 7:S0140-6736(24)02755-7. doi: 10.1016/S0140-6736(24)02755-7.


