Adv Sci 西南医科大学谭晓秋/雷鸣/张春祥教授团队揭示心肌细胞PAK2调控心律失常的作用机制及干预价值
时间:2025-03-18 12:08:27 热度:37.1℃ 作者:网络
心脏性猝死是心血管疾病死亡的主要原因之一,而恶性室性心律失常是心脏性猝死的最常见原因。尽管现有的抗心律失常治疗手段在一定程度上有效,但它们在抗心律失常的同时也存在致心律失常的风险,亟需寻找新的干预策略和靶点。线粒体功能障碍被认为是心律失常发生的重要机制之一,而P21激活激酶2 (Pak2)在心脏保护中的作用逐渐受到关注。
2025年3月12日,西南医科大学谭晓秋/雷鸣/张春祥教授团队在Advanced Science杂志在线发表题为“P21-Activated Kinase 2 as a Novel Target for Ventricular Tachyarrhythmias Associated with Cardiac Adrenergic Stress and Hypertrophy”的论文,揭示了Pak2在心脏肾上腺素应激和肥厚相关的室性心律失常中的关键作用和干预价值,为治疗室性心律失常提供了新的潜在靶点。

该研究通过构建特异性敲除心肌细胞Pak2 (Pak2cko)和过表达(Pak2ctg)基因修饰小鼠,探讨了Pak2在急性肾上腺素应激和慢性主动脉缩窄(TAC)诱导的心脏肥厚中的抗心律失常作用。研究还开发了一种新型Pak2激动剂JB2019A,进一步验证了Pak2作为抗心律失常靶点的潜力。
1. 首先发现,心脏Pak2的缺失增加了小鼠在急性异丙肾上腺素(ISO)或慢性TAC (5周)刺激下的心律失常易感性(图1)。在异丙肾上腺素诱导的急性心脏应激下,Pak2cko小鼠的室性心律失常发生率显著增加。在TAC诱导的慢性心脏肥厚模型中,Pak2cko小鼠的心律失常发生率进一步增加,且心脏功能显著恶化。
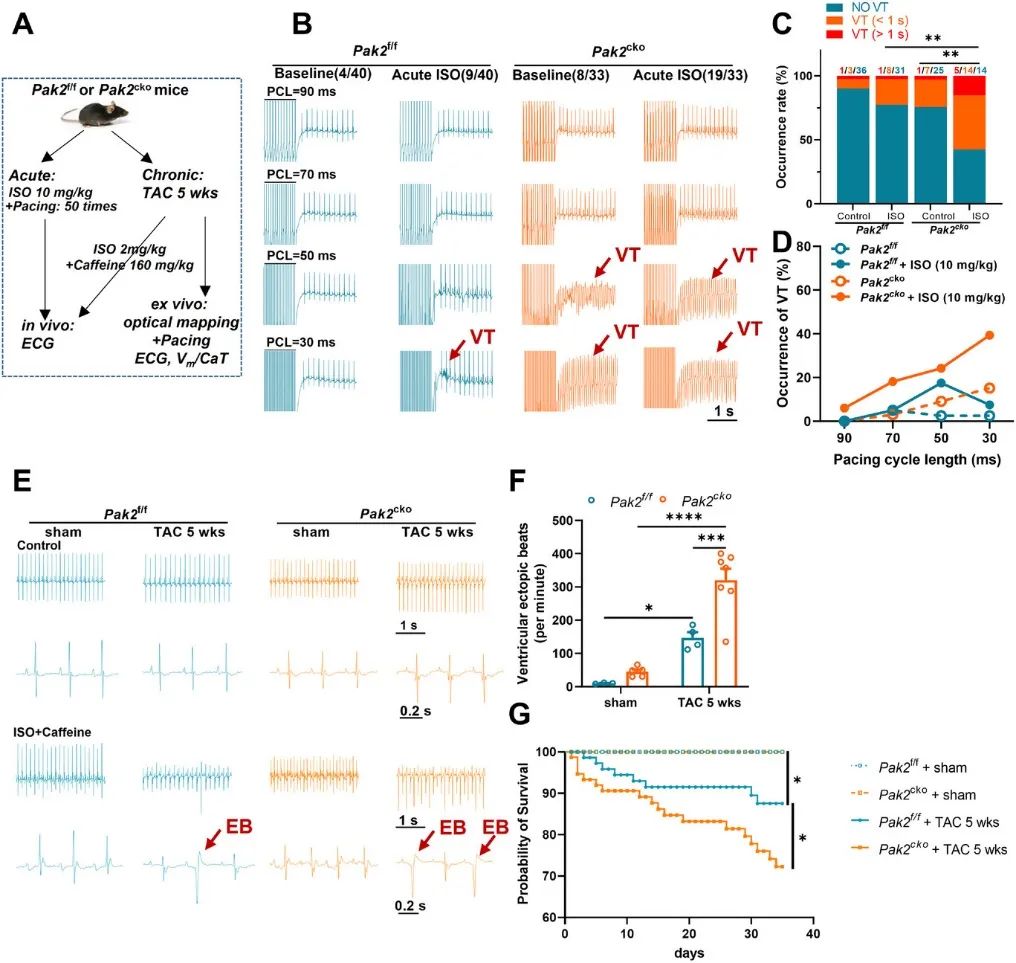
图1. 心脏Pak2的缺失增加了小鼠在急性异丙肾上腺素或慢性TAC刺激下的心律失常易感性
2. 使用离体心脏光标测技术同步检测心脏的膜电位和钙信号(图2)。Pak2cko小鼠在慢性TAC刺激下,离体心脏室性心律失常和钙交替的易感性明显增加。Pak2缺失显著加重了钙交替的频率,这也提示心脏的电活动稳定性恶化,进一步导致心律失常的发生。
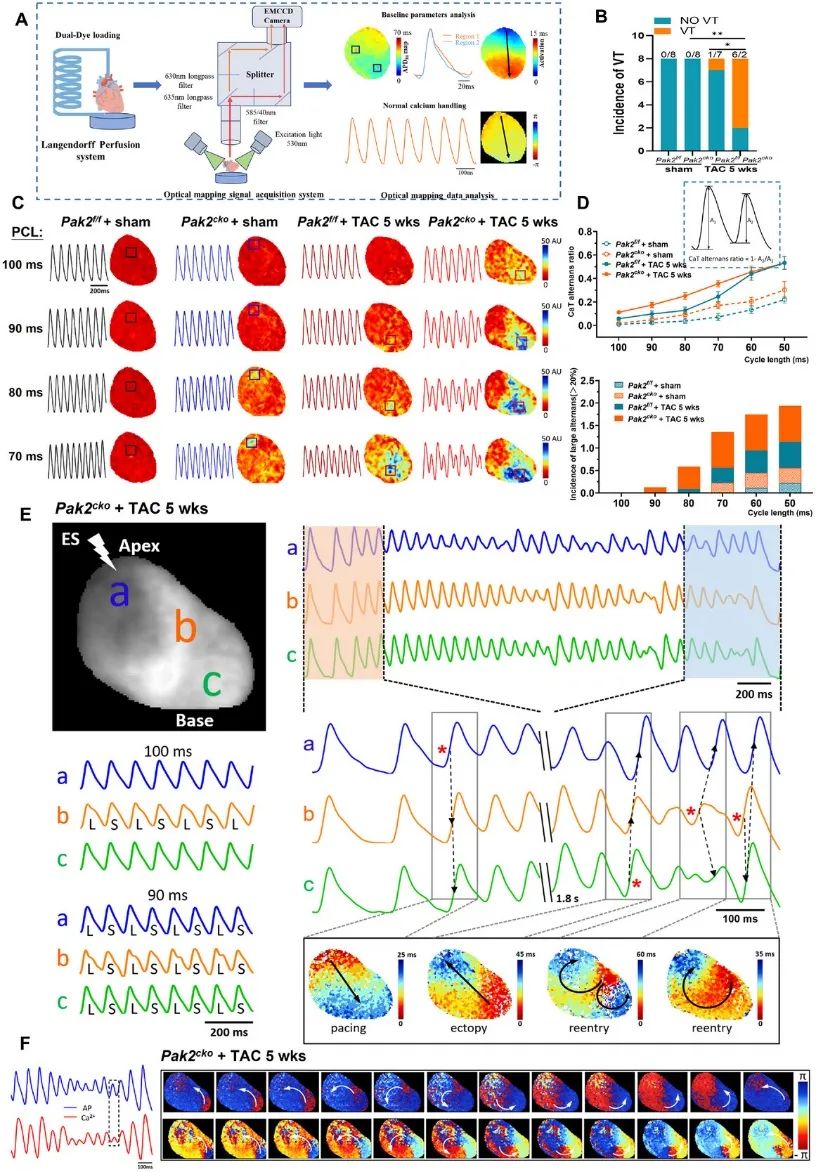
图2. 心脏Pak2的缺失加剧了TAC挑战下离体心脏室性心律失常和钙交替的易感性
3. 单个心肌细胞钙线扫结果提示,急性ISO和慢性TAC刺激,Pak2cko小鼠心室肌细胞有更高的自发性钙离子瞬变(SCT)和钙离子振荡(CO)发生率,这也提示心肌细胞Pak2缺失加重了ISO和TAC引起的心室肌细胞异常钙动力学变化(图3)。
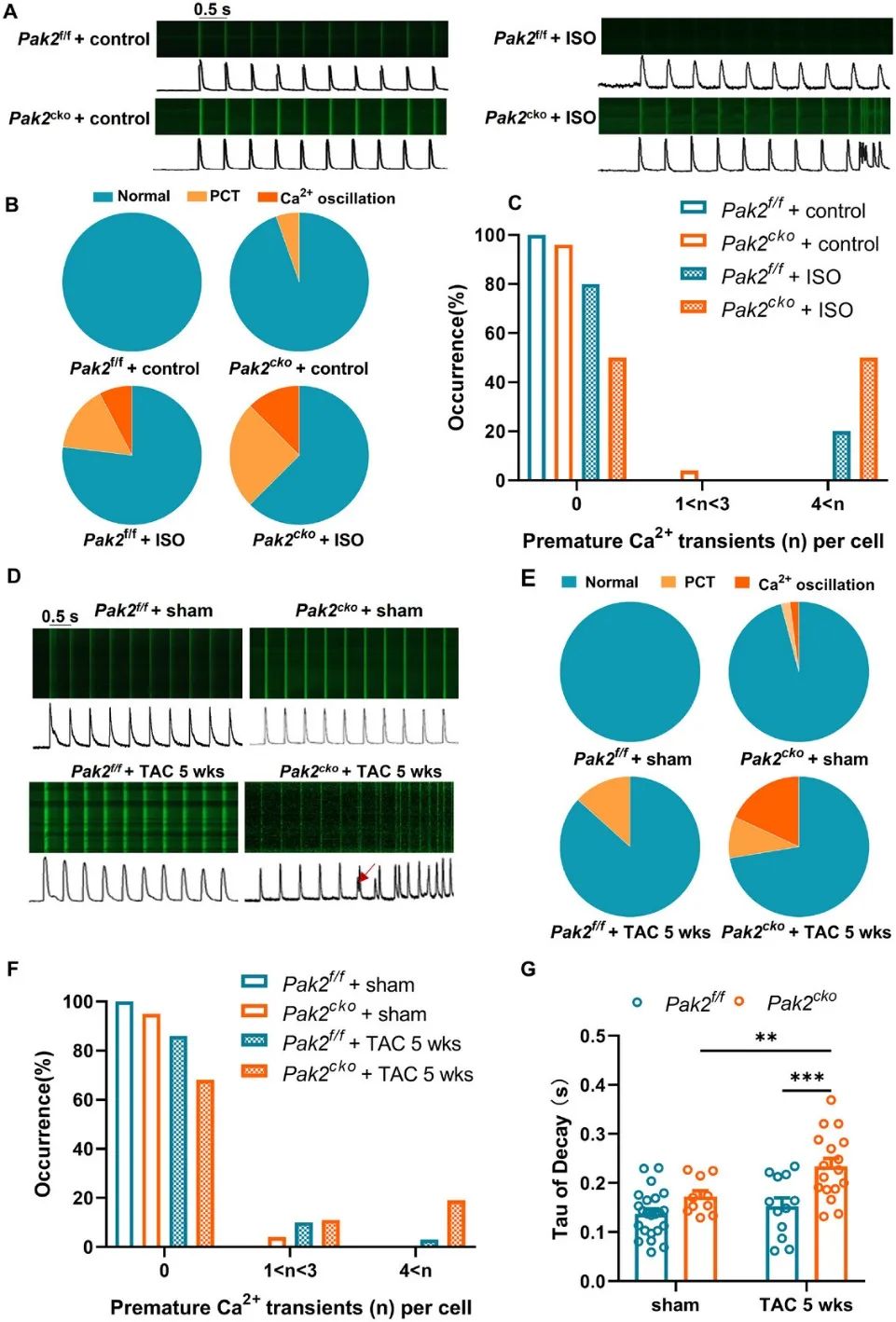
图3. Pak2缺失加剧了异丙肾上腺素和TAC诱导的心脏细胞内钙稳态紊乱
4. 进一步通过蛋白质组和磷酸化组学进行机制分析,结果提示,Pak2cko小鼠心脏线粒体生物合成障碍与氧化磷酸化增加(图4)。
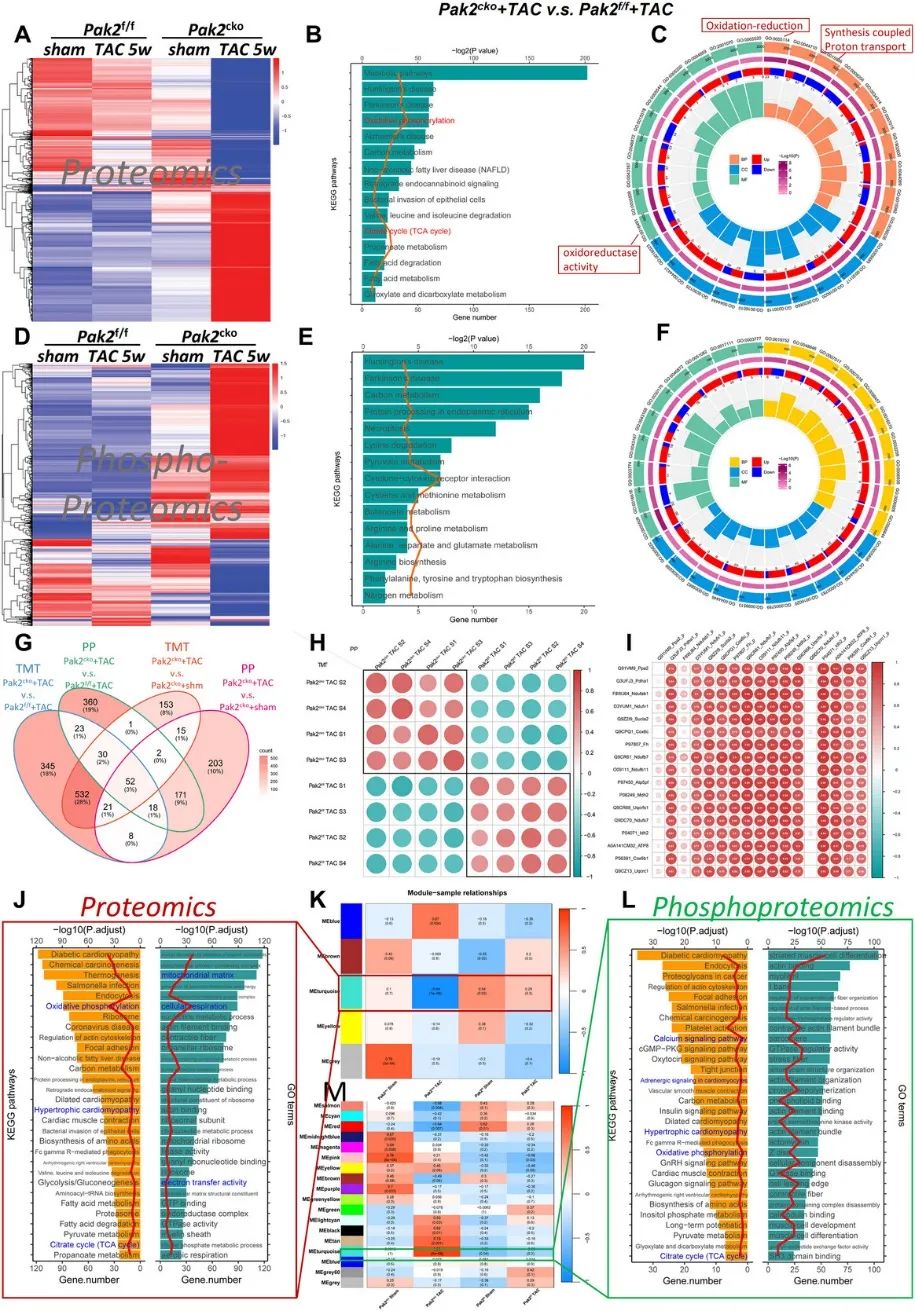
图4. Pak2缺失加剧了TAC诱导的心脏氧化应激
5. NOXs是心肌细胞ROS产生的主要来源。因此,该研究发现NOX4/ROS介导的CaMKII通路激活参与Pak2对TAC诱导的心肌电重构的影响(图5)。
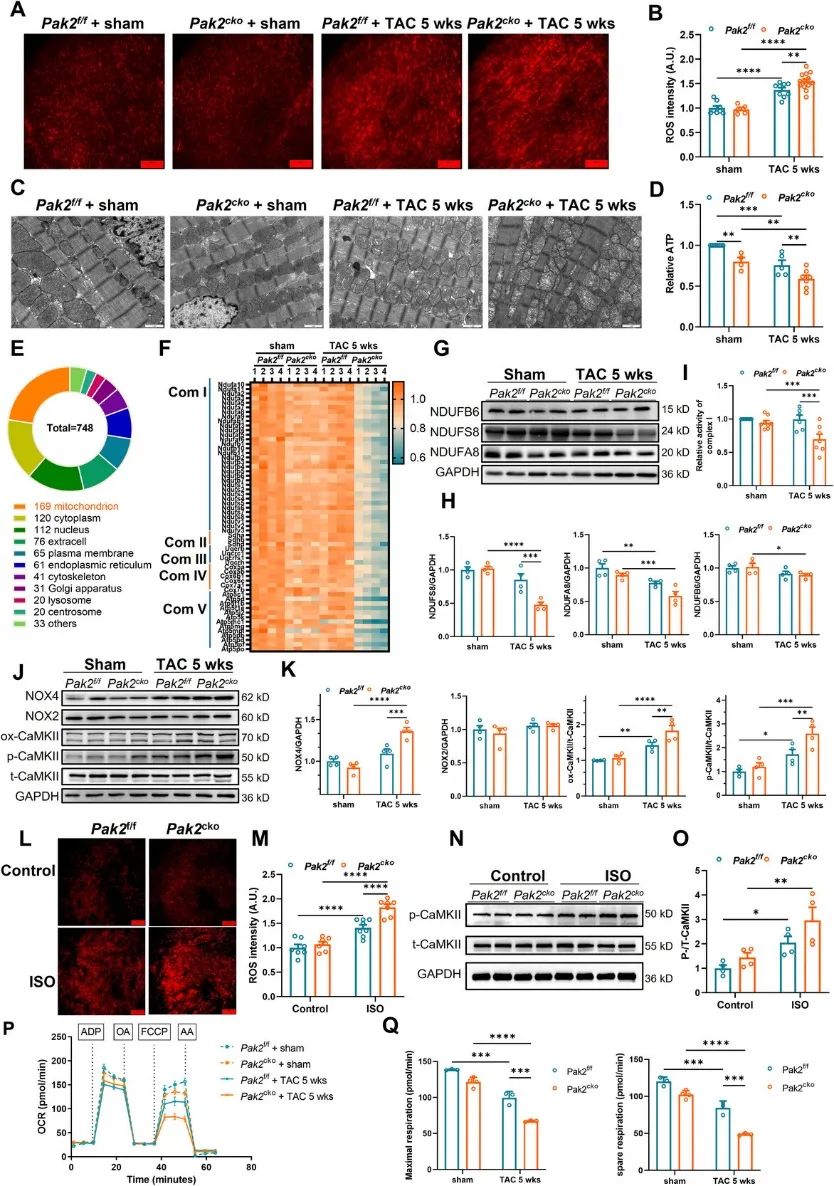
图5. Pak2缺失通过损害线粒体功能加剧心脏功能障碍
6. 构建心肌特异性Pak2过表达小鼠,结果发现Pak2过表达抑制TAC和急性ISO引起的心律失常和钙交替。进一步机制研究表明,Pak2过表达能够抑制TAC和ISO导致的氧化应激(图6)。
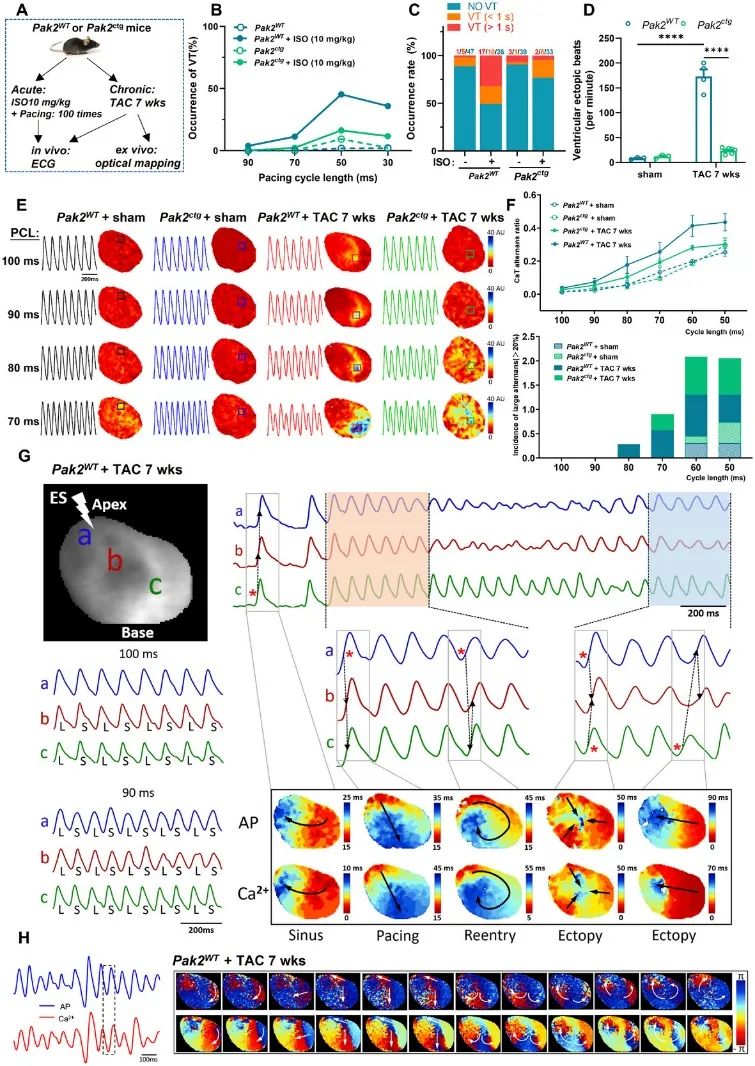
图6. 心脏特异性Pak2过表达减轻了异丙肾上腺素或TAC诱导的心律失常和钙交替
7. 为了研究Pak2作为心脏肥大和心律失常临床治疗的可行性,团队开发了小分子Pak2激活剂JB2019A。在急性异丙肾上腺素和慢性TAC刺激的情况下,JB2019A都显著降低了心律失常的发生率。机制研究显示,JB2019A也能够抑制TAC和ISO导致的氧化应激(图7)。
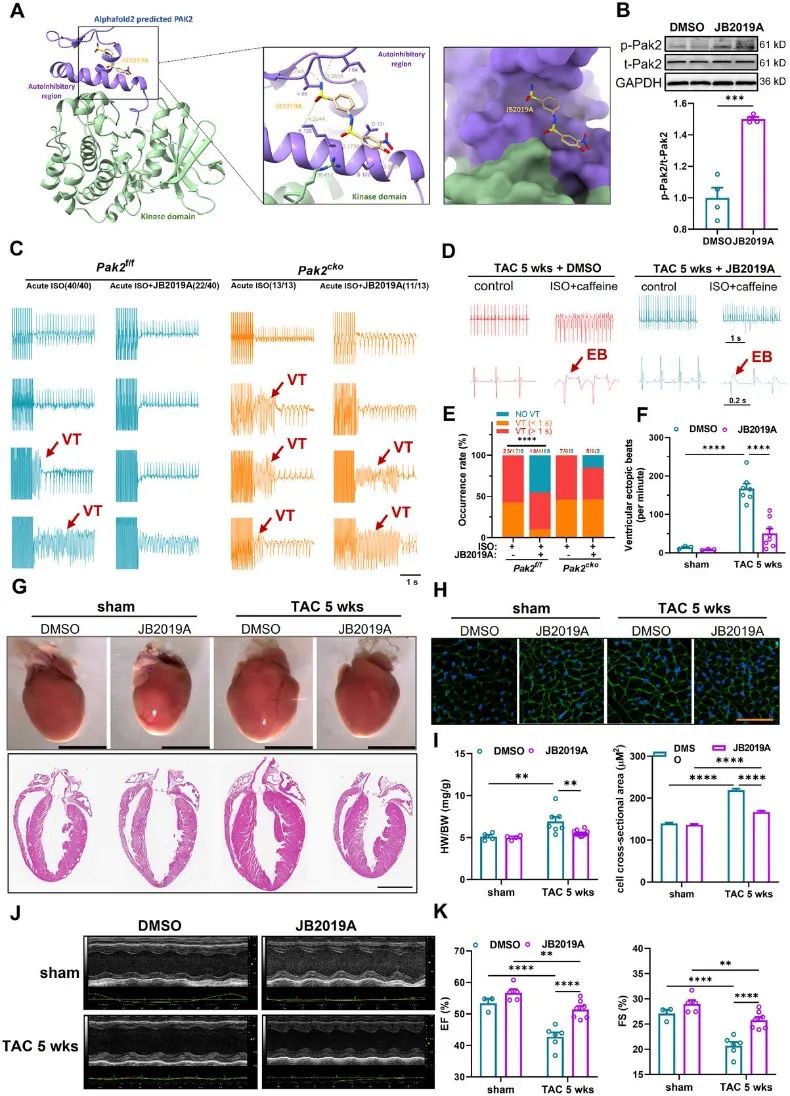
图7. Pak2激活剂JB2019A减轻了TAC诱导的心脏肥大和室性心律失常的易感性
综上,本研究首次揭示了Pak2在心脏应激和肥厚相关室性心律失常中的保护作用。Pak2通过调控线粒体功能和ROS生成,维持细胞内钙稳态,从而减少心律失常的发生。Pak2激动剂JB2019A的开发为未来抗心律失常药物的研发提供了新的方向。
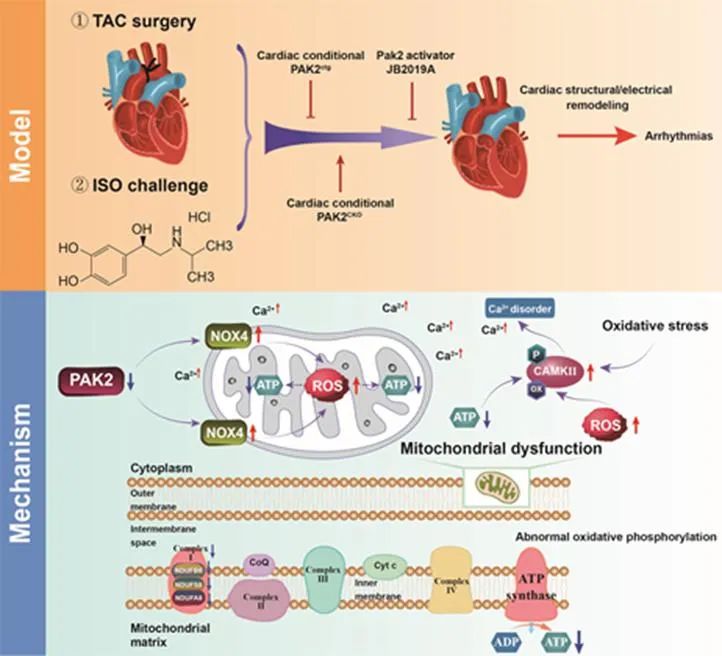
机制示意图
西南医科大学医学电生理学教育部重点实验室/基础医学院谭晓秋教授、张春祥教授和英国牛津大学雷鸣教授为该论文共同通讯作者,团队李涛副教授和研究生刘婷、王艳、李阳鹏为第一作者,研究得到了英国剑桥大学Christopher Huang教授、曼切斯特大学Xin Wang教授、四川大学华西医院李涛教授、西南医科大学附属医院万居易教授等的大力支持和国家自然科学基金、四川省科技计划项目等多个项目资助。
谭晓秋/雷鸣团队依托医学电生理学教育部重点实验室,已建立了稳定和成熟的整体心脏、心肌组织切片和培养心肌细胞的电生理平台。尤其是近年来建立的心脏光标测技术与电标测技术、膜片钳技术等有机结合,从整体、组织、细胞等不同层次和水平深入进行心律失常电生理机制研究。
原文链接:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202411987


