Nature Biotechnology:基因编辑再升级:RNA精准“微调”时代来临!
时间:2025-04-01 12:12:53 热度:37.1℃ 作者:网络
引言
近年来,基因编辑技术如同生物医学领域的一颗璀璨明星,吸引着全球科学家的目光。CRISPR-Cas9等DNA编辑技术的出现,为治疗遗传性疾病带来了前所未有的希望。然而,如同硬币的两面,DNA编辑技术在展现巨大潜力的同时,也面临着一些技术瓶颈,其中最令人担忧的就是“脱靶效应”(off-target editing)。这种效应指的是编辑工具可能会意外地修改基因组中非目标区域的DNA序列,从而引发潜在的副作用。研究人员一直在努力寻找更加精准、安全的基因编辑方法。
现在,一个令人振奋的消息传来!3月26日一项发表在《Nature Biotechnology》上的研究“Specific and efficient RNA A-to-I editing through cleavage of an ADAR inhibitor”,为我们带来了全新的解决方案。研究人员不再直接“操刀”DNA,而是将目光投向了它的“信使”——RNA(核糖核酸)。他们开发出了一种名为RNA转换腺嘌呤碱基编辑器(RNA transformer adenosine base editor,RtABE)的创新技术。这项技术能够对RNA上的特定碱基进行精确的修改,就像给RNA进行了一次精密的“微调”,更重要的是,它展现出了惊人的靶向性(specificity),有望彻底告别“脱靶”的困扰,为疾病治疗开辟一条更安全、更高效的道路。

告别“脱靶”烦恼:RtABE如何实现RNA的“指哪打哪”?
要理解RtABE的独特之处,我们首先需要了解DNA和RNA在细胞中的作用。DNA是细胞的“总司令部”,存储着所有的遗传信息。而RNA则像是“信使”和“执行官”,负责将DNA的指令传递给蛋白质工厂,并直接参与蛋白质的合成。许多疾病的发生,都与RNA分子的异常有关。因此,对异常的RNA进行精准的编辑和修复,同样可以达到治疗疾病的目的。
RtABE的核心优势在于其极高的靶向性。为了实现这一点,研究团队巧妙地利用了一类被称为ADAR抑制剂(ADAR inhibitors,ADIs)的分子。ADAR(adenosine deaminase acting on RNA)是一类天然存在的RNA编辑酶,而RtABE的关键组成部分正是ADAR2的脱氨酶结构域(ADAR2 deamination domain,ADAR2DD),它负责将RNA上的腺嘌呤(A)碱基转化为肌苷(I),而肌苷在细胞中会被识别为鸟嘌呤(G)。
那么,如何才能让ADAR2DD只在目标RNA位点发挥作用,而不去编辑其他RNA分子呢?这正是RtABE设计的精妙之处。
“分子锁”与“精准钥匙”:RtABE特异性编辑背后的设计
研究人员将ADI与ADAR2DD巧妙地融合在一起,形成一个“分子复合物”。在没有到达目标RNA序列时,ADI就像一把“分子锁”,紧紧地抑制住ADAR2DD的活性,使其无法进行RNA编辑。只有当RtABE成功结合到预先设定的目标RNA序列后,一个被称为TEV蛋白酶(TEV protease)的“精准钥匙”才会发挥作用。
具体来说,研究团队利用了MS2噬菌体衣壳蛋白(MS2 coat protein,MCP)与MS2 RNA发夹结构(MS2 RNA aptamer)的特异性结合,以及BoxB RNA发夹结构(BoxB RNA aptamer)与λ噬菌体N蛋白(λN peptide)的相互作用。他们将MCP融合到ADAR2DD-ADI复合物上,并设计了一段包含MS2和BoxB RNA发夹结构的引导RNA(engineered agRNA,eagRNA)。同时,他们还引入了TEV蛋白酶的N端片段(TEVn)和C端片段(TEVc),其中TEVc与λN肽融合。
当eagRNA与目标RNA结合后,MCP-ADAR2DD-ADI复合物会被招募到目标位点。与此同时,游离的TEVn也会扩散到目标位点,并与TEVc结合,形成完整的、具有活性的TEV蛋白酶(TEVp)。TEVp能够特异性地识别并切割ADI,解除ADI对ADAR2DD的抑制。一旦“分子锁”被打开,ADAR2DD就会被激活,开始高效地对目标RNA上的腺嘌呤进行编辑,将其转化为肌苷。
这种“先抑制后激活”的策略,就好比一把只有在特定条件下才能解锁的工具,确保了RtABE只在目标RNA位点进行编辑,从而实现了极高的编辑特异性,有效避免了“脱靶”效应的发生。
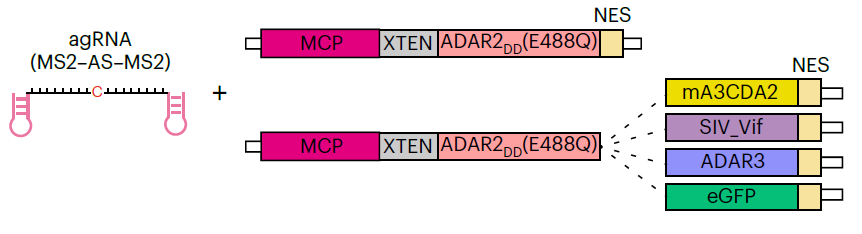
示意图(Credit: Nature Biotechnology)
小鼠模型显神威:RtABE成功治疗罕见病带来新希望
为了验证RtABE技术的有效性和安全性,研究团队选择了一种名为黏多糖贮积症I型(Hurler syndrome)的罕见遗传病小鼠模型进行实验。这种疾病是由于编码α-L-艾杜糖醛酸酶(α-L-iduronidase,IDUA)的基因发生突变,导致患者体内无法正常分解特定的糖类物质,进而引发一系列严重的健康问题,包括骨骼畸形、智力障碍和器官功能衰竭。
研究人员通过腺相关病毒(adeno-associated virus,AAV)将编码RtABE的遗传物质递送到患病小鼠的肝脏细胞中。肝脏是合成和分泌α-L-艾杜糖醛酸酶的主要器官。实验结果令人惊喜!研究发现,经过RtABE治疗后,小鼠肝脏细胞中α-L-艾杜糖醛酸酶的活性得到了显著恢复。这表明RtABE成功地对突变的RNA进行了编辑,产生了功能正常的酶。
更重要的是,研究团队对接受RtABE治疗的小鼠的多个组织(包括肝脏、脾脏、肾脏、心脏和大脑)进行了全面的脱靶编辑分析。他们利用高通量测序技术,检测了这些组织中是否存在非目标RNA的编辑事件。结果显示,与传统的RNA编辑方法相比,RtABE的脱靶编辑水平非常低,几乎可以忽略不计。这充分证明了RtABE具有出色的靶向性和安全性,为将其应用于临床治疗罕见病奠定了坚实的基础。
此外,研究人员还检测了接受RtABE治疗的小鼠的疾病相关指标。他们发现,经过治疗后,小鼠体内与黏多糖贮积相关的代谢产物水平显著降低,疾病症状得到了明显的改善。这些结果进一步证实了RtABE在治疗黏多糖贮积症I型方面的巨大潜力。
多重实验验证:RtABE展现高效性和广谱性
除了在黏多糖贮积症I型小鼠模型中的成功应用,研究团队还进行了多项额外的实验,以更全面地评估RtABE技术的性能。
他们设计了不同的引导RNA(eagRNA),靶向不同的RNA序列,发现在多种不同的序列背景下(包括UAN、AAN、CAN和GAN等),RtABE都能够高效地进行A-to-I的编辑。这表明RtABE具有广泛的适用性,可以用于编辑各种不同的RNA靶点。
为了进一步验证RtABE的特异性,研究人员还进行了敲低实验(knockdown experiment)。他们利用小干扰RNA(small interfering RNA,siRNA)敲低了目标RNA的表达,结果发现RtABE的编辑活性也随之显著降低。这表明RtABE的编辑是高度依赖于目标RNA的存在的,进一步证实了其靶向性。研究人员还通过蛋白质印迹法(Western blot)分析了在目标转录本被敲低时A3DADI的切割情况,结果与RT-qPCR数据一致,进一步支持了RtABE的作用机制。
此外,研究团队还对RtABE的组成部分进行了优化,例如对ADAR2DD进行了突变改造(E488Q),以进一步提高其编辑效率和特异性。他们还探索了不同的递送方式,例如利用腺相关病毒(AAV)进行体内递送,为未来的临床应用提供了更多的选择。
这些多方面的实验结果充分证明,RtABE是一种高效、特异性强、且具有广谱性的RNA编辑工具,在基础研究和疾病治疗领域都具有巨大的潜力。
RNA编辑潜力无限:未来医学领域的新星冉冉升起
DNA编辑技术无疑是基因治疗领域的重要里程碑,但RNA编辑作为一种新兴的技术,也展现出了独特的优势和广阔的应用前景。与DNA编辑相比,RNA编辑具有以下几个显著的特点:
更高的安全性:RNA的半衰期较短,编辑效果通常是暂时的,不会对基因组造成永久性的改变,从而降低了潜在的长期副作用风险。这对于一些只需要短期治疗的疾病来说,具有明显的优势。
更强的可调控性:RNA的表达水平和修饰状态可以受到多种细胞信号和环境因素的调控,这为疾病治疗提供了更加灵活的策略。例如,我们可以根据疾病的进展情况,动态地调整RNA编辑的效率。
更广泛的应用范围:除了遗传性疾病,RNA编辑在感染性疾病、神经退行性疾病、癌症等多个领域都展现出了巨大的潜力。例如,通过编辑病毒的RNA,可以抑制病毒的复制;通过编辑肿瘤细胞的RNA,可以抑制肿瘤的生长和转移;通过编辑神经细胞的RNA,可以延缓神经退行性疾病的进展。
RtABE技术的出现,正是RNA编辑领域的一项重大突破。它解决了RNA编辑长期以来面临的关键挑战——特异性问题,使得RNA编辑技术在疾病治疗方面迈出了坚实的一步。许多研究人员认为,随着技术的不断成熟和完善,RNA编辑有望成为继DNA编辑之后,基因治疗领域的又一个“风口”,为人类健康带来更多的福音。
精准医疗新篇章:RtABE引领基因治疗迈向更安全高效的未来
总而言之,这项名为RtABE的RNA编辑新技术,通过巧妙地融合ADAR抑制剂和TEV蛋白酶系统,实现了对RNA的精准编辑,有效克服了传统基因编辑技术可能存在的“脱靶”难题。在黏多糖贮积症I型小鼠模型中取得的成功,充分证明了RtABE在治疗遗传性疾病方面的巨大潜力。
这项研究的突破性进展,不仅为治疗罕见病带来了新的希望,也为RNA编辑技术在更广泛的疾病领域应用奠定了坚实的基础。我们有理由相信,随着未来研究的不断深入和技术的持续发展,RNA编辑技术将在精准医疗时代发挥越来越重要的作用,为人类的健康福祉贡献力量。让我们共同期待这项令人兴奋的技术能够早日走向临床,造福更多的患者!
参考文献
Li G, Chen G, Yuan GH, Wei J, Ni Q, Wu J, Yang B, Yang L, Chen J. Specific and efficient RNA A-to-I editing through cleavage of an ADAR inhibitor. Nat Biotechnol. 2025 Mar 26. doi: 10.1038/s41587-025-02591-2. Epub ahead of print. PMID: 40140558.


