【麻海新知】择期成人患者服用GLP-1RA、GIP RA和SGLT2i的围手术期管理:一项多学科共识声明
时间:2025-03-03 12:18:50 热度:37.1℃ 作者:网络
新型抗高血糖药物越来越多地用于治疗糖尿病和非糖尿病,降低心血管、肾脏的发病率和死亡率,包括:基于肠促胰岛素的激素疗法,即胰高血糖素样肽-1受体激动剂(GLP-1RA);双葡萄糖依赖性促胰岛素肽受体激动剂(GIP)/GLP-1 RA;以及钠-葡萄糖共转运蛋白-2(SGLT2)抑制剂。
除糖尿病外,GLP-1 RA最常见的适应证是肥胖,进一步的适应证正在研究中,包括:骨关节炎、阻塞性睡眠呼吸暂停、代谢功能障碍相关脂肪变性肝病、代谢功能障碍相关脂肪性肝炎。因此,接受手术或其有麻醉需求的人服用此类药物的可能性不断增加。由于胃排空延迟,反流和/或肺误吸,该领域缺乏高质量的证据,既往文献对服用GLP-1RA的患者的围手术期管理提出了相互矛盾的建议,关于最安全的围手术期管理策略存在不确定性。
SGLT2抑制剂现在也被许可用于治疗非糖尿病患者的心力衰竭和慢性肾病,这些药物适应证的增加导致需要手术的患者中使用这类药物的人数增加。由于这些药物可能导致糖尿病酮症酸中毒(DKA),特别是血糖正常的DKA(血糖浓度<11.0 mmol/L),针对围手术期管理中出现了相互矛盾的建议。
本共识旨在代表麻醉医师协会、英国临床糖尿病学家协会、英国肥胖和代谢外科协会、围手术期护理中心、英国糖尿病学会住院患者护理联合委员会、皇家麻醉医师学院和肥胖与减肥麻醉学会,针对服用GLP-1RAs或SGLT2抑制剂的择期成人患者围手术期管理发表的一份多学科共识声明。相关内容发表在2025年1月的Anaesthsia杂志。

方法
参加制定本共识声明的包括外科医师、麻醉科医师、内科医师、药剂师以及有相关经验的患者代表。进行定向文献综述以获取相关证据,支持建议的制定。第一轮,分发给所有作者所有建议,作者匿名对每条建议进行评价,选择“同意”、“不同意”或“需要修改”,同时在 Excel表格中提供匿名评论。第二轮,≥75%的建议保持不变并进入下一轮;50% ~ 74%的建议进行修改;<50%的建议被认为不适合推荐。第二轮的流程与第一轮类似,在每轮之后公开匿名评论和完整的投票结果。最后,举行一次虚拟圆桌会议,以达成最终共识并批准。最终建议提交给支持该共识的组织以供批准。
胰高血糖素样肽-1受体(GLP-1)和依赖葡萄糖的胰岛素促进多肽(GIP)受体激动剂
肠促胰岛素激素GLP-1和GIP从小肠内壁分泌,GLP-1由整个肠道的L细胞分泌,在回肠远端浓度较高;GIP由十二指肠和空肠的K细胞分泌,两者都参与肠道内葡萄糖的调节。除了引起β细胞胰岛素分泌的葡萄糖依赖性增加,还具有多种其他影响,包括:改变胰岛α细胞分泌胰高血糖素:GLP-1减少胰高血糖素分泌,而GIP则增加胰高血糖素分泌;延缓胃排空,从而减缓餐后血糖上升;还能通过激活下丘脑饱腹中枢发挥中枢作用,这也是这些药物在初始使用或剂量增加时常见恶心这一不良反应的主要原因,同时,对饱腹感的影响也是这些药物用于成功减肥的原因之一;此外,这两种激素都能增加胰岛素敏感性,尽管其机制不同:GLP-1主要作用于肝脏,而GIP则作用于骨骼肌。患有2型糖尿病或肥胖的人血浆中肠促胰岛素激素的浓度与正常人相比非常低。
GLP-1受体激动剂利拉鲁肽、司美格鲁肽和度拉糖肽越来越多地被用于治疗糖尿病患者,能改善血糖控制并降低主要不良心血管事件的风险(Table1)。尽管心血管结局的研究结果尚未公布,但GLP-1/GIP受体激动剂替西帕肽已被证明能显著改善糖尿病人群和非糖尿病人群的心血管疾病替代指标。此外,由于替西帕肽对减肥的显著益处:在非糖尿病的人群中,平均体重减轻超过初始体重的20%(72周内)。许多此类药物现在也被批准用于治疗糖尿病/非糖尿病的肥胖人群。
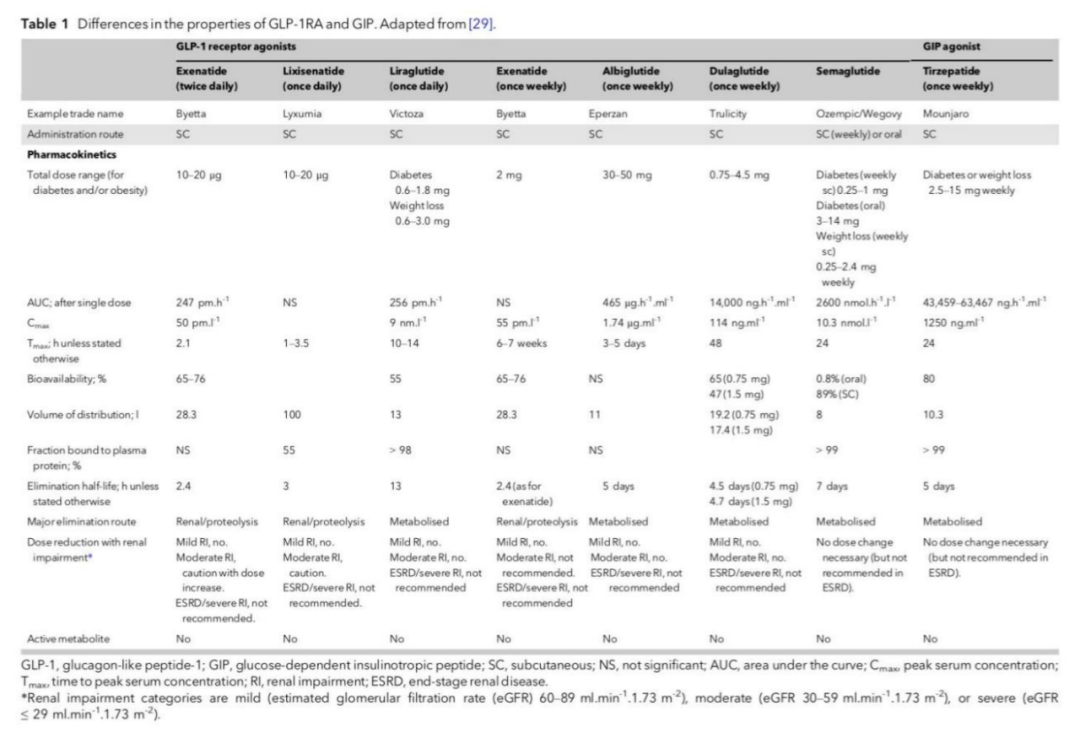
因此,建议在已知有心血管疾病和/或肥胖危险因素的2型糖尿病患者中早期使用肠促胰岛素疗法。数据显示在围手术期中,临时使用(手术干预前后几小时内)与以下方面结局相关:改善围手术期血糖控制;降低术后胰岛素需求;降低低血糖风险;以及改善心血管结局。
一些研究表明,围手术期GLP-1受体激动剂与肺部误吸的风险增加有关,在择期手术中报告的OR(95%CI)为10.23(2.94-35.82),内窥镜检查中的HR(95%CI)为1.33(1.02-1.74)。关于风险的严重程度,数据存在相互矛盾。欧洲药品管理局药物警戒风险评估委员会强调:服用GLP-1 R受体激动剂的人胃排空可能会延迟。
在长期使用GLP-1受体激动剂的人群中,关于肺部误吸风险的确定性较小,长期使用对胃排空的影响尚不清楚。由于其延缓胃排空作用以及早期关于肺部误吸的病例报告,美国麻醉师协会(ASA)建议这些药物应在手术前一天停止(每日一次用药人群)或在手术前一周停止(每周一次用药人群)。理论上是最小化因胃排空不完全而导致在麻醉诱导时发生肺部误吸的风险。但必须考虑多个因素,包括药物特性、个体患者特征、手术类型以及麻醉方式。重点是必须考虑停药的不良影响(Table 2)。

有明确证据表明,GLP-1 RAs在大多数情况下与胃排空延迟有关,可通过内镜检查(包括胶囊内镜)、超声检查、放射性碳标记摄入、对乙酰氨基酚摄入以及闪烁扫描证实。但大多数研究观察对象为近期开始使用GLP-1 RAs的影响,而不是围手术期的长期使用。最近有围手术期环境的前瞻性数据强调:近期和持续使用时残余胃内容物的风险增加,同时长期使用GLP-1 RAs可能会出现快速耐受,所以,近期开始使用或剂量增加时的胃排空延迟可能具有特别重要的临床意义。长期使用GLP-1 RAs对需要接受麻醉手术的糖尿病患者或肥胖患者的影响仍有待明确。有病例报告,在适当禁食患者中,无论是接受镇静或全身麻醉进行择期手术/内镜检查,都出现了胃排空延迟。
考虑GLP-1 RAs的药代动力学和药效动力学,这些药物的半衰期各不相同,从几小时到一周不等(Table1)。如果一个每周服用1mg司美格鲁肽治疗糖尿病的人停药一周,血浆浓度将与每周服用0.5mg未停药的人相同。数据表明,GLP-1 RAs停用的时间越长,胃残余胃内容物增加的可能性越低。然而,即使停药一周,对于适当禁食手术的患者来说,残余胃内容物的风险仍然很高。有病例报告表明,完全停用GLP-1 RAs一周也并不足以降低肺部误吸风险。最近有数据表示,停用GLP-1 RAs长达三周也与胃容量增加有关。
使用GLP-1 RAs的患者胃排空延迟的风险因素:药物、糖尿病和/或肥胖、手术性质和麻醉因素。急诊手术本身是肺部误吸的风险因素,使用镇静或不进行气管插管的手术也可能带来更大的肺部误吸风险。
胃内容物是饱胃的先决条件,但本身不会导致误吸,是发生误吸的许多变量之一。有数据表明,遵循择期手术禁食指南的患者中,6%~16%的患者有胃内容物或与更高误吸风险相关的胃容量。强调床旁胃超声在进行风险分层和适当干预以避免不良后果方面的实用性。虽然尚未广泛使用,但床旁超声在围手术期管理中的作用越来越大。
对疑似饱胃的患者进行快速顺序诱导也存在潜在风险,包括气管插管困难和失败、食管插管、过敏反应、诱导期的术中知晓以及气道创伤。快速顺序诱导只是一种干预措施,可以实施其他干预措施来降低误吸的风险,包括:使用促胃动力药物(诱导前1~2h给予红霉素3 mg/kg);选择气管插管而不是声门上气道装置;正确使用环状软骨压迫;头高位;以及在麻醉诱导和气管拔管前使用口胃管或鼻胃管。没有数据证明延长禁食时间的安全性或有效性。
同时还应考虑停止使用药物的影响。围手术期高血糖与伤害有关,包括(但不限于):住院时间延长、手术部位感染、急性肾损伤、急性冠状动脉综合征、重症监护转入、或呼吸机使用时间、因血糖升高导致手术延迟或取消,都可能导致成本增加、床位周转减慢、对医疗经济产生影响。
英国糖尿病患者手术围手术期管理指南包含了所有糖尿病药物术前操作的实用指南,包括术前一天或手术当天(无论上午或下午),对于没有糖尿病并且正在使用这些药物减肥的人来说,围手术期患高血糖症的风险可能会增加。
应激性高血糖是指之前不知道患有糖尿病的人群中血糖浓度暂时升高。最常发生在有发展为2型糖尿病风险的人群中,包括但不限于:肥胖人群、有妊娠糖尿病史、有糖尿病家族史、长期使用糖皮质激素、年龄>40岁、或南亚裔人群。发生应激性高血糖的患者比患有糖尿病的患者围手术期不良结局风险更高。既往不知道患有糖尿病但出现高血糖的患者,其血糖监测频率并不像患有糖尿病频繁,即使血糖控制不佳,也没有开始干预。因此,使用GLP-1RA治疗肥胖的人有发生应激性高血糖的风险,应该定期进行血糖测量,如果发生高血糖,应立即进行干预。肥胖患者使用GLP-1RA或停止和重新开始GLP-1RA对患应激性高血糖风险的影响尚不清楚。
使用胰高血糖素样肽-1受体激动剂和葡萄糖依赖性促胰岛素肽的围手术期管理建议:

钠-葡萄糖共转运蛋白- 2抑制剂
钠-葡萄糖共转运蛋-2(SGLT2)抑制剂通过抑制近曲小管的重吸收和诱导糖尿来降低血糖水平,模拟饥饿状态。在健康个体中,血糖是胰岛素分泌的主要驱动力,如果由于糖尿导致血糖浓度下降,胰岛素分泌的驱动力也会减弱。如果没有胰岛素,葡萄糖进入细胞的能力也会降低。因此,细胞需要一种替代的能量底物,即酮体。随着胰岛素浓度的降低,胰高血糖素浓度增加,胰岛素/胰高血糖素比例的变化使得脂肪细胞中的游离脂肪酸得以释放,这些脂肪酸随后被运输到肝脏并转化为酮体。因此,即使是健康个体,在饥饿状态下也会出现酮症,如果碳水化合物限制时间延长,酮体浓度可能会超过6 mmol/L。酮体达到浓度所需的时间内,允许肾脏和呼吸系统进行充分的代偿,以防止代谢性酸中毒,所以,对于无糖尿病且没有其他伴随疾病的健康个体并不危险。
SGLT2抑制剂用于糖尿病管理已有数年历史,但由于其额外的心血管益处,现在与二甲双胍并列为心血管高风险或已有动脉粥样硬化疾病、心力衰竭或慢性肾脏疾病患者治疗的首选药物。
SGLT2抑制剂诱导的糖尿伴随着渗透性利尿,导致循环血量减少、血压降低以及心脏负荷和肾小球压力的降低。新数据表明,轻度高酮血症可以提高心肌细胞线粒体的效率和功能。综合来看,这些作用对心力衰竭有积极影响,并有助于防止慢性肾脏病的进展,此类药物也因此被批准用于上述适应证,无论患者是否患有糖尿病。
此类药物的半衰期均为12~13h,且没有活性代谢产物。但在患或不患2型糖尿病的人群中,对尿葡萄糖排泄的药效作用明显超过了有效的血浆药物浓度。尽管停药24h后仅剩下25%的血浆药物浓度,但48h后尿葡萄糖排泄量仍会继续增加。如果SGLT2抑制剂停药72h,循环中仍有<1%的药物残留,尿葡萄糖排泄恢复到基线水平。从理论上讲,尿糖排泄的药理学效应可能与胰岛素/胰高血糖素比例的变化有关,因此酮体生成的风险可能与药理学效应而非血浆药物浓度的关系更为密切。在围手术期,对于这些药物术前停药时间的建议存在差异,美国药品和保健品管理局(MHRA)的指导建议,在计划进行大手术的前1d应停药,而美国食品和药物管理局的指导建议在任何择期手术前3~4d考虑停药。
关于围手术期使用SGLT2抑制剂的主要问题是糖尿病酮症酸中毒(DKA)的发生,特别是正常血糖性DKA和酮症酸中毒,无论患者是否患有糖尿病,血糖浓度均为正常水平(即<11.0 mmol/L)。由于血糖浓度降低,以及由此导致的胰岛素/胰高血糖素比例的变化和酮症倾向,任何导致应激激素产生的生理应激增加都会进一步推动高酮血症的发展。由于酮体浓度上升迅速,且无法对由此产生的酸血症进行代偿,酮体浓度可能会迅速上升至>3.0 mmol/L,pH值可能会降至<7.3,这是定义DKA的阈值。其中的“D”表示血糖可能>11.0 mmol/L,或者有糖尿病病史。
有数据显示,围手术期使用SGLT2抑制剂的患者发生DKA的风险高于未使用该类药物的患者(每1000例患者中分别为1.02比0.69,OR 1.48,95%CI 1.02–2.15,p = 0.037)。对近100例围手术期DKA病例深层回顾表明,术前停药超过2d并未导致DKA的发生。其他研究表明,围手术期停用SGLT2抑制剂与高阴离子间隙酸中毒风险降低有关。数据还表明,急诊手术患者的围手术期酮症酸中毒发生率高于择期手术患者(1.1% vs. 0.17%),而在非手术环境中,糖尿病患者的酮症酸中毒发生率高于非糖尿病患者(1/339 vs. 1/15,592)。这些数据可能与显著的混杂因素有关,应避免将结果常规应用于临床实践。
时至今日,大众还认为没有糖尿病的人有足够浓度的胰岛素来预防严重的酮症,但有报道对此提出质疑,报告中描述的4名患者中,没有一人患有糖尿病,都出现了正常血糖性酮症酸中毒,其病理生理学保持不变。所以,即使在没有糖尿病的人群中,围手术期继续使用SGLT2抑制剂的患者需警惕这种罕见情况。
与停用GLP-1受体激动剂相关的围手术期高血糖的危害相同的论点也可以用于SGLT2抑制剂。数据显示,对于因心力衰竭而接受SGLT2抑制剂治疗的患者,停药可能与心力衰竭恶化有关。因此,需要在早期停药以防止酮症酸中毒的风险与因术前高血糖和术后并发症而推迟或取消手术的风险之间取得平衡。鉴于证据和药代动力学/药理学特性以及务实的考量,先前英国指南建议手术前1d停药仍然是可以接受的。如果药物在早上服用,且手术也在早上进行,这将相当于至少48h的间隔——如果是下午手术,则超过52h。如果在晚上服用,也至少有36h的间隔。
有报道显示,即使患者停用SGLT2抑制剂超过72h,术后仍可能发生酮症酸中毒,说明并发症的风险是连续的,而不存在不发生酮症酸中毒的明确阈值。在不可避免的长时间禁食期间,使用含葡萄糖的静脉输液来缓解酮体生成可能是有益的。
在某些类型的手术之前,包括减肥手术和一些腹腔镜手术,患者可能会开始一个极低能量饮食,也称为肝脏减容饮食。这种饮食主要是基于牛奶、酸奶和汤,通常每天摄入800~1000卡路里,同时碳水化合物和脂肪含量极低。其目的是通过迫使身体消耗肝脏中储存的碳水化合物来减小肝脏的大小。这可以确保最大的手术操作空间,使肝脏更柔软、更易于移动,被认为可以提高患者的安全性。通常,患者会在术前极低能量饮食两周,但一些中心建议对于体重指数非常高的患者可以延长至四周。除了可能降低胰岛素抵抗和改善血糖控制外,这种饮食本身也会导致一定程度的酮症,因此,对于患有糖尿病的患者,继续使用SGLT2抑制剂可能会导致严重的酮症酸中毒,这一类患者需要特别考虑。
疾病日规则(也称为疾病日用药指导)是针对药物使用进行的调整,以降低急性疾病期间与药物相关的不良事件的风险,涉及药物的暂停使用或剂量调整。接受SGLT2抑制剂治疗糖尿病的患者可能对这些规则比较熟悉,但在围手术期环境中,提供具体的疾病日规则以确保安全康复是非常重要的。这些信息可以包括:关于管理糖尿病的一般建议;降低并发症风险的策略;关于糖尿病酮症酸中毒(DKA)的症状和体征的信息;术后生病时应采取的措施;SGLT2抑制剂剂量管理的具体内容以及寻求帮助的联系方式。
围手术期使用钠-葡萄糖共转运蛋白- 2抑制剂患者的管理建议:

麻海新知·述评
鉴于缺乏高质量的围手术期研究,关于使用肠促胰岛素受体激动剂(GIP/GLP-1 RAs)和钠-葡萄糖共转运蛋白-2抑制剂(SGLT2抑制剂)的患者在围手术期的最佳管理方式仍存在不确定性。本共识声明综合了现有的证据,并提出了实用的建议,以支持临床医生和患者之间的共同决策。对于使用GIP/GLP-1受体激动剂的患者,目前建议继续治疗,但应通过风险评估和分层、共同决策以及使用围手术期技术来降低肺部误吸的风险,若条件允许,可在麻醉诱导前使用床旁胃超声来协助风险分层;使用SGLT2抑制剂的患者应在手术前1d或当天停用,关注发生酮症酸中毒的风险。
尽管我们关注个体药物的围手术期使用,但还有许多因素可能会对肺部误吸、血糖失调、心脏、肾脏和酮症状态的风险产生不利影响;临床医生在提供个体化治疗时应考虑所有这些因素。本共识关注的是择期围手术期管理,但在急诊手术、内镜检查以及其他环境中,这些建议可能并不适用。
所有建议的局限性主要源于有限的证据基础。迄今为止的研究主要是病例报告或存在潜在偏倚的回顾性临床试验。这一领域的证据仍在不断演变,这些建议仅在撰写本文时有效。由于所关注的不良结果发生率相对较低,只有通过大规模的前瞻性观察性研究,才可能得出明确的结论。药物的使用情况也会随着时间而变化,有些人可能在没有医生处方的情况下获得GIP/GLP-1受体激动剂,临床医生在未来可能会更频繁地遇到使用这些药物的人。此外,某些具体的管理要素很难基于没有证据的情况下提出明确建议,同时还需要考虑机构的能力和容量,例如,无法推荐对使用SGLT2抑制剂的人进行酮体监测的频率。
未来的研究需要探索肺部误吸的风险,并指导GIP/GLP-1受体激动剂的开始使用和停用时间、术前禁食时间以及风险缓解策略。还需要研究SGLT2抑制剂的最佳停用时间以及在糖尿病患者和非糖尿病患者中发生酮症酸中毒的风险。
原始文献:
El-Boghdadly K, Dhesi J, Fabb P, Levy N, Lobo DN, McKechnie A, Mustafa O, Newland-Jones P, Patel A, Pournaras DJ, Clare K, Dhatariya K. Elective peri-operative management of adults taking glucagon-like peptide-1 receptor agonists, glucose-dependent insulinotropic peptide agonists and sodium-glucose cotransporter-2 inhibitors: a multidisciplinary consensus statement: A consensus statement from the Association of Anaesthetists, Association of British Clinical Diabetologists, British Obesity and Metabolic Surgery Society, Centre for Perioperative Care, Joint British Diabetes Societies for Inpatient Care, Royal College of Anaesthetists, Society for Obesity and Bariatric Anaesthesia and UK Clinical Pharmacy Association. Anaesthesia. 2025 Jan;79(1). Doi: 10.1111/anae.16541.


