Circulation:中国科学技术大学单革团队发现治疗心力衰竭的潜在新策略
时间:2025-02-25 12:08:12 热度:37.1℃ 作者:网络
在动物细胞中鉴定了来源于核基因组和线粒体基因组的环状RNA。线粒体编码的环状RNA(mecciRNAs)正引起越来越多的关注,并且已经认识到mecciRNAs的几个成员在调节线粒体功能中的作用。众所周知,线粒体功能障碍与心力衰竭(HF)有关。
2025年2月20日,中国科学技术大学单革团队在Circulation在线发表题为“Fast Degradation of MecciRNAs by SUPV3L1/ELAC2 Provides a Novel Opportunity to Tackle Heart Failure With Exogenous MecciRNA”的研究论文,该研究发现SUPV3L1/ ELAC2对MecciRNA的快速降解为外源性MecciRNA治疗心力衰竭提供了新的机会。
研究发现mecciRNAs被解旋酶SUPV3L1 (var1,3-like protein1的抑制因子)和内切核糖核酸酶ELAC2 (elaC核糖核酸酶Z 2)的动物保守复合物迅速降解。MecciRNA降解复合物和mecciRNAs与线粒体通透性转换孔及其调节剂相互作用,包括TRAP1 (TNF受体相关蛋白1)和CypD(亲环素D)。MecciRNAs调节线粒体TRAP1和CypD的水平,以调节线粒体通透性转换孔的开放和线粒体活性氧的释放。外源性应用的mecciRNAs与胞质TRAP1相互作用,增加TRAP1的线粒体水平,并导致线粒体通透性转换孔更封闭的状态,以抑制有害的活性氧物质释放。心力衰竭条件导致mecciRNA降解,体外合成的mecciRNA对阿霉素和压力超负荷诱导的心力衰竭小鼠模型均有显著的保护作用。该研究证明了mecciRNAs的快速降解以及mecciRNAs对线粒体通透性转换孔的线粒体活性氧释放的相关调节。心力衰竭条件导致代谢酶降解失调,外源性代谢酶在心力衰竭小鼠模型中显示出治疗潜力。

心力衰竭(HF)是一种复杂的临床综合征,由遗传因素和非遗传因素引起,如心脏病发作、高血压和心肌功能障碍。扩张型心肌病是最常见的心肌病类型,超过50%的扩张型心肌病患者出现心力衰竭症状。一些药物(如蒽环类药物多柔比星[DOX])也可能导致或加重心力衰竭。尽管了解其发病机制,但目前针对心力衰竭的药物治疗主要旨在控制症状,并且仍然需要恢复心脏功能的治疗。
线粒体是细胞内活性氧(ROS)的主要来源,线粒体通透性转换孔(mPTP)负责线粒体ROS (mtROS)的释放。mPTP是一种非特异性孔隙,在线粒体功能障碍时,它会对ROS或钙水平的增加做出反应。在心力衰竭中,心脏的机械能量耦合异常,线粒体生物能功能障碍导致ROS的过度产生,从而导致心脏缺陷的进展。
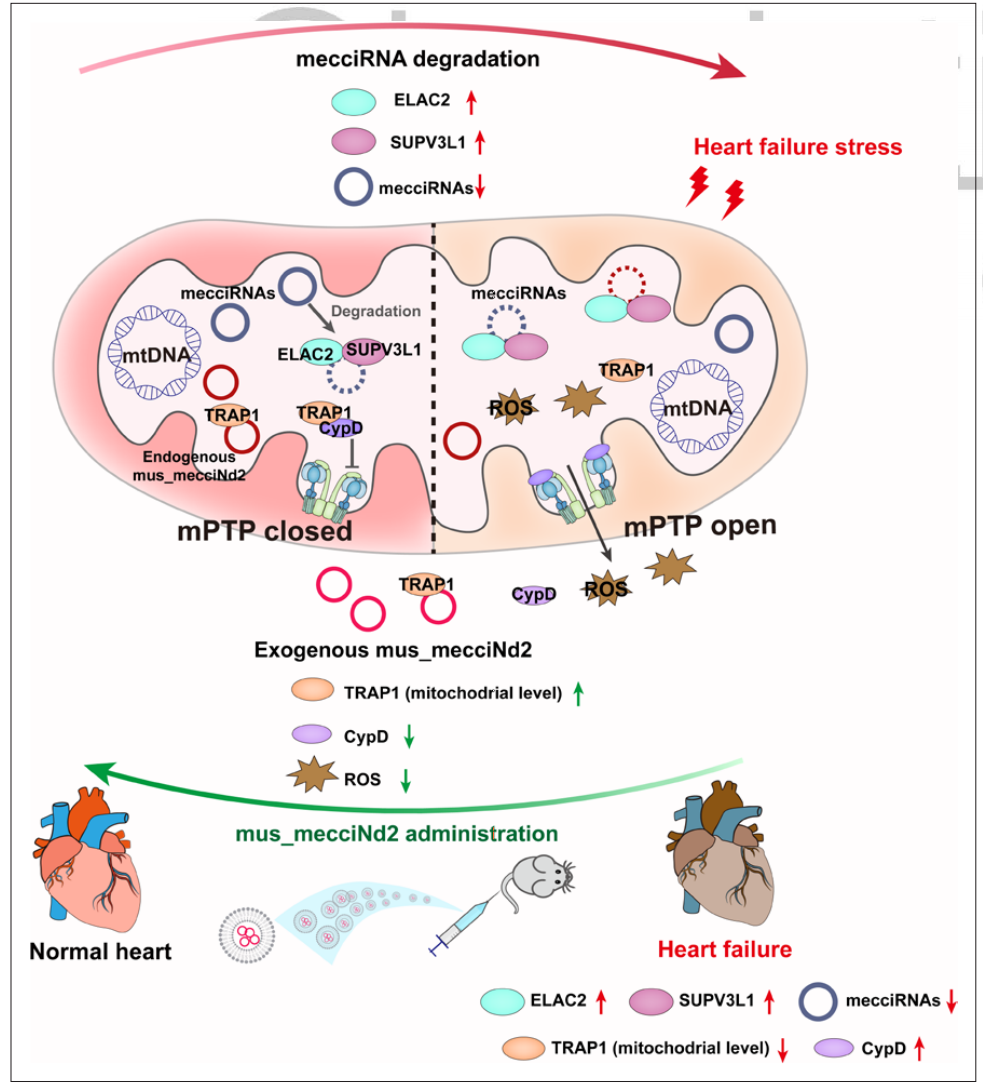
mecciRNA降解的工作模式及外源mecciND2在治疗心力衰竭中的应用(图源自Circulation)
在哺乳动物细胞中,一般认为线粒体基因组产生多顺反子转录物,这些转录物被tRNA基因的短片段分开,充当标点符号。RNase P复合物和ELAC2 ,具有RNase Z活性,切割这些tRNA的5 '和3 '末端,释放成熟的mRNAs。ELAC2的突变被报道为婴儿肥厚型心肌病患者的病因缺陷。酵母ATP-依赖性解旋酶SUV3的人类直系同源物, SUPV3L1,是RNA代谢的另一个保守的关键因子,已知调节成熟线粒体mRNA的稳定性和线性中间体的加工。
在这项研究中,作者研究了mecciRNA降解的机制,它在心力衰竭中的功能作用,以及mecciRNA的潜在治疗价值。从发现保守的SUPV3L1/ELAC2复合物对mecciRNAs的快速降解以及mecciRNAs对mPTP的相关调节开始, 该研究提供了一系列证据,支持利用mecciRNA降解机制和外源性mecciND2(与TRAP1相互作用)的潜力,通过维持mPTP的关闭状态来治疗心力衰竭,从而有效减少mtROS的有害释放。
参考消息:
https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.124.070840


