“百年神药”再立功!多项研究:长期低剂量服用阿司匹林不仅预防癌症,还能降低癌症转移风险!关键靠这一信号通路
时间:2025-03-24 12:09:16 热度:37.1℃ 作者:网络
如果要评选药物界的“长青树”,阿司匹林绝对榜上有名——这位“药坛顶流”已经陪伴人类走过百余年,横跨解热、镇痛、抗炎等多个领域。
学界对阿司匹林的研究热情也从未冷却。尤其近年来,阿司匹林的新临床用途层出不穷,不仅能缓解痛风、代谢性肥胖,还在糖尿病、癌症等领域展现出潜力。而其中最让人瞩目的,莫过于阿司匹林在癌症治疗中的惊人发现。
哈佛医学院等研究团队对超过10万人的数据进行深入分析,发表于JAMA Oncology的一项研究[1]表明,阿司匹林对结直肠癌(CRC)有显著的预防作用,而且竟在那些生活方式糟糕透顶的人群中表现得尤为明显。
简单来说,这意味着阿司匹林能预防CRC的发生,但问题是——它对所有人都有效吗?答案是:越不健康,受益越大!随着生活方式评分的升高,与定期服用阿司匹林相关的绝对风险降低率(ARR)逐渐降低。
那么,到底是什么影响了阿司匹林的防癌“威力”?在这五个生活方式因素中,最能决定阿司匹林“好不好使”的是BMI和抽烟。换言之,如果一个人体重超标(BMI≥25)、抽烟成瘾,那么阿司匹林的防癌潜力就能得到最大化的发挥。
并且,这个趋势在20年的累积数据里仍然成立:无论生活方式如何,定期服用阿司匹林的20年CRC累积发病率为4.05%,依然低于非定期服用者。随着生活方式评分的增加,服用阿司匹林相关的ARR会逐渐降低,从评分0-1的1.39%下降到评分4-5的0.04%。
不久前,来自剑桥大学的研究团队发表于Nature的一项研究[2]又给阿司匹林的“履历”添上浓墨重彩的一笔:这位百年“老将”还能抑制癌症转移!研究表明,阿司匹林能够释放受血栓素A2(TXA2)抑制的T细胞,激活人体免疫系统,狙击癌细胞的“迁徙计划”。
其实,癌症之所以可怕,90%的死亡源于“转移”。就像蒲公英种子随风飘散,癌细胞会悄悄潜入血液,扎根在肺、肝、脑等重要器官。按理说,这些刚刚落脚的“微小转移灶”本应是最脆弱的——它们还没有构建起保护自己的“免疫屏障”,很快被免疫细胞“剿灭”。然而现实中,免疫细胞却频频“失手”。这让研究团队开始怀疑,是不是有什么“内鬼”在暗中瓦解了免疫细胞的“战斗力”。
而早在此前的一项大规模体内基因筛选中,研究者就识别了一批与癌症转移密切相关的宿主调控基因,其中编码ARHGEF1的基因显得尤为可疑。这一发现点燃了团队的好奇心,ARHGEF1 是否就是那个在暗中“通风报信”的“内鬼”呢?为了弄清真相,研究者们开始了一系列实验。
这个结果让人眼前一亮:ARHGEF1主要通过血液系统中的细胞介导来“捣乱”,而非其他组织的细胞。
那么,问题来了:在这些细胞中,到底是谁在和癌细胞“勾结”呢?
为了查清ARHGEF1究竟在哪类血液系统细胞中发挥免疫抑制作用,研究团队瞄准了三类“免疫战士”——NK细胞、巨噬细胞和T细胞,逐一展开“精准打击”实验。
这一发现无疑是发现了T细胞中隐藏的“叛徒”,是 ARHGEF1的存在抑制了T细胞的“战斗力”,让癌细胞“有机可乘”。
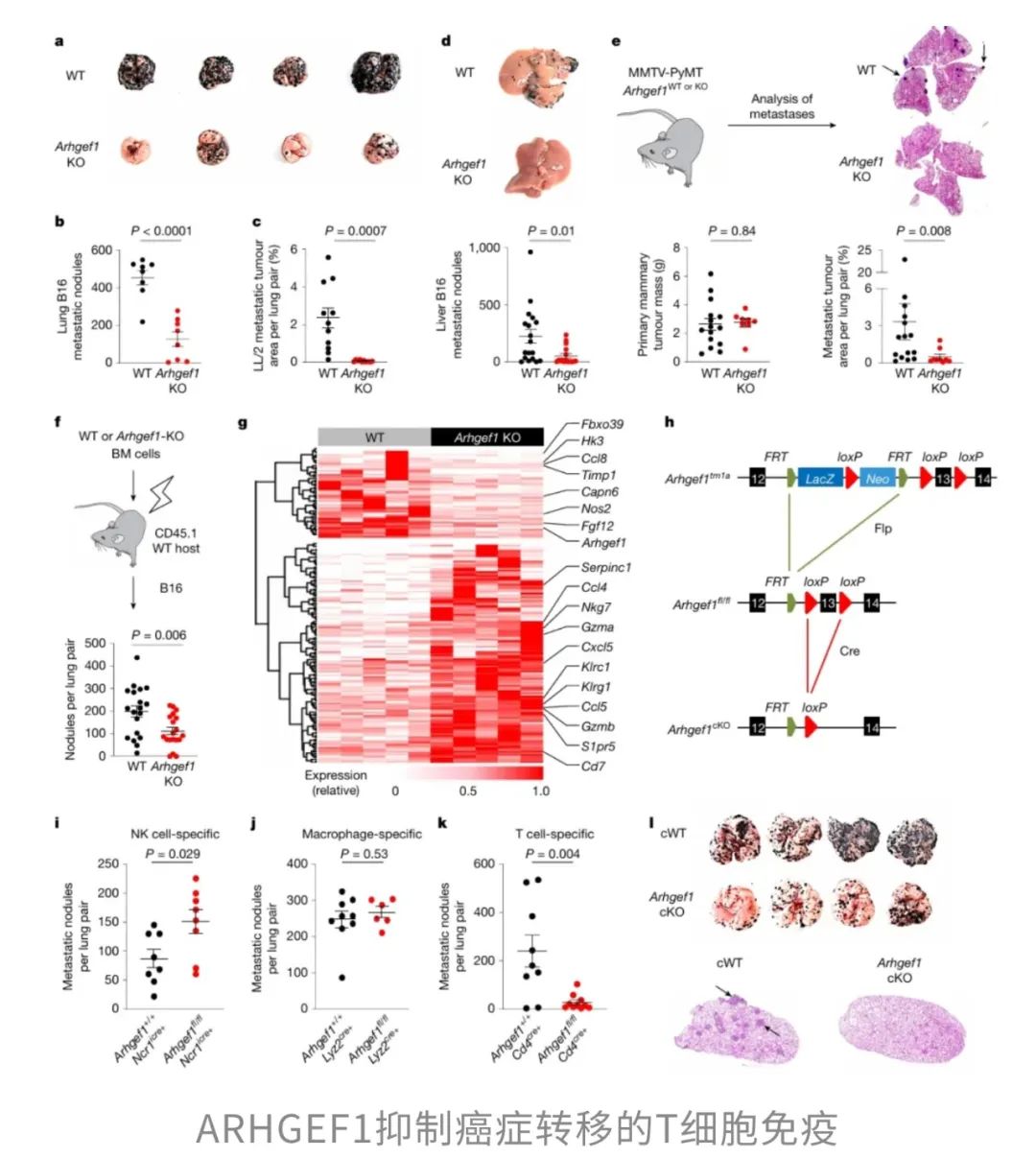
更为形象地来说,ARHGEF1好比免疫系统里的“刹车片”,关键时刻它会限制T细胞的多功能性和抗肿瘤效应,导致细胞更容易陷入耗竭状态,减弱其免疫杀伤力,这才让癌细胞有了“喘息”和转移的机会。而一旦“摘掉”这块刹车片,T 细胞的多功能性和抗肿瘤效应显著增强。
ARHGEF1遏制T细胞“战斗力”的“幕后操控者”
所以,到底是谁在背后悄悄操控ARHGEF1,遏制了T细胞的“战斗欲望”。
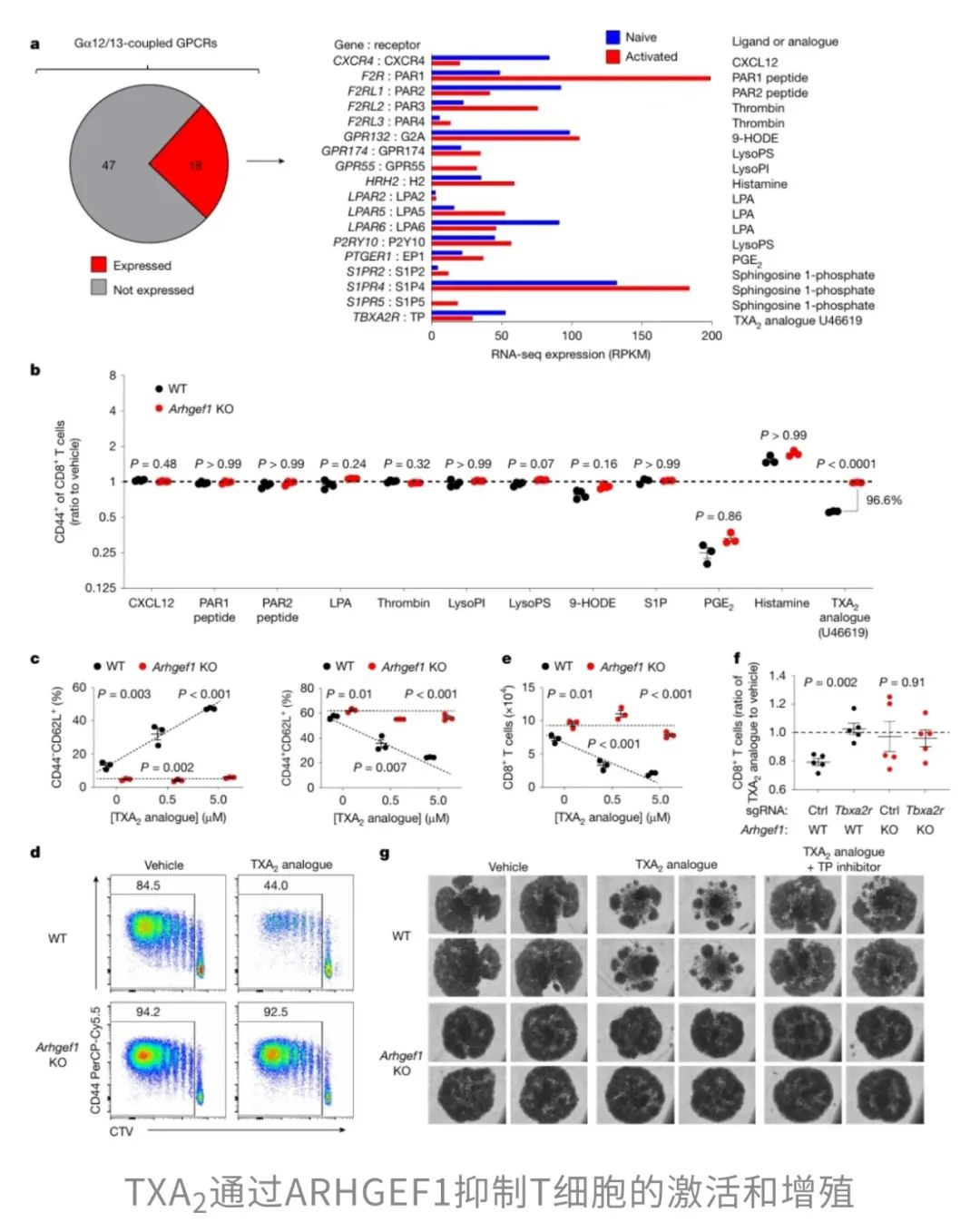
于是,研究者分析了T细胞中ARHGEF1上下游的受体和配体,首先锁定了那些能激活ARHGEF1的G蛋白偶联受体(GPCR)。GPCR受体就像T细胞表面的“信号天线”,接收外界的信号指令,而部分GPCR能够与Gα12/13这类特殊的信号分子合作,共同激活ARHGEF1。
为了进一步确认哪位GPCR是ARHGEF1真正的“幕后操控者”,研究人员还追踪了这些受体的“密友”——已知的配体,看看谁能有效遏制T细胞的“战斗力”。结果显示,大部分配体都只是“路人甲”,而TXA2的稳定类似物U46619却成了那个“例外”!它不仅显著抑制了T细胞的活化和增殖,而且这种抑制效果几乎完全依赖于ARHGEF1的存在——一旦ARHGEF1被敲除,U46619的指令就无法传达。看来,TXA2就是这个关键的“反派”。
正所谓无巧不成书,这个“反派”的出现,让人联想到阿司匹林的作用机制。为什么这么说呢?
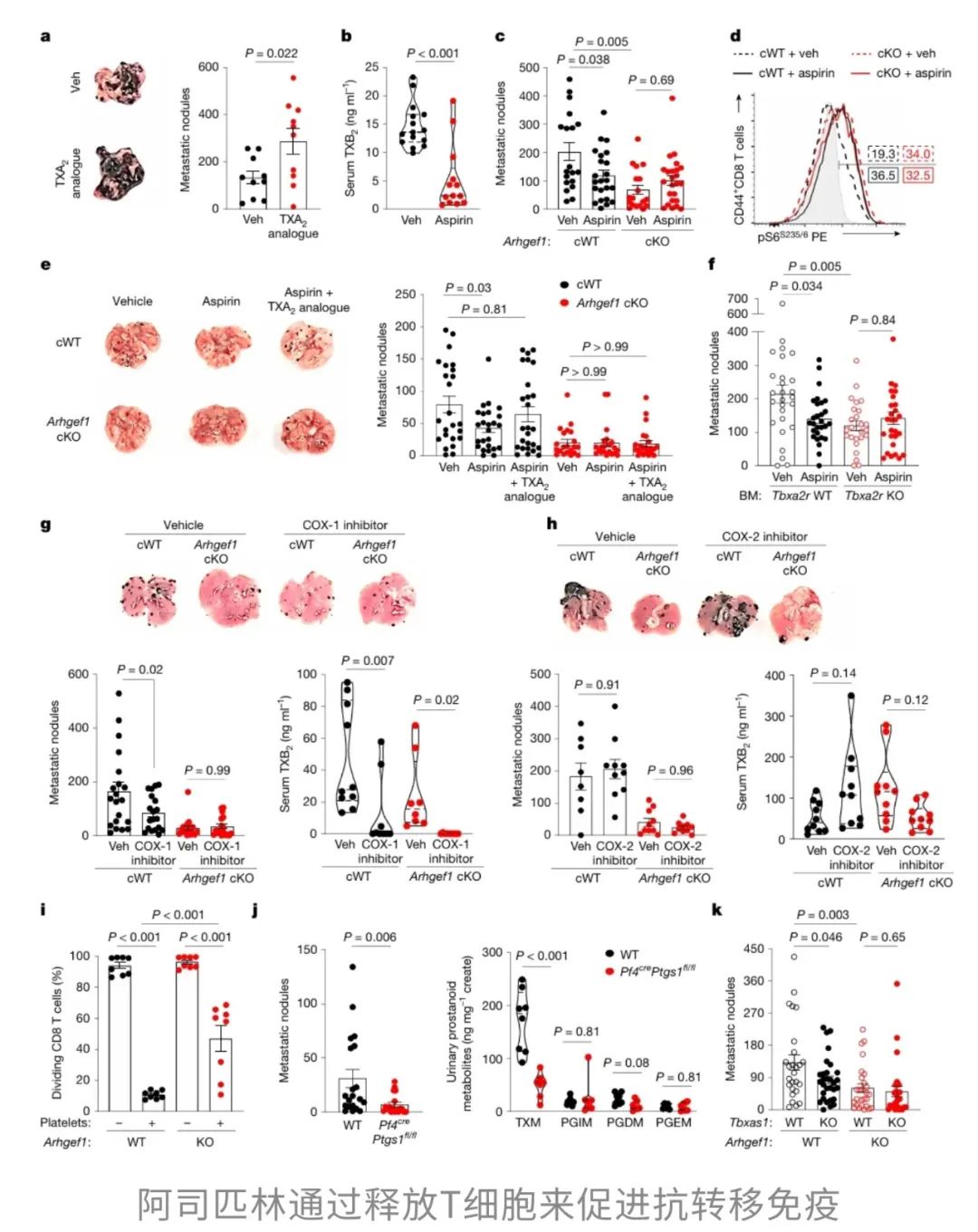
事情得从阿司匹林抑制环氧合酶(COX),减少TXA2的生成开始讲起。TXA2是种与血小板聚集、血管收缩有关的分子,但研究人员却注意到,它还会限制T细胞的活化,进而削弱免疫系统的抗肿瘤能力。既往的大规模临床试验和荟萃分析也表明,阿司匹林的使用与多种肿瘤转移风险降低有关。这让研究者产生了一个大胆的假设:阿司匹林会不会是通过抑制TXA2的产生,释放T细胞,让它们重燃“战斗力”,从而阻止癌细胞的转移?
这似乎说明,阿司匹林的“抗癌魔法”离不开ARHGEF1的参与。
这也再次佐证了,阿司匹林是通过降低TXA2水平,解除其对T细胞的抑制,实现了抗肿瘤转移效果。
进一步机制分析揭示,COX抑制剂可以有效降低小鼠血清中TXA2代谢产物的含量,而COX正是血小板生产TXA2的关键。血小板不仅是血液凝集的重要参与者,还能通过分泌TXA2“远程遥控”T细胞的活性,压制其抗肿瘤的“战斗力”。而当研究人员用抗体耗竭法去除小鼠体内的血小板时,即便这些小鼠具备ARHGEF1的表达,也无法发生肿瘤转移。由此可以确定,血小板通过释放TXA2抑制T细胞,这正是阿司匹林抗肿瘤转移的关键所在。
总的来说,这项研究揭示了与健康生活的人群相比,服用阿司匹林更能“拯救”生活方式不健康的参与者,使其绝对获益最大。5种健康生活方式里,与阿司匹林使用相关的ARR差异最大的是BMI和吸烟。并且其能够通过抑制TXA2-ARHGEF1信号通路,增强T细胞的抗肿瘤免疫反应,从而有效抑制肿瘤的转移。
看来,阿司匹林这种看似普通的白色药片,承载着人类对医学奥秘的探索和对生命健康的追求。它不仅是工业时代科技和医疗进步的象征,更是人类与疾病顽强抗争的见证者。在抗癌的战场中,阿司匹林无疑成为了我们手中的一把利剑,帮助我们抵御肿瘤和其他疾病的侵袭。
仍需指出的是,研究[2]主要基于小鼠模型,尽管这些模型在癌症研究中具有重要价值,但与人类癌症仍存在生物学差异,限制了直接外推至人类的适用性。
[1]Sikavi DR, Wang K, Ma W, Drew DA, Ogino S, Giovannucci EL, Cao Y, Song M, Nguyen LH, Chan AT. Aspirin Use and Incidence of Colorectal Cancer According to Lifestyle Risk. JAMA Oncol. 2024 Oct 1;10(10):1354-1361. doi: 10.1001/jamaoncol.2024.2503. PMID: 39088221; PMCID: PMC11295063.
[2]Yang, J., Yamashita-Kanemaru, Y., Morris, B.I.et al. Aspirin prevents metastasis by limiting platelet TXA2 suppression of T cell immunity. Nature (2025). https://doi.org/10.1038/s41586-025-08626-7