徐兵河教授:中国乳腺癌药物临床研究进展与展望
时间:2025-03-22 12:13:36 热度:37.1℃ 作者:网络
编者按:近期,2025年南北汇·第七届乳腺肿瘤论坛在上海隆重召开。会议邀请了乳腺肿瘤领域的资深专家围绕前沿进展和热点话题展开精彩报告和讨论。本次会议上,中国医学科学院肿瘤医院徐兵河院士发表了题为《中国乳腺癌药物临床研究进展与展望》的主题演讲。【医悦汇】特整理演讲内容,以飨读者。
乳腺癌流行现状及中国乳腺癌药物发展
乳腺癌是全球范围内女性发病率最高的肿瘤之一,我国也不例外。据GLOBOCAN 2022 最新数据显示全球每年乳腺癌新发病例数约为230万例,死亡病例约67万例,其中中国每年新发乳腺癌病例数约为35.72万。近年来,中国乳腺癌的发病率呈不断上升趋势,但与发达国家相比,中国国乳腺癌的5年生存率仍存在一定差距,整体相差约10%。

在乳腺癌新药临床研究领域,中国研究从参与走向原创,已取得了显著进展。中国专家学者参与了多项具有国际影响力、能够改变国际乳腺癌诊疗指南的临床研究,例如DESTINY-Breast系列、NATALEE等重要研究。这些研究不仅提升了中国国乳腺癌领域的科研水平,也为全球乳腺癌治疗贡献了中国智慧。

中国参与的原创性研究
DESTINY-Breast 系列研究
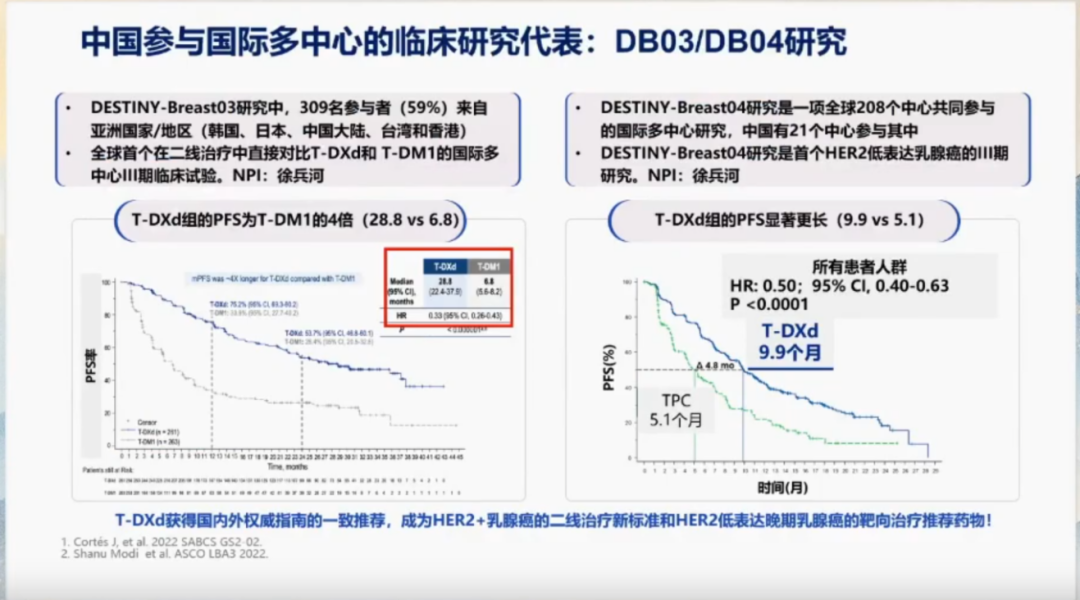
在中国,众多原创性研究也取得了显著成果。例如,DESTINY-Breast03和DESTINY-Breast04研究备受关注。其中,DESTINY-Breast03是一项全球多中心的二线治疗研究,共纳入309名患者,旨在对比T-DXd与TDM1的疗效。该研究由我牵头开展,其成果成功改写了HER2阳性晚期乳腺癌二线治疗的临床标准。
DESTINY-Breast04研究则聚焦于HER2低表达患者,研究结果表明,T-DXd相较于医生选择的化疗方案,能够显著延长患者的无进展生存期,延长幅度接近一倍。这一研究是首次将靶向治疗药物应用于HER2低表达患者群体,并正式提出了“HER2低表达”这一重要概念。
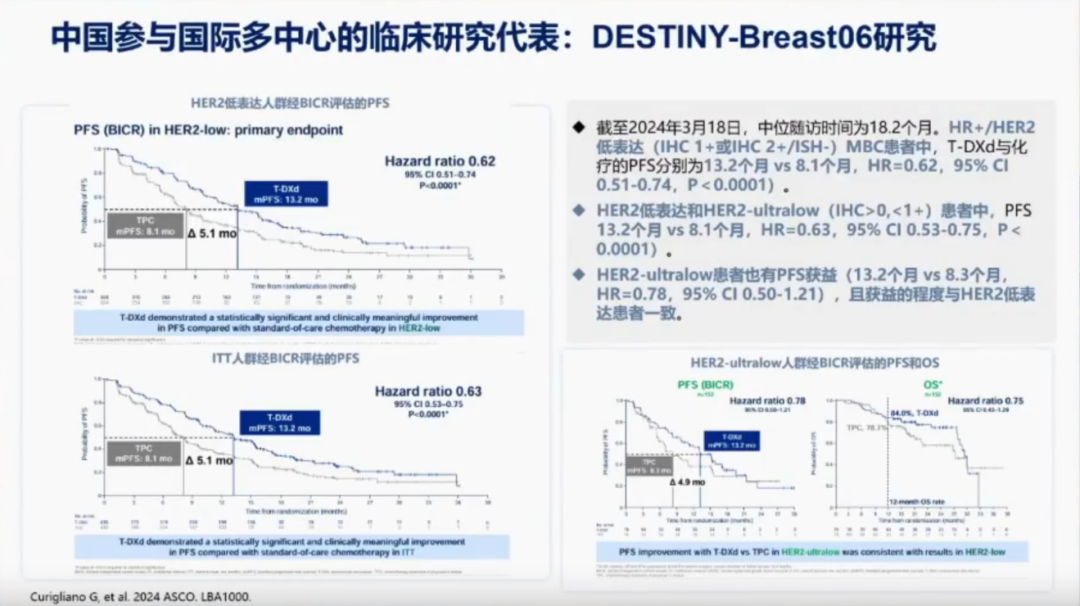
DESTINY-Breast06研究与DESTINY-Breast04研究在设计上有相似之处,但其纳入的患者群体主要是HER2超低表达患者。值得注意的是,参与DESTINY-Breast06研究的患者均未接受过化疗,而DESTINY-Breast04研究的患者则经过了化疗。研究结果再次证实,在未经化疗的HER2低表达或超低表达患者中,T-DXd的疗效优于医生选择的化疗方案。该研究结果已于去年发表在新西兰医学杂志上,胡夕春教授作为主要研究者之一,为这一成果做出了重要贡献。
NATALEE研究
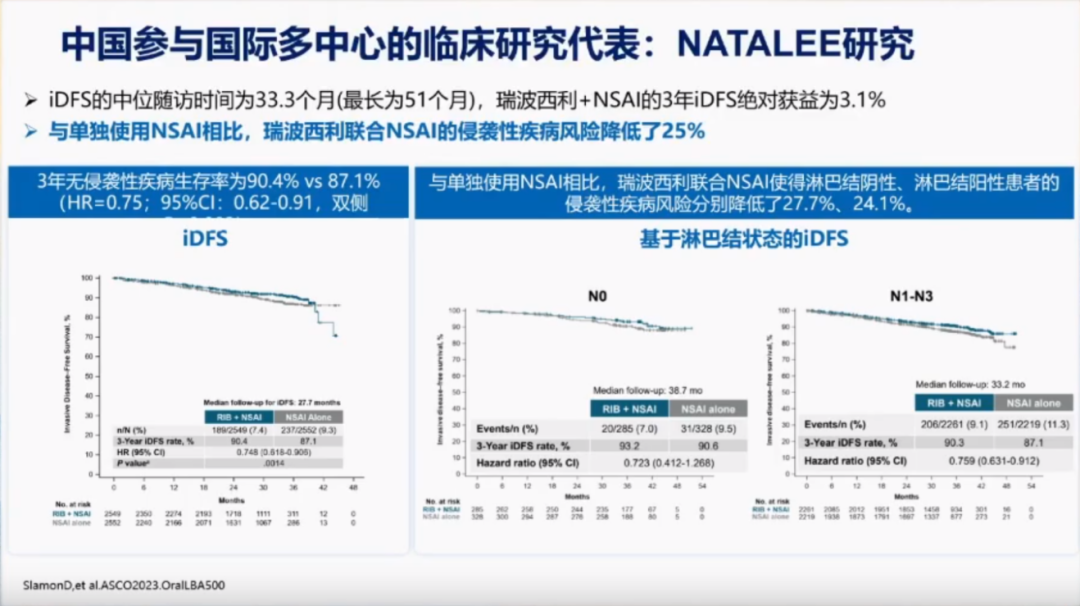
NATALEE研究也是一项国际多中心的研究,研究结果显示CDK4/6、瑞博西利联合非载体类化疗药物与单用非载体的化疗药相比,能够降低疾病的复发风险25%,能够使淋巴结阳性和淋巴结阴性的这种术后患者能够获得一个生存的获益,IDFS的中位随访时间为33.3个月,瑞博西利联合非载体类化疗药物3年IDFS绝对获益是3.1%。
中国原创研究
HR + 乳腺癌
DAWNA-1研究
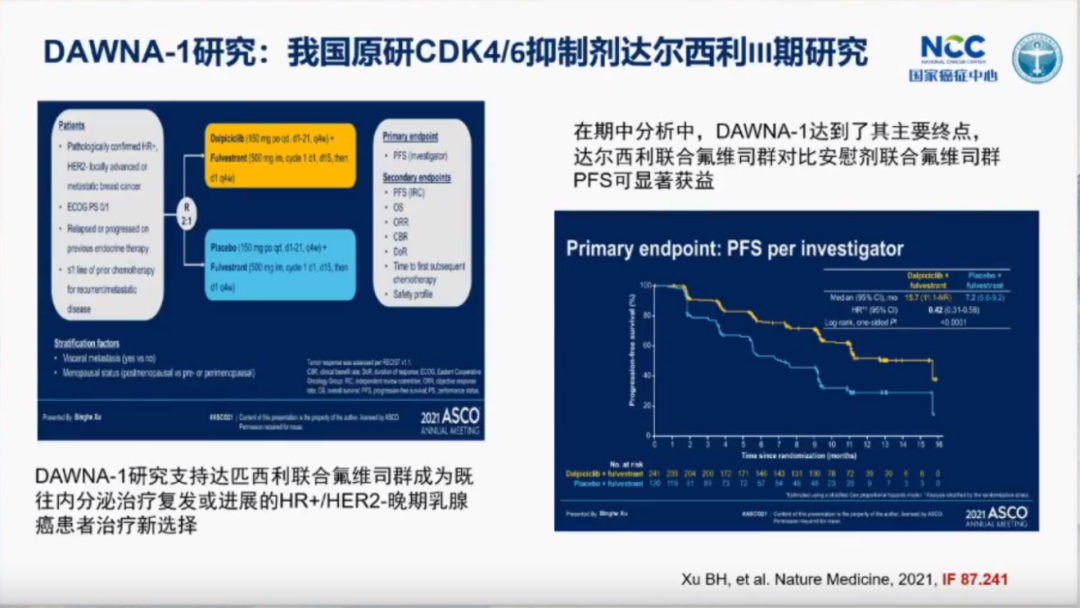
DAWNA-1研究是中国自主研发的CDK4/6抑制剂达尔西利的III期临床研究,由徐兵河院士牵头开展。该研究通过达尔西利联合氟维司群与安慰剂联合氟维司群进行对比。在期中分析中,DAWNA-1研究达到了其主要终点,结果显示达尔西利联合氟维司群相较于安慰剂联合氟维司群可显著延长患者的无进展生存期(PFS),两组的中位PFS分别为15.7个月和7.2个月(HR=0.42,95%CI:0.31-0.58,P<0.0001)。这一成果在2021年美国临床肿瘤学会(ASCO)年会上以口头报告的形式亮相,并于2021年11月4日在国际顶级期刊《Nature Medicine》上发表。
DAWNA-2研究
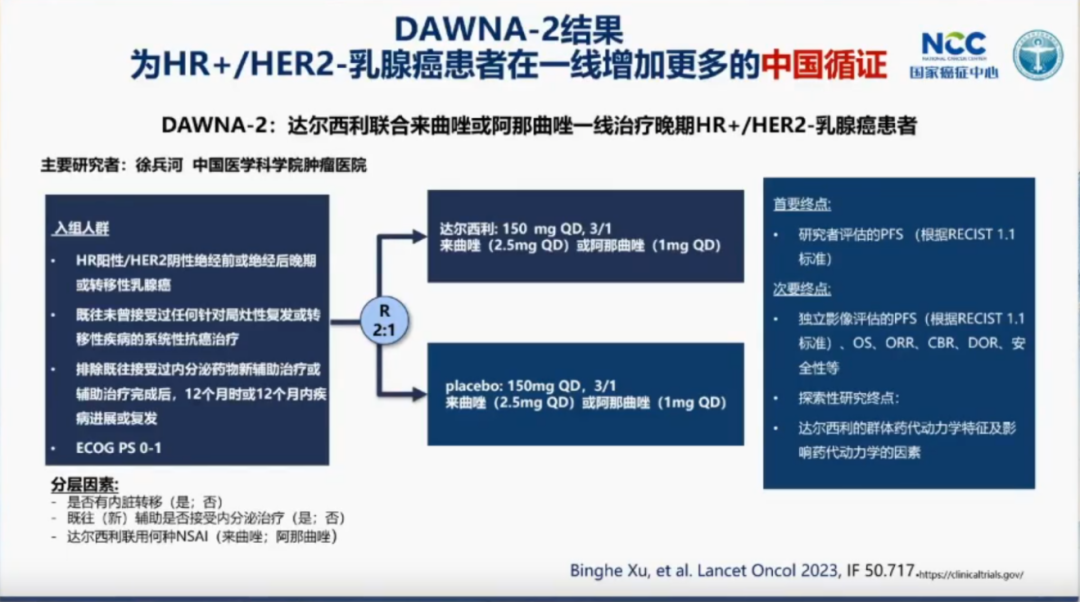
在DAWNA-1研究的基础上,DAWNA-2研究进一步为HR+/HER2-乳腺癌患者的一线治疗提供了更多中国循证医学证据。DAWNA-2是一项多中心、随机对照、双盲的Ⅲ期临床试验,旨在评估达尔西利联合来曲唑或阿那曲唑作为HR+/HER2-晚期乳腺癌患者一线治疗的疗效。研究结果显示,达尔西利联合来曲唑/阿那曲唑显著改善了患者的无进展生存期(PFS),研究者评估的中位PFS分别为30.6个月和18.2个月(HR=0.51,95%CI:0.38-0.69,P<0.0001)。这一结果表明,达尔西利联合芳香化酶抑制剂在一线治疗中优于单药芳香化酶抑制剂。该研究结果已发表在国际肿瘤学领域顶级期刊《The Lancet Oncology》上。
MIRACLE 研究
与西方国家不同的是,在包括中国在内的亚洲乳腺癌患者大部分(55%~60%)为绝经前女性,而依维莫司联合内分泌治疗对绝经前妇女的益处尚未得到很好的描述。在依维莫司联合来曲唑的II期MIRACLE研究中,依维莫司组和对照组的中位PFS分别为19.2个月和11.0个月,且在一线来曲唑单药治疗进展的患者接受依维莫司联合来曲唑治疗仍可获得额外5.5个月的PFS。

ACE研究
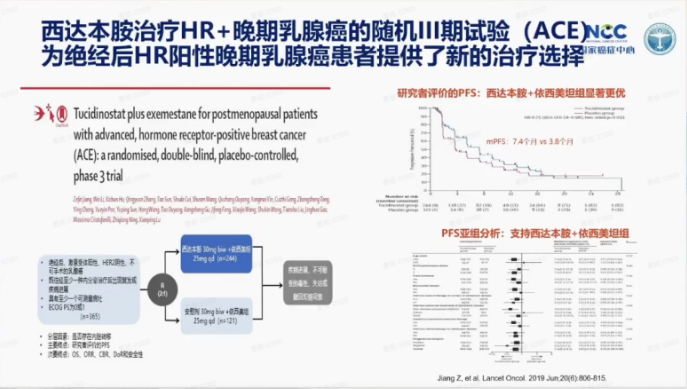
西大本胺是中国自主研发的创新药物,其相关研究由江泽飞教授教授牵头,名为ACE研究。该研究聚焦于HR+晚期乳腺癌的二线治疗,旨在评估依西美坦联合西大本胺对比安慰剂联合依西美坦的疗效。研究结果显示,联合治疗组的中位无进展生存期(PFS)为7.4个月,显著高于对照组的3.8个月(HR=0.75,95%CI:0.58-0.98,P=0.033),联合组相比对照组延长了近3个月的PFS。这一成果为HR+晚期乳腺癌的二线治疗提供了重要循证医学证据,并于发表在国际肿瘤学顶级期刊《The Lancet Oncology》上。
恩替诺特联合依西美坦治疗HR+ABC的随机对照III期试验
表观遗传学药物HDACi恩替诺特在治疗激素受体阳性乳腺癌患者中的研究。研究显示,恩替诺特联合依西美坦治疗内分泌耐药的HR阳性乳腺癌患者,能够显著延长中位无进展生存期(PFS),从3.72个月提升至6.32个月,风险比(HR)为0.74,统计学意义显著(p=0.021)。此外,该药物显示出可耐受的安全性和疗效,客观缓解率(ORR)为9.52%,临床获益率(CBR)为42.86%,中位PFS为9.41个月。这些结果在SABCS大会上得到了报告,进一步确认了HDAC抑制剂的安全性和疗效,为晚期乳腺癌患者提供了更多的治疗选择。

BG01-1323L研究
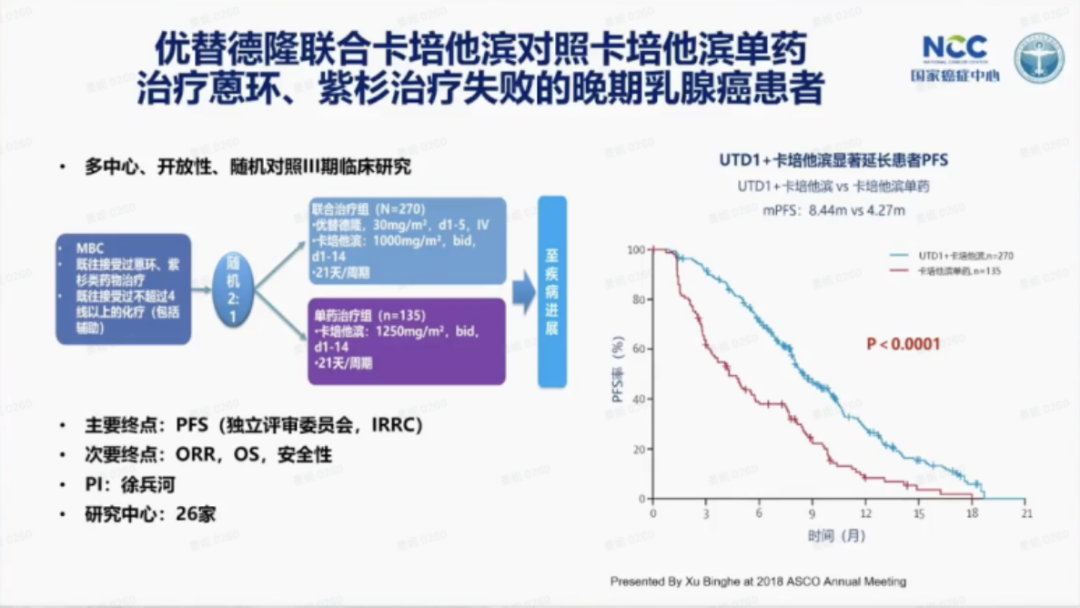
BG01-1323L研究是一项在中国26家医院开展的多中心、开放标签、前瞻性随机对照试验,纳入405例蒽环类和紫杉类化疗方案耐药的转移性乳腺癌患者。结果显示,与卡培他滨单药治疗相比,优替德隆联合卡培他滨显著提高客观缓解率(ORR:49.8% vs 26.7%,P<0.0001)和临床获益率(CBR:60% vs 33.3%,P<0.001),并延长无进展生存期(PFS:8.57个月 vs 4.11个月,P<0.0001;HR=0.46)和总生存期(OS:20.9个月 vs 15.7个月,P<0.0032;HR=0.69),降低晚期患者死亡风险31%。该研究结果于2016年和2018年两次入选ASCO年会口头报告,全文分别于2017年发表于《Lancet Oncology》和2021年发表于《Annals of Oncology》。作为20年来中国唯一一项创新化疗药研究,其受到业内高度评价,如《Nature Reviews Clinical Oncology》发表特评,认为该方案为难治性晚期乳腺癌患者提供了有效的治疗选择。
三阴性乳腺癌
三阴性乳腺癌(TNBC)预后较差,但近年来国内在TNBC分型方面取得了显著进展,受到国际关注。2011年Lehmann将TNBC分为6个分子亚型,2015年Burstein提出TNBC四分型,2016年邵志敏教授团队创新性地提出TNBC“复旦四分型”。因此,当前TNBC相关研究多基于分子分型展开。
铂类药物一线治疗晚期TNBC的II期研究
我国开展的一项铂类药物一线治疗晚期TNBC的II期临床研究,入组患者随机分配接受多西他赛 + 顺铂(TP)或多西他赛 + 卡培他滨(TX)治疗,研究结果显示,TP组的中位PFS(10.9 vs 4.8个月)和中位OS(32.8 vs 21.5个月)均优于TX组,研究结果曾发表于Annals of Oncology。

CBCSG 006研究
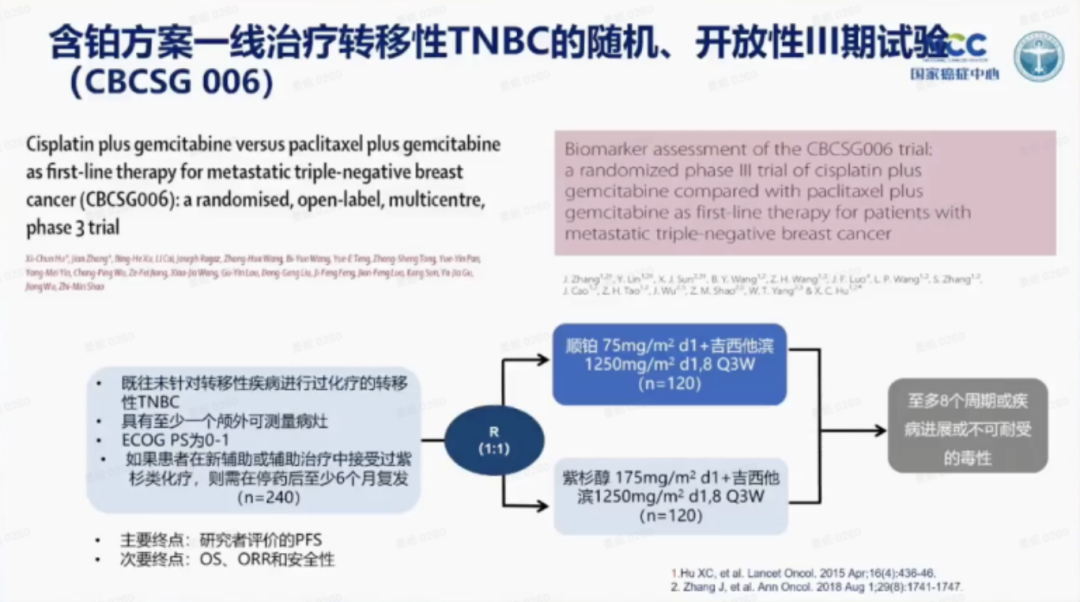
CBCSG 006研究是一项评估了顺铂+吉西他滨和紫杉醇+吉西他滨治疗TNBC的III期随机研究,由胡夕春教授牵头,研究发现顺铂+吉西他滨组的客观缓解率(ORR)显著高于紫杉醇+吉西他滨组(64% vs 49%),中位 PFS 也更优( 7.73 vs. 6.47 个月),同时亚组分析提示携带胚系BRCA1/2突变患者经含铂方案治疗的疗效数值更优。基于中国研究者的研究结果,德国和中国乳腺癌诊疗指南推荐含铂方案作为转移性TNBC标准一线治疗。该研究结果先后发布于 Lancet Oncology 和 Annals of Oncology。
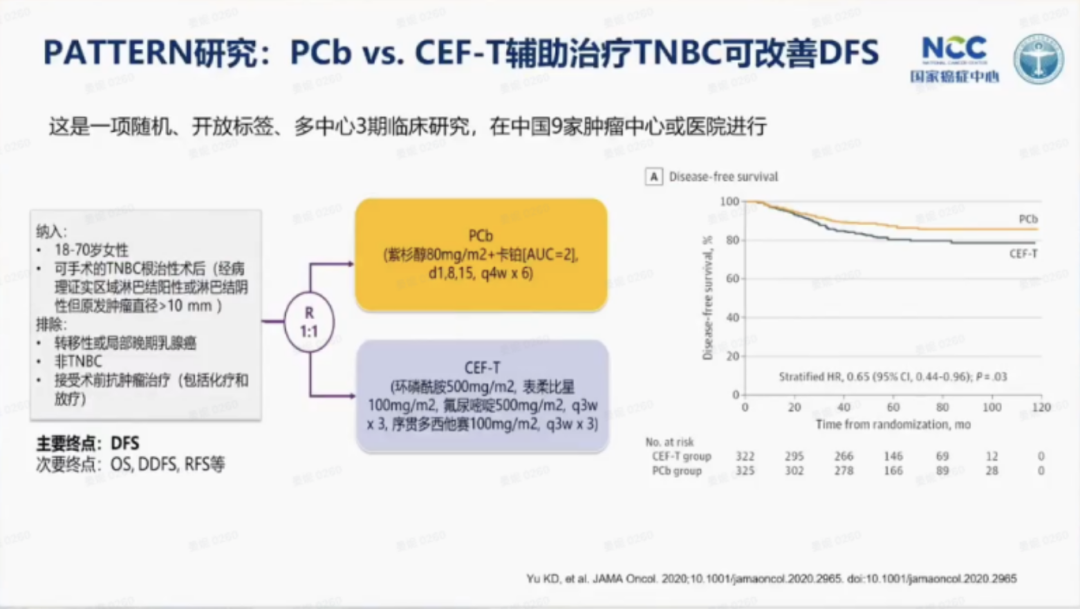
PATTERN研究
PATTERN研究是一项由邵志敏教授牵头的Ⅲ期临床研究,旨在评估卡铂+紫杉醇(PCb)与环磷酰胺+表柔比星+氟尿嘧啶+多西他赛(CEF-T)在早期三阴性乳腺癌(TNBC)术后辅助治疗中的疗效和安全性。结果显示,与CEF-T方案相比,PCb方案将早期可手术TNBC患者的5年无病生存率(DFS)提高6.4%(86.5% vs. 80.3%;HR=0.65,95%CI:0.44-0.96;P=0.03),证实了铂类药物在TNBC辅助治疗中的优效性。该研究结果发表于2020年的《JAMA Oncology》
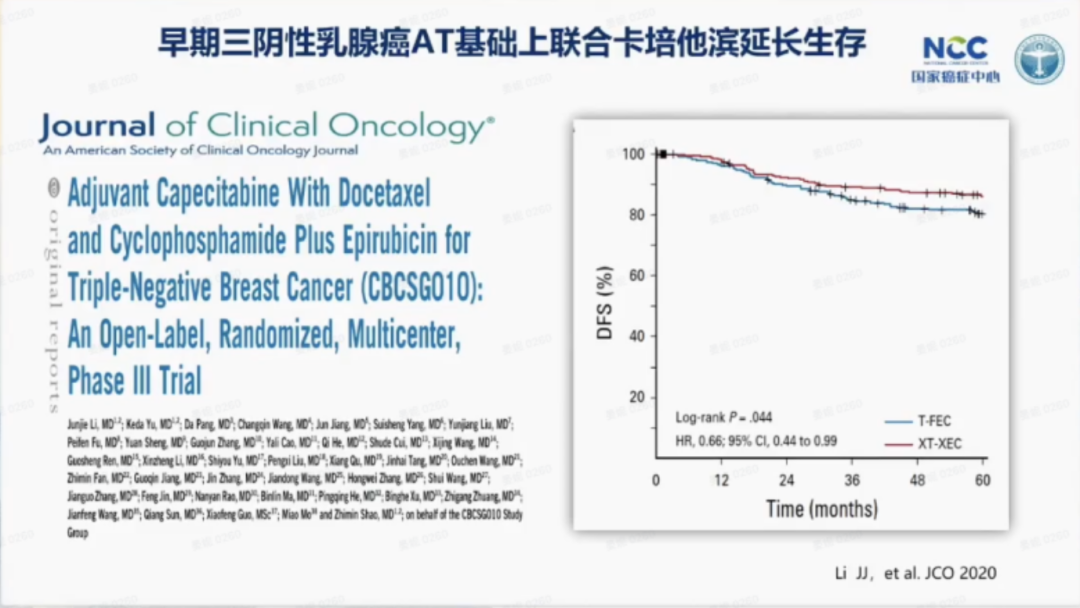
CBCSG010研究
CBCSG010是一项前瞻性、随机、Ⅲ期临床试验,旨在评估在三阴性乳腺癌(TNBC)辅助治疗的现有标准化疗方案(蒽环与紫杉类药物序贯方案)中加入卡培他滨的有效性和安全性。研究纳入符合条件的早期TNBC患者,随机分配至卡培他滨联合方案(3个周期卡培他滨+多西他赛,序贯3个周期卡培他滨+表柔比星+环磷酰胺)或对照方案(3个周期多西他赛,序贯3个周期氟尿嘧啶+表柔比星+环磷酰胺)。结果显示,卡培他滨组的5年无病生存率(DFS)显著高于对照组(86.3% vs. 80.4%;HR=0.66,95%CI:0.44-0.99;P=0.044),表明卡培他滨的加入显著改善了TNBC患者的预后。该研究结果发表于2020年的《Journal of Clinical Oncology》。
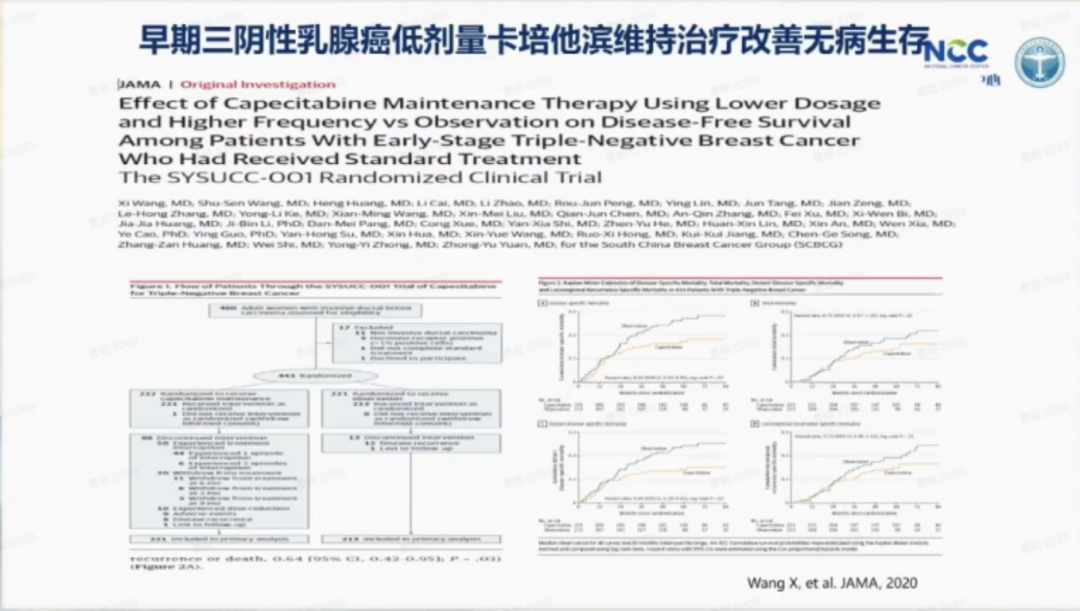
SYSUCC-001 研究
该研究为中山大学肿瘤防治中心袁中玉教授等乳腺癌团队所完成的“可手术三阴性乳腺癌标准治疗后卡培他滨节拍维持的III期临床研究。研究结果显示卡培他滨节拍化疗作为维持治疗,将早期三阴性乳腺癌的复发风险降低了1/3以上,将患者的5年无疾病生存率(DFS)从73.0%提高至82.8%。节拍化疗的安全性良好,83%患者可以顺利完成全程治疗而没有严重毒副反应。该研究是目前国际上首个将节拍化疗用于三阴乳腺癌标准治疗后的维持治疗并取得阳性结果的大型Ⅲ期临床试验。研究结果成功发表于2020年的JAMA主刊。
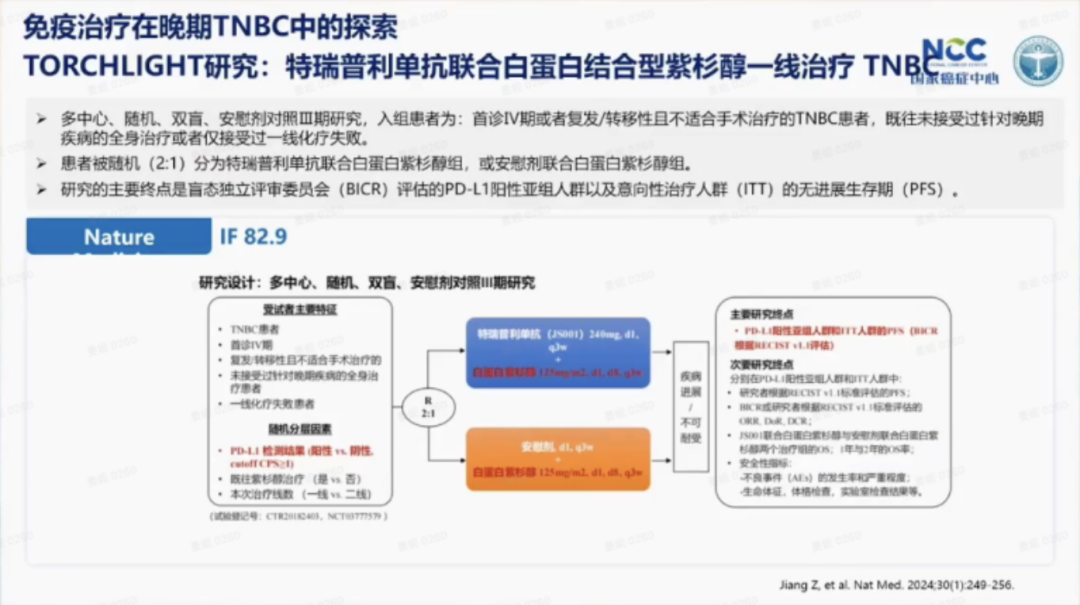
TORCHLIGHT研究
TORCHLIGHT是一项由江泽飞教授牵头的III期研究,旨在比较特瑞普利单抗与安慰剂联合白蛋白结合型紫杉醇(nab-P)治疗不能手术的初治局部晚期和转移性或术后复发的晚期TNBC患者的疗效和安全性。研究结果表明,晚期TNBC患者在接受特瑞普利单抗联合白蛋白结合型紫杉醇一线治疗时取得优异疗效,显著延长了患者的中位PFS(2.8个月)和中位OS(32.8 vs. 19.5 个月),成为国内治疗晚期TNBC的标准一线治疗方案。这项研究的主要结果发表于2024年《Nature Medicine》。
节拍化疗联合免疫治疗用于HER2阴性乳腺癌疗效与安全性的II期临床研究
该研究由徐兵河教授、马飞教授牵头,采用贝叶斯后验概率的随机方式和疗效监测方法,研究共入组了97例患者,并随机将其分为5个队列:(1)长春瑞滨(NVB)单药节拍化疗(n=11),(2)长春瑞滨节拍化疗联合PD-1抑制剂(α-PD1+NVB组,n=7);(3)长春瑞滨节拍化疗联合顺铂常规化疗和PD-1抑制剂(DDP组,n=26);(4)长春瑞滨节拍化疗联合贝伐珠单抗和PD-1抑制剂(BEV组,n=27);(5)长春瑞滨+卡培他滨+环磷酰胺节拍化疗联合PD-1抑制剂(VEX组,n=26)。主要终点为疾病控制率(DCR)。次要目标包括无进展生存期(PFS)和安全性。研究结果显示节拍化疗联合免疫治疗会产生1+1<1;1+1>1或者1+1>2等不同的结果。其中在VEX治疗组,三药化疗+免疫治疗可以显著提升患者的DCR和PFS、OS(DCR为69.7%,PFS为6.6个月,OS为42.6个月)。该研究发表于 2024 年 《Nature Medicine》。

OptiTROP-Breast01研究
SKB264是中国首个原创的TROP2 ADC药物,OptiTROP-Breast01是一项Ⅲ期随机对照、开放标签的中国多中心研究,由徐兵河院士牵头,旨在对比SKB264与化疗在治疗复发或难治性晚期TNBC患者中的疗效和安全性。研究结果显示SKB264组患者的疾病进展风险显著降低69%(HR=0.31,95%CI:0.22-0.45;P<0.00001),死亡风险显著降低47%(HR=0.53,95%CI:0.36-0.78;P=0.0005)。中位无进展生存期(PFS)和总生存期(OS)均优于化疗组。

CamRelief研究
CamRelief研究是由复旦大学附属肿瘤医院邵志敏教授团队牵头的随机双盲、Ⅲ期临床研究,旨在评估卡瑞利珠单抗联合化疗新辅助治疗早期或局部晚期三阴性乳腺癌(TNBC)的疗效和安全性。研究于2020年11月25日至2023年5月12日在中国40家医院开展,纳入441例Ⅱ~Ⅲ期高危TNBC患者,按1:1随机分为卡瑞利珠单抗+化疗组(222例)和安慰剂+化疗组(219例)。治疗方案为前16周每28天的第1、8和15天给予白蛋白紫杉醇+卡铂,随后8周每2周给予表柔比星+环磷酰胺。结果显示,截至2023年9月30日,中位随访14.4个月,卡瑞利珠单抗+化疗组的病理完全缓解率(pCR)为56.8%,显著高于安慰剂+化疗组的44.7%(率差12.2%,单侧P=0.0038)。亚组分析表明,无论患者年龄、淋巴结状态、临床分期或PD-L1表达水平,卡瑞利珠单抗组均显示出更高的治疗有效率。该研究是卡瑞利珠单抗在乳腺癌治疗领域的首个大型随机对照研究,结果表明卡瑞利珠单抗联合化疗可显著提高TNBC患者的pCR率,且安全性可控,有望成为早期或局部晚期TNBC新辅助治疗的新选择。研究结果于2024年发表于《JAMA》。

HER2阳性乳腺癌
吡咯替尼I期-Ⅲ期研究
吡咯替尼是首个国产的泛HER酪氨酸激酶抑制剂(TKI),已成为国内 HER2阳性早期/转移性乳腺癌标准治疗选择。吡咯替尼的Ib期研究曾开创了中国自主研发抗肿瘤药物仅凭借I期研究就登上顶级期刊的先河,而后基于吡咯替尼II期研究的结果与2018年在中国获批上市,III期PHOEBE研究更是多次登上ASCO、SABCS等国际舞台。
PHILA研究
PHILA研究对比了吡咯替尼+曲妥珠单抗+多西他赛(PyHT方案)和曲妥珠单抗+多西他赛一线治疗HER2阳性晚期乳腺癌的疗效与安全性,研究结果显示吡咯替尼的加入使得独立审查委员会评估的PFS延长22.6个月(33.0 个月 vs. 10.4 个月,HR:0.35;P<0.001)。本研究创立的“PyHT方案”成为晚期HER2阳性乳腺癌治疗新标准,研究结果发表于 《British Medical Journal》。

展望
最后,徐兵河教授展望乳腺癌研究的未来,他指出,人工智能辅助靶点发现和药物分子设计将成为重要研究方向。徐兵河教授团队正在与地方政府、大型企业和人工智能公司合作,利用人工智能技术辅助发现肿瘤药物新靶点,快速筛选抗乳腺癌新药。此外,他认为还需探索AI模型与个体化药物治疗的关系,预测新药疗效的分子标志物,以及靶向治疗耐药机制和逆转方法。
在免疫治疗方面,其团队已开展多项研究,包括基因表达谱分析、免疫治疗联合化疗药物的疗效研究等,并发现免疫治疗联合不同化疗药物的疗效存在差异,且不同给药方式联合免疫治疗的效果也不尽相同。目前,免疫治疗仍有许多问题待解决,尤其是新型免疫治疗药物和抗体药物的研究。此外,其团队都也正在开展双抗药物对比标准化方案的研究,初步结果良好。未来,还将探索三抗、四抗乃至五抗药物的研究,但其副作用和研究设计仍需深入探讨。
乳腺癌药物研究的未来涉及众多领域,徐兵河教授期待国内同行加强合作,共同推动中国原创药物的研发与临床研究,将更多创新药物推向国内外市场。


