Blood Cancer J | 来那度胺联合R-CHOP(R2-CHOP)在新诊断的双表达弥漫大B细胞淋巴瘤中的应用
时间:2025-03-09 12:09:08 热度:37.1℃ 作者:网络
弥漫性大B细胞淋巴瘤(Diffuse Large B-cell Lymphoma, DLBCL)是非霍奇金淋巴瘤(Non-Hodgkin's Lymphoma, NHL)中最常见的亚型,占成人病例的30-40%。DLBCL具有显著的异质性,包括细胞起源、形态学、免疫组织化学表型和分子特征等。双表达弥漫大B细胞淋巴瘤(Double Expressor Diffuse Large B-cell Lymphoma, DE-DLBCL)是一种特定的亚型,其特征是MYC和BCL-2的高表达。与非双表达DLBCL相比,DE-DLBCL患者的预后较差,五年总生存率(OS)和无进展生存率(PFS)分别为36%和32%。目前,DE-DLBCL缺乏标准的治疗方案,尽管一些高强度化疗方案显示出一定的疗效,但往往伴随着更严重的副作用。

方法
本研究是一项前瞻性、单臂、II期临床试验,旨在评估来那度胺(Lenalidomide)联合R-CHOP(R2-CHOP)在新诊断的DE-DLBCL患者中的疗效和安全性。研究在复旦大学附属肿瘤医院进行,符合条件患者年龄在18-75岁之间,通过免疫组织化学检测MYC≥40%和BCL-2≥50%。主要排除标准包括原发性纵隔大B细胞淋巴瘤、EBV阳性DLBCL、中枢神经系统淋巴瘤、HIV阳性、活动性乙型或丙型肝炎病毒感染者。患者接受标准的R-CHOP21方案治疗,并在第1-10天每天口服来那度胺 25 mg,每21天为一个周期,共6个周期。主要终点:2年无进展生存期(PFS)。次要终点:总缓解率(ORR)、总生存期(OS)、安全性评估。
研究结果
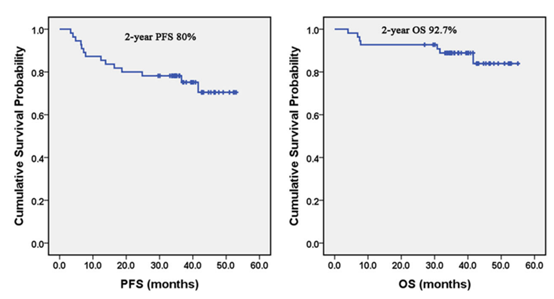
在55例可评估疗效的患者中,总缓解率(ORR)为94.5%,完全缓解率(CR)为83.6%。中位随访时间为38.0个月,7例患者死亡,主要原因是淋巴瘤难治或进展(6例)和继发性肿瘤发展(1例)。2年和3年的无进展生存率(PFS)分别为80.0%(95% CI 70.1%-91.3%)和78.2%(95% CI 68.0%-89.9%),2年和3年的总生存率(OS)分别为92.7%(95% CI 86.1%-99.8%)和88.9%(95% CI 80.8%-97.7%)。未达到中位PFS和OS。
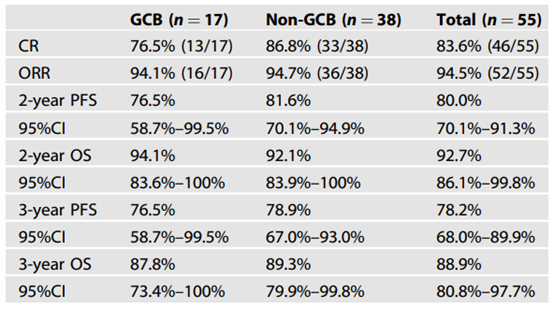
在不同病理特征的患者中,非GCB亚型患者的2年PFS率为81.6%(95% CI 70.1%-94.9%),而GCB亚型为76.5%(95% CI 58.7%-99.5%)。非GCB亚型的CR率为86.8%,而GCB亚型为76.5%。ORR在非GCB亚型为94.7%,在GCB亚型为94.1%。总体来看,R2-CHOP方案在DE-DLBCL患者中表现出较高的缓解率和生存率,尤其是在非GCB亚型患者中。
安全性分析
安全性分析显示,最常见的3或4级血液学毒性包括中性粒细胞减少(67.1%)、血小板减少(19.4%)和贫血(4.5%)。最常见的非血液学不良事件为1至2级,包括疲劳、丙氨酸转氨酶或天冬氨酸转氨酶升高、粘膜炎、恶心和呕吐。3级肺炎发生率为5%,其中两名患者因治疗周期延迟超过21天而退出试验。由于不良事件导致的来那度胺或R-CHOP剂量调整分别占43.6%和20.0%。来那度胺和R-CHOP的相对剂量强度分别为91.5%和98.1%。值得注意的是,在研究期间没有发生治疗相关死亡。
结论
本研究结果表明,来那度胺联合R-CHOP(R2-CHOP)作为新诊断的DE-DLBCL患者的一线治疗方案,显示出较高的疗效和可管理的不良事件。2年PFS率达到80%,符合预定的试验目标。尽管超过60%的患者为晚期疾病(III/IV期),但在六个周期的R2-CHOP治疗后,完全缓解率令人鼓舞,2年和3年的PFS率超过了之前的报告。来那度胺联合R-CHOP在DE-DLBCL患者中的应用显示出良好的前景,尤其是在非GCB亚型患者中。
原始出处
Liu Y, Zhang Q, Lv F, Liu X, Ji D, Xia Z, Jin J, Tao R, Zhang W, Li Q, Zhang S, Wang Z, Wang J, Hong X, Cao J. Lenalidomide combined with R-CHOP (R2-CHOP) in the treatment of newly diagnosed double-expressor diffuse large B-cell lymphoma: a prospective phase II clinical trial. Blood Cancer J. 2025;15:24. https://doi.org/10.1038/s41408-025-01229-5.


