CA“神刊”全球首篇临床试验论著!中山大学肿瘤防治中心马骏院士团队揭示诱导化疗后缩小体积放疗,无复发生存率达 91.5%
时间:2025-03-09 12:09:06 热度:37.1℃ 作者:网络
鼻咽癌是一种具有独特生物学特性和地域分布的恶性肿瘤,尤其在中国南方地区高发。既往针对鼻咽癌的标准治疗模式为诱导化疗(IC)后序贯同期化疗放疗(CCRT)。但因为传统放疗方案基于诱导化疗前的肿瘤体积设计,忽略了随着化疗疗程的进行,肿瘤体积会不断缩小的期刊,导致正常组织也遭受到了辐射,增加了治疗毒性,使得患者预后较差。
而针对这一情况,近日,中山大学肿瘤防治中心马骏院士、孙颖教授、唐玲珑教授团队在被业界称为“神刊”的国际肿瘤学期刊《临床医师癌症杂志》(CA:A Cancer Journal for Clinicians)上发表了一项开放性、非劣效性、多中心、随机III期临床试验研究成果,这是该期刊创刊以来的全球首篇临床试验研究论著。研究结果表明:诱导化疗后缩小体积放疗方案在保证疗效的同时,显著降低了放疗的毒副作用,改善了鼻咽癌患者的生存质量。

研究内容与思路
一、试验设计和参与者
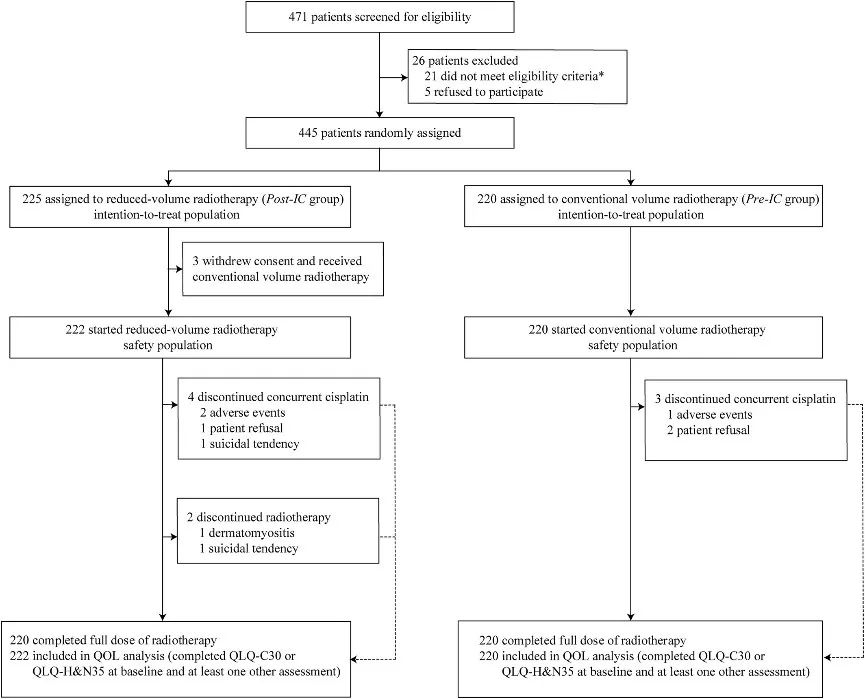
研究纳入了新诊断的、组织学确认的445例非角化性鼻咽癌患者,分期为III-IVA期(AJCC/UICC第8版),年龄18-70岁,Karnofsky表现状态评分≥70分,且已完成3个周期的吉西他滨+顺铂诱导化疗。患者随机划分为缩小体积放疗组(基于诱导化疗后肿瘤体积,Post-IC组,n=225)和传统体积放疗组(基于诱导化疗前肿瘤体积,Pre-IC组,n=220),用以评估缩小体积放疗在肿瘤控制和毒性方面的表现,分层因素包括试验中心和疾病分期。
所有患者均采用强度调控放疗(IMRT)。缩小体积放疗组基于诱导化疗后的MRI影像定义靶区,仅包括残留的软组织肿瘤和骨侵犯区域;传统体积放疗组组则基于诱导化疗前的MRI影像定义靶区,涵盖所有初始肿瘤侵犯区域。剂量分配为原发肿瘤70Gy,颈部淋巴结66-70Gy,高危临床靶区(CTV)60-62Gy,低危CTV 54-56Gy,分30-33次照射。
研究随访时间为每3个月一次,持续3年;之后每6个月一次,直至患者死亡。主要终点为局部区域无复发生存率(LRFS),次要终点包括总生存率(OS)、无远处转移生存率(DMFS)、无失败生存率(FFS)、治疗相关毒性反应和生活质量。毒性评估采用NCI CTCAE v4.0和RTOG/EORTC标准,生活质量评估使用EORTC QLQ-C30和QLQ-H&N35问卷。
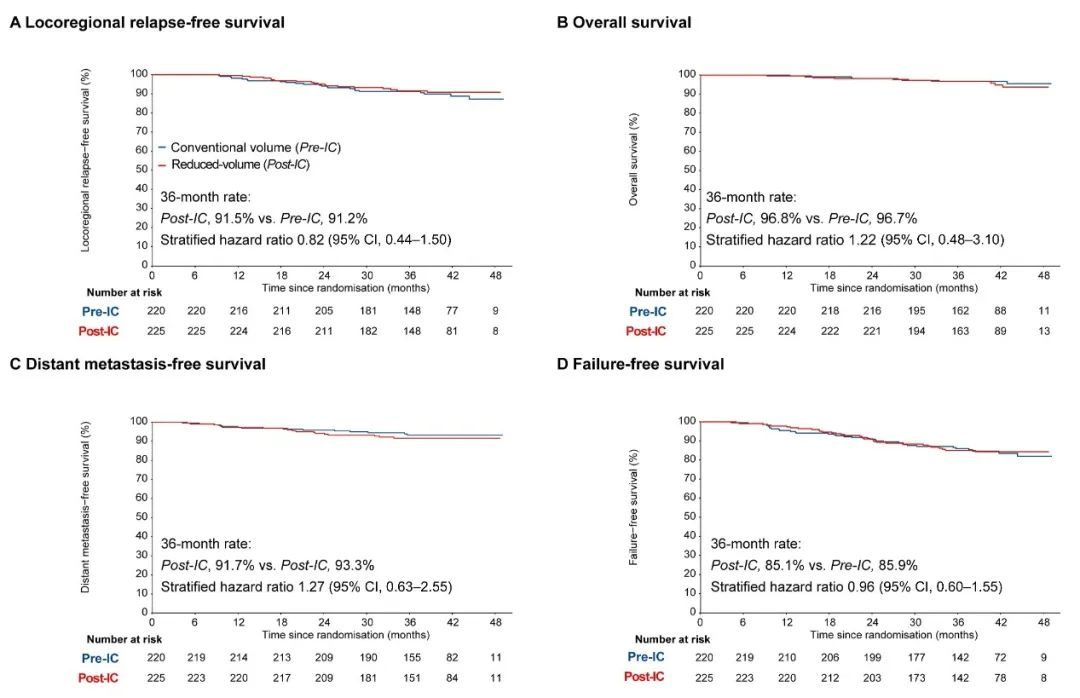
二、剂量及疗效分析
研究结果显示缩小体积放疗组接受根治剂量的平均体积为66.6 cm³,而传统体积放疗组为80.9 cm³。随访40.4个月后,缩小体积放疗组的3年局部区域无复发生存率为91.5%,传统体积放疗组无复发生存率为91.2%,且两组患者总生存率相似。这一结果表明,减体积放疗在保证疗效的同时,显著降低了对周围正常组织的辐射剂量。
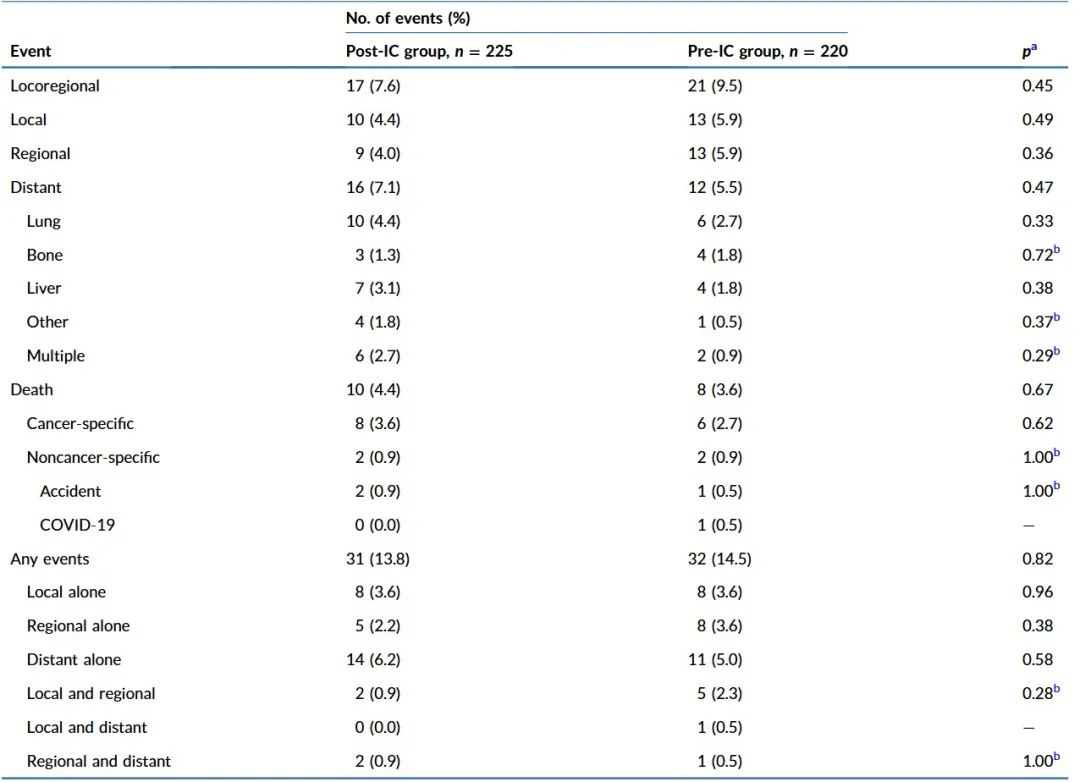
三、不良事件与生活质量
研究发现缩小体积放疗组的3-4级放射相关毒性发生率较低,包括放疗期间严重放射性口腔黏膜炎(缩小体积放疗组vs传统体积放疗组:19.8% vs. 34.1%)放疗后晚期严重放疗相关性中耳炎(9.5% vs. 20.9%)和口干(3.6% vs. 9.5%)的发生率,同时改善了患者的总体健康状况、体力状况和情绪功能,降低了患者口干和唾液粘稠的症状。这些毒性反应的降低不仅减轻了患者的痛苦,还减少了因治疗毒性导致的长期并发症风险,且提高了患者的生活质量及心理健康。
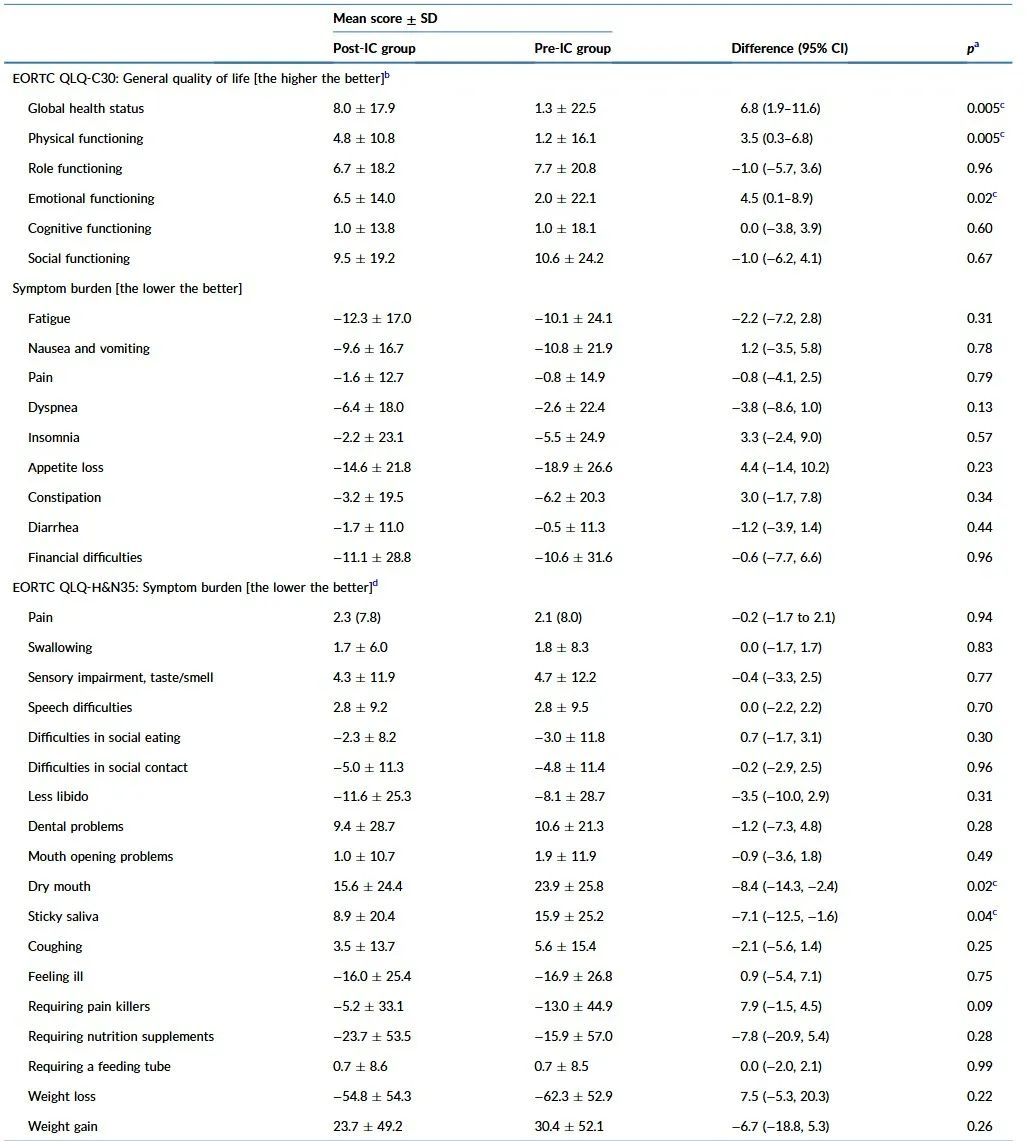
小结
在这项III期、多中心、随机对照试验中,研究人员证实了缩小体积放疗所得疗效与传统体积放疗疗效是相似的,但缩小体积放疗能够提供给患者更低的晚期毒性、更高的生活质量及预后。
这项研究具有以下创新点:
一、减体积放疗概念的提出:研究首次提出基于诱导化疗后肿瘤体积变化的减体积放疗方案,突破了传统放疗模式的局限。
二、多中心、随机对照设计:作为全球首项针对鼻咽癌减体积放疗的多中心、随机对照III期临床试验,该研究严格遵循国际标准,确保了结果的科学性和可靠性。
三、全面评估生活质量:研究不仅关注治疗效果和毒性反应,还通过标准化问卷对患者的生活质量进行了长期随访评估,填补了以往研究的空白。
该研究的成功实施为鼻咽癌的精准放疗提供了新的标准,有望改写未来治疗指南。
参考文献:
[1] Tang LL, Chen L, Xu GQ, et al. Reduced-volume radiotherapy versus conventional-volume radiotherapy after induction chemotherapy in nasopharyngeal carcinoma: An open-label, noninferiority, multicenter, randomized phase 3 trial.CA Cancer J Clin. Published online February 19, 2025. doi:10.3322/caac.21881


