不做手术也能治?61岁子宫内膜癌肺转移患者的个体化治疗历程 | MDT病例分享
时间:2024-11-26 16:00:30 热度:37.1℃ 作者:网络
01 病例介绍
患者基本情况
患者:女,61岁
首次住院时间: 2020.12.10
主诉:发现子宫内膜癌1月
现病史:2020.11 因“绝经后阴道不规则出血4月,加重2天”就诊于西安市第四医院,11.8 行“宫腔镜下诊刮术”,术后病理:宫腔小块组织低分化子宫内膜样癌,ER(+),PR(+),Ki67(70%),p53(灶+),p16(斑片+),CD10(-)。
既往史:半年前查见肝硬化、脾大、血小板减少症 ,食管胃底静脉曲张。输血前检查:乙肝五项:2,5 阳性,余阴性。
妇科查体:外阴:(-) ;阴道:(-) ;宫颈:直径3cm,光,质中;盆腔:宫体饱满、表面尚光滑,活动度可;双侧宫旁:(-);三合诊:(-)。
入院血常规: 白细胞 2.42,血小板 73
初步诊断:子宫内膜样腺癌III级
治疗经过
2020.12.11 CT:右肺下叶胸膜下小结节,建议定期复查。右肺中叶及左肺上叶舌段条索灶。
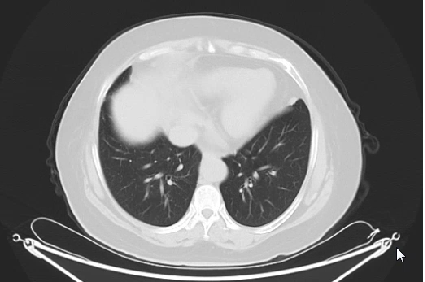
2020.12.14 MRI:子宫内膜癌,侵及深肌层,子宫峡部,右上方肠管受侵不除外。
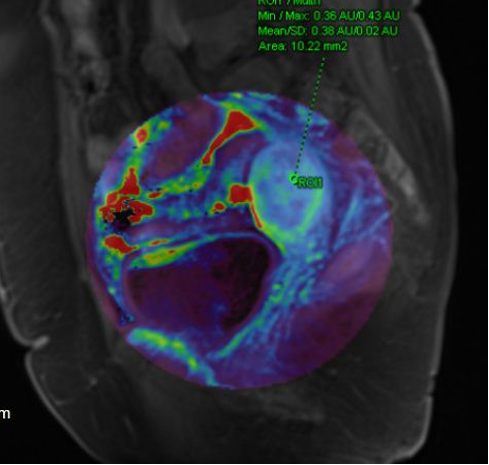
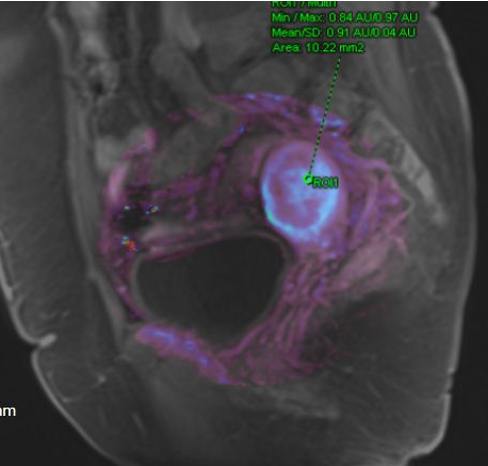
外院诊刮病理我院会诊:片内结构结合外院免疫组化结果提示考虑子宫内膜样腺癌III级。
院内MDT:
传染科:Child分级B,可耐受出血量不多的手术,需尽快缩短手术时间。
麻醉科:术前需行肝功能支持治疗、血压控制、血常规对症处理。
普外科:深肌层受侵,子宫底部病灶与周围肠管关系密切,必要时有可能行吻合术。
妇瘤科:患者手术风险大,需控制手术时间和术中出血,但是选择放疗也存在放疗导致肠瘘的风险。
综合风险后,家属要求行根治性放疗。
2021.1开始行体外放疗 VMAT:Dt :48.1Gy/26f,单次剂量1.85Gy/f。
随后行腔内后装治疗,上双管,共3次的累积剂量:末次放疗时间2021.4.30。
HR-CTV:D90-EQD2:14.52/18.01Gy
累积剂量:66.11Gy
直肠:8.62/10.1Gy
乙状结肠:7.95/8.9Gy
膀胱:10.23/13.1Gy
小肠:8.39/9.6Gy
2021.5.26 盆腔MRI:子宫病变范围较前缩小,宫颈黏膜增厚,较前无著变。
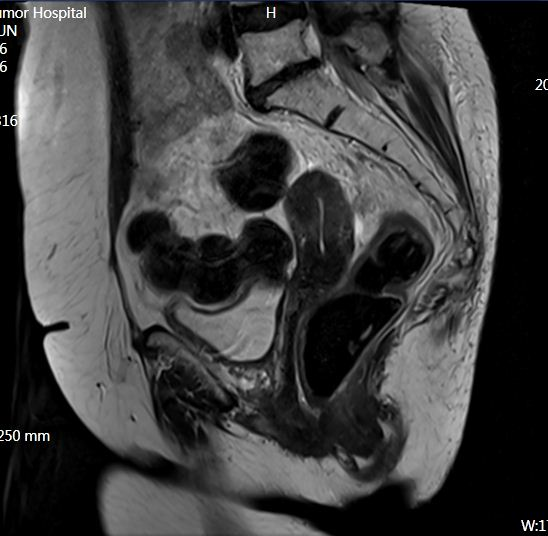
2021.5.26 CT:肝胃间隙及腹主动脉旁多发小淋巴结,肝周少许积液,同期无著变。网膜、肠系膜及腹膜影增厚。
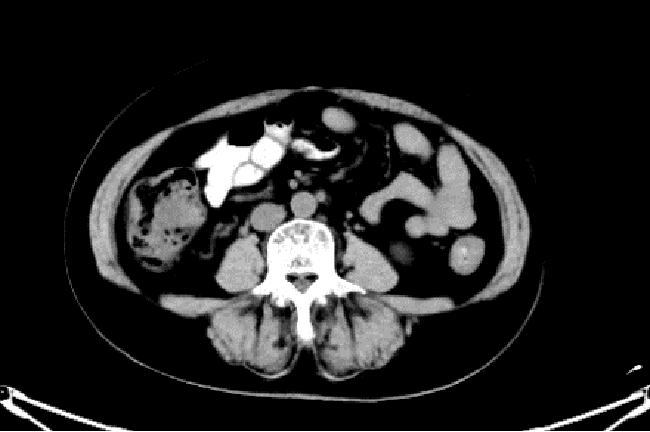
2021.5.26 CT:双肺多发结节影,较前增多、增大,提示肺转移瘤。右肺中叶及左肺上叶舌段条索状同期无著变。
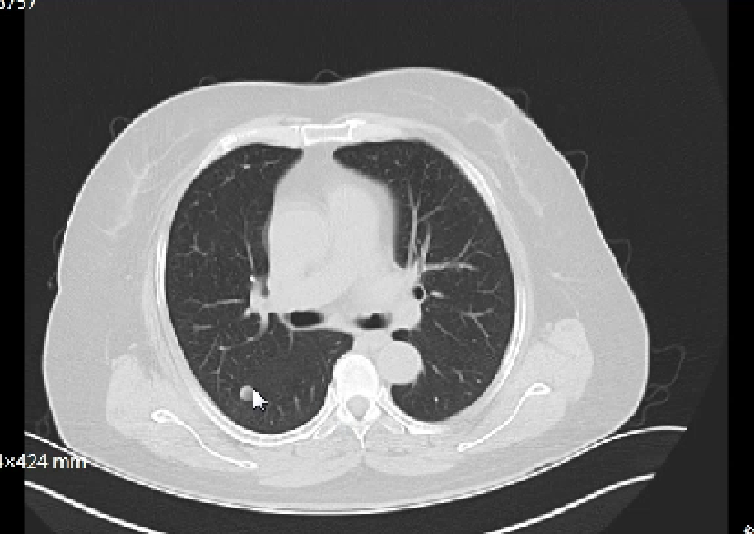
再次行免疫组化检测:PD-L1(-);
错配修复蛋白检测:MLH1(-),MSH6(+),PMS2(-),MSH2(+),结果判读为:dMMR。
2021.6.8,7.20,8.27,9.25,11.3,12.19,2022.2.25全身化疗:替雷利珠单抗200mg*7次+顺铂80mg*4次、100mg*3次。
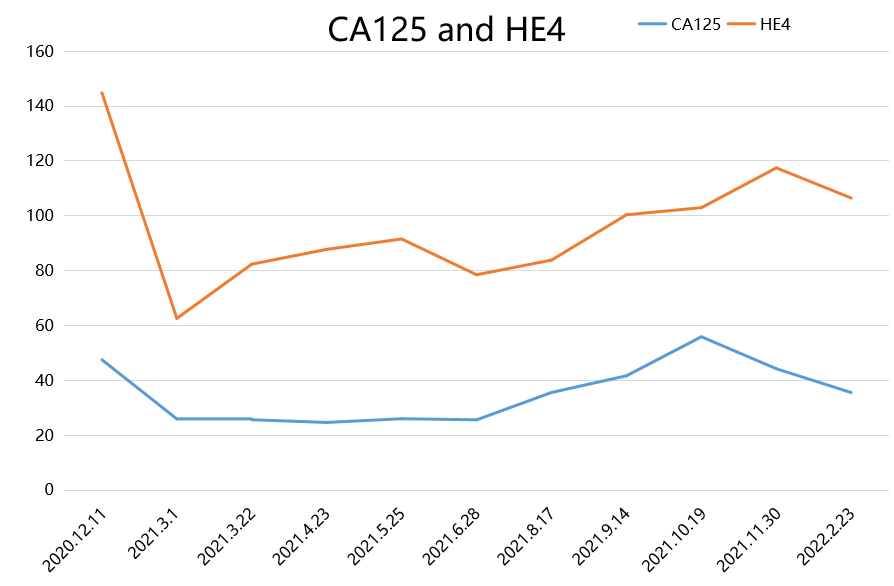
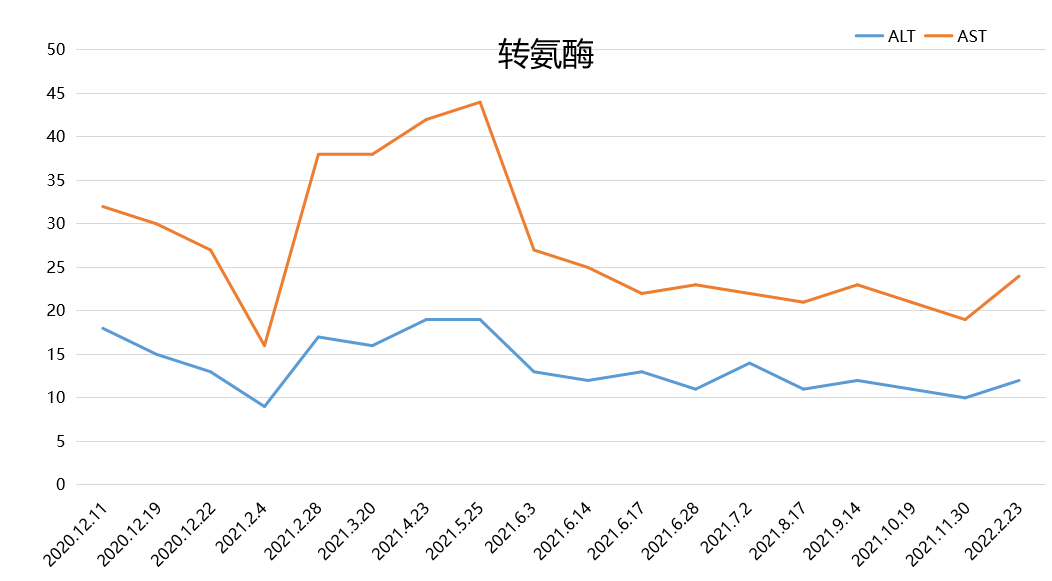
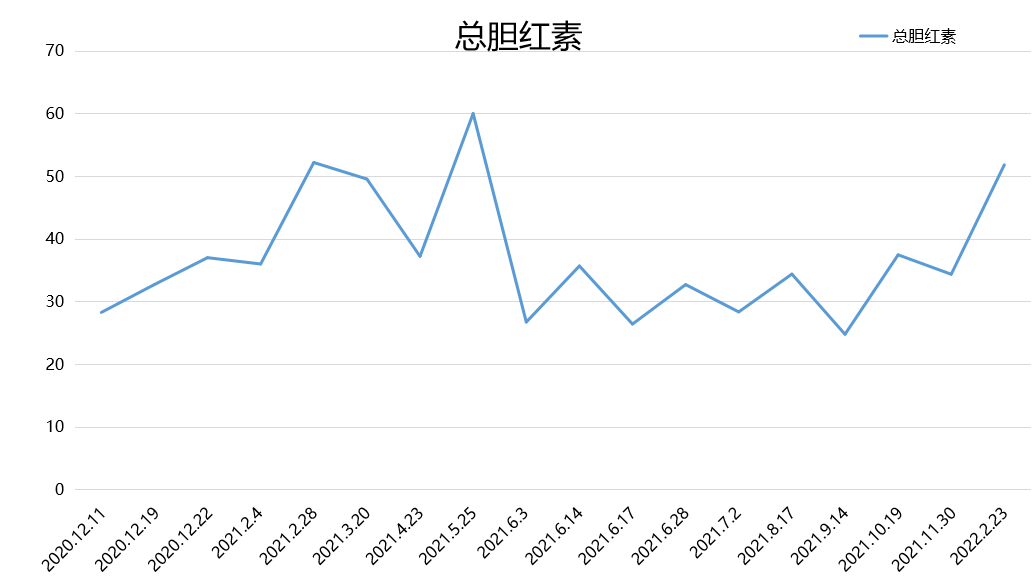
2021.9.16 CT:双肺多发结节影,提示肺转移瘤,同2021.5.26对比部分较前缩小。右肺中叶及左肺上叶舌段条索状同期无著变。
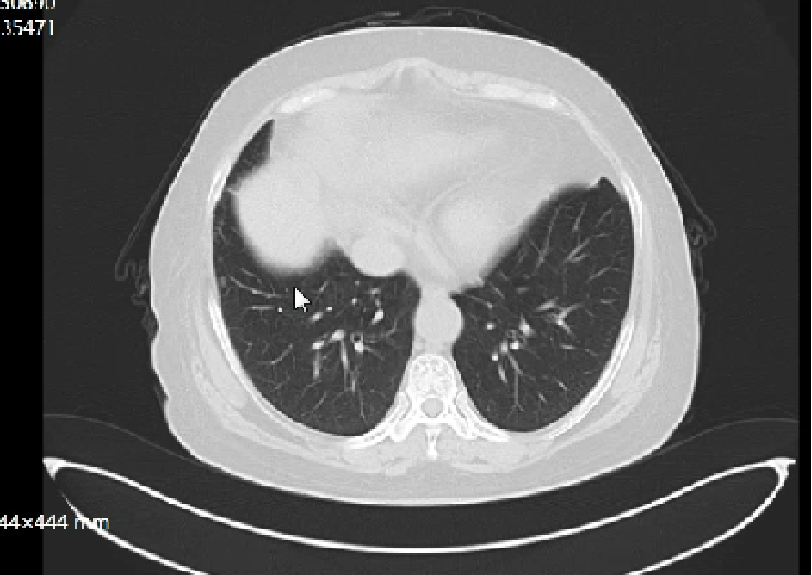
2021.9.16 盆腔MRI:子宫肌层信号欠均匀,DWI未见显著扩散,较前变化不著。
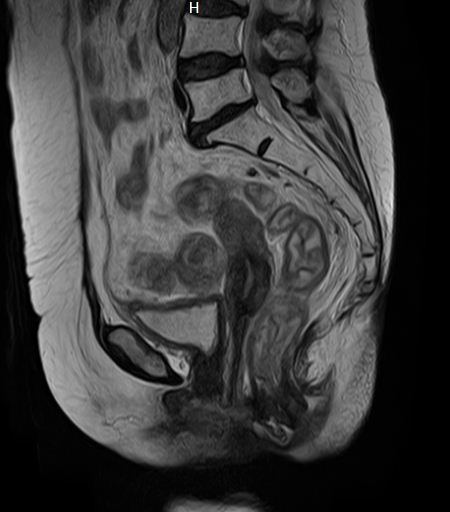
2021.12.2 CT:双肺多发结节影,同2021.9.16对比无著变。
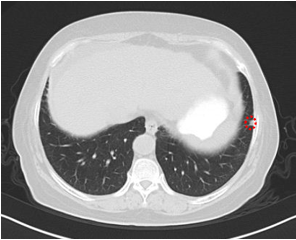
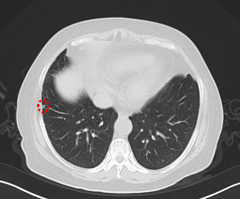
2021.12.2 CT:肝脏表面呈波浪样改变,系肝硬化征象。
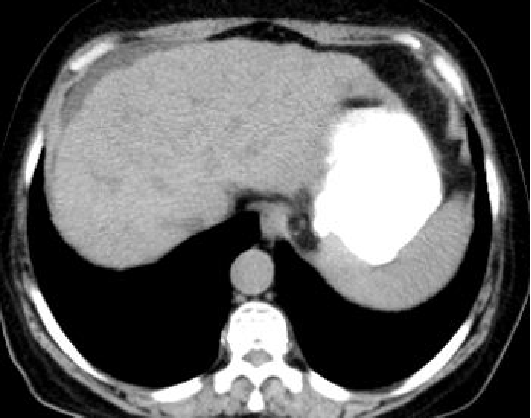
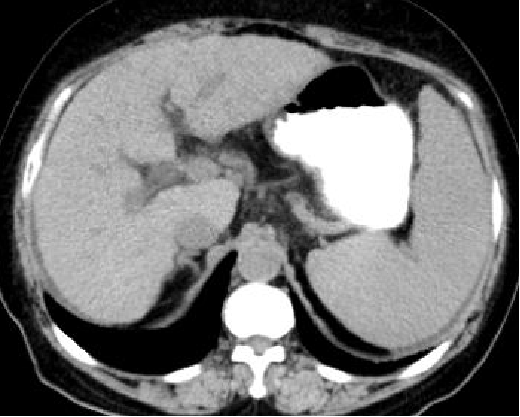
2022.2.24 CT:结节影同2021.12.2对比无著变。
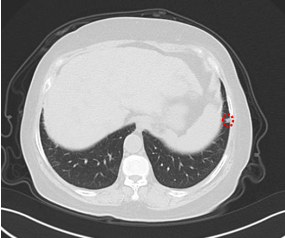
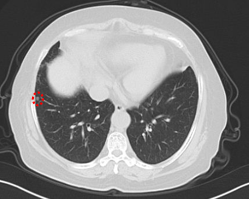
2022.07.04 CT:提示免疫性肺炎可能。
处理:单药顺铂80mg,并予以口服泼尼松治疗免疫性肺炎。
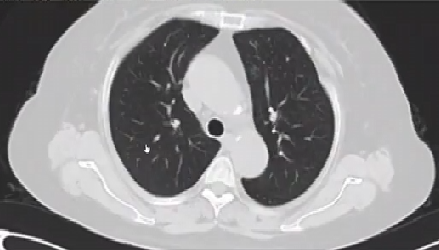
2022.10 CT:肺部病灶较前好转,继续于2022.10.09,2023.03.24行替雷利珠单抗200mg*2次+顺铂80mg*2次。
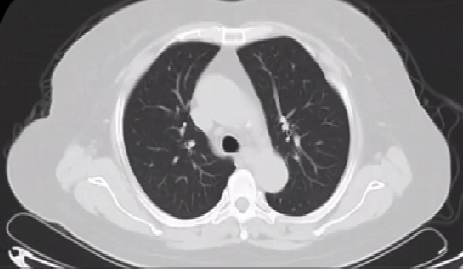
2023.08 MRI:经MRI充分评估未见肠管明显受侵的证据后,加用靶向治疗维持,继续于2023.08.03行替雷利珠单抗200mg+顺铂80mg+贝伐珠单抗500mg。
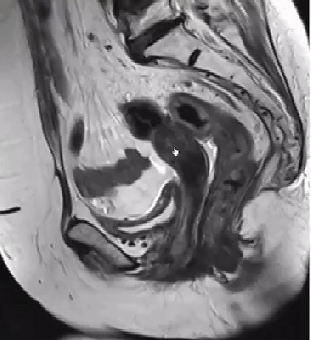
2023.10 CT、MRI:考虑患者间断应用顺铂达12次,且目前治疗效果稳定,后续维持治疗建议免疫+靶向,遂继续于2023.10.13,2024.01.10行替雷利珠单抗200mg+贝伐珠单抗500mg。
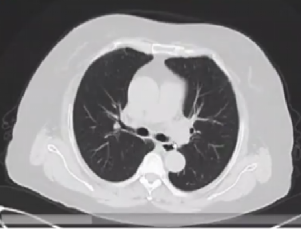
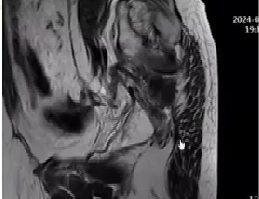
2024.04 CT、MRI:双肺结节影同前无著变,肠系膜及腹膜增厚,部分较前好转。子宫腔内未见DWI明显扩散受限。
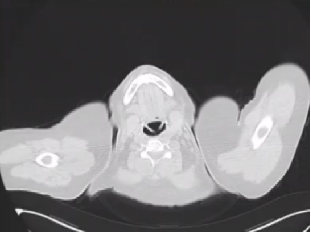
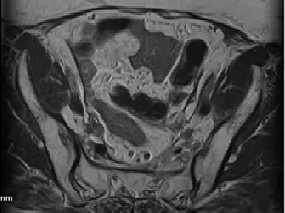
治疗经过小结

02 病例讨论
问题 1:患者目前SD,后续继续应用该方案维持的频率如何把控,还是在合适的时机停药?对于一些特殊情况的患者,个体化治疗是否是更加合适的方式?
青海大学附属医院-肿瘤妇科-李妍:在席教授分享的这个病例中,我们可以看到一个非常典型的个体化治疗的案例。这个病例的复杂性主要体现在患者的多重健康问题上,例如肝功能不全(Child-Pugh B级)、脾亢等,这些都对标准化治疗方案的实施带来了挑战。然而,通过个体化的治疗策略,包括放疗、化疗和后续的维持治疗,最终取得了良好的效果。我对这个病例存在几个疑问。
首先,患者在2020.12做了第一次胸片,2021.01开始放疗,2021.05发现肺转移,如果在2020.12胸片中能早期发现并确认肺部的小结节为转移病灶,比如通过PET-CT或穿刺,可能化疗和放疗的时机会有所调整,使患者获得更好的治疗获益。当然,在临床上并不是每位患者都会做PET-CT或肺穿刺,这也取决于患者的情况以及影像科医生的经验判断。
其次,这位患者在治疗过程中出现了脾功能亢进和血小板下降,显然对化疗产生了一定影响。对于维持治疗,目前针对卵巢癌的PARP抑制剂、宫颈癌的贝伐珠单抗、卡度尼利单抗已经写进指南或共识,但对于子宫内膜癌的维持治疗还缺乏明确指导。这名患者当前处于SD状态,后续治疗需结合其一般情况及免疫性肺炎等因素进行决策。
关于患者的激素使用问题,长期使用40mg泼尼松是否会影响免疫治疗效果?我查阅了一些文献,发现通常PD-1或CTLA单抗治疗过程中如果需要使用糖皮质激素(如预防紫杉醇类药物的过敏反应),一般不会显著影响治疗效果。然而,也有研究表明,如果基线治疗中泼尼松的剂量超过10mg,可能会降低免疫疗法的效果。一篇2019年发表在《Journal of Clinical Oncology》上的文章指出,糖皮质激素在处理肿瘤相关症状(如脑转移或骨转移)时可能影响疗效,但在非肿瘤因素(如类风湿关节炎或过敏)下使用则不影响疗效。因此,我认为后续可以继续尝试免疫抑制剂维持治疗。
分子分型在子宫内膜癌中的应用也十分重要,2020年NCCN指南及2023年FIGO分期都将分子分型纳入子宫内膜癌管理。分子分型不仅能指导治疗策略,还可为患者保留生育功能的决策提供依据。例如,对于不同的分子分型,手术方式的选择可能会有所不同。分子分型的临床价值不仅体现在治疗策略的制定上,还包括免疫和靶向药物的应用,以及生育功能保留的决策。
对于维持治疗中是否添加内分泌治疗方案,我认为这是一个可行的选择。尤其在ER/PR阳性情况下,内分泌治疗可能在维持治疗中发挥积极作用。此外,患者因肝硬化导致门静脉系统回流问题,脾脏增大引起血小板减少,或许可以考虑多学科会诊。是否能够耐受脾切除手术,或通过介入下的脾动脉栓塞治疗,也应作为综合考虑的选项。
甘肃省人民医院-妇科二病区-曲波:这个病例的主管医生是放疗科专业的,如果这个病人在我们手术科室进行治疗,尽管存在肝脏问题和血小板偏低的情况,我个人认为如果患者能够接受手术,预后可能会更好。原因如下:
首先,内膜癌常见于子宫及其周围组织的浸润,但累及肠管的风险相对较低。虽然影像学检查未能完全排除这一可能,但在临床实践中,肠管被累及通常需要伴随子宫穿孔或盆腔积脓、积血等情况。因此,对于本病例,若与家属沟通后能进行微创手术切除原发病灶,可以有效降低肿瘤复发的概率。即使在复发的情况下,切除干净的内膜癌预后也优于未切除干净的情况。
其次,根治性放疗可能对全身状态有影响。根治性放疗通常需要较长的疗程,并且常需配合化疗,时间跨度大,可能对身体造成更大的系统性影响。而手术的话,术后的预防性治疗剂量和疗程相对较低,对机体的影响也较小。
另外,对于已经进行手术或根治性放疗的患者,以预防或降低肿瘤复发风险为目的的辅助治疗选择的话,免疫治疗的理论依据尚不充分。免疫治疗更适用于姑息性手术后、治疗后残留或持续存在肿瘤的患者。
虽然免疫治疗近年来发展迅速,但根据数据显示,2023年1月的子宫内膜癌NCCN指南推荐,PD-1单抗(如帕博利珠单抗、纳武利尤单抗、多塔利单抗)适用于dMMR患者,仑伐替尼用于dMMR或非MSI-H的患者,其ORR约为47%,中位OS为65.4个月。结合分子分型,如果患者为dMMR,根治性放疗后可以考虑TC化疗联合免疫治疗作为预防复发的策略。RUBY实验表明,对于dMMR患者,使用紫杉醇卡铂加度伐利尤单抗治疗后,可以通过免疫单药进行维持治疗。对于非dMMR或MSS的患者,则可以考虑免疫联合PARP抑制剂的维持治疗方案。
此外,患者的肺转移可能是在治疗过程中出现,或在初期未发现后期逐渐进展。对于维持治疗,可以进一步考虑检测HER2状态或加入PARP抑制剂,以优化治疗效果。
西安交通大学第一附属医院-肿瘤放疗科-施璠:这类患者在临床上治疗确实非常棘手,因为合并肝硬化的情况使得传统治疗手段难以规范使用。就如曲波教授提到的手术方案,且不论治疗前CT检查中肺部小结节的性质,即使假设当时肺结节不存在问题,考虑到患者深基层浸润至少为1b期,加上FIGO 3级的病理分级,也就是确定为1BG3。这样的患者即使完成手术后进行完全分期,仍需要进行放疗。席教授团队在MDT讨论后可能正是考虑到手术风险较大,才未选择手术治疗。
患者虽然血小板下降至73,程度不算严重,但对手术医生来说仍有影响。综合各方面因素后,团队选择了个体化的治疗方案。这种情况在临床上并非个例,我们经常遇到子宫内膜癌合并肝功能不全、肝硬化或心脏病的患者,治疗起来都比较棘手,难以完全按照指南执行。对这类患者,我们更强调个体化治疗,制定符合患者身体状况和耐受程度的方案,而非完全遵循规范治疗。
就本例而言,如果在我们医院,患者一开始就会进行分子分型检测。现在无论是手术后还是放疗前的患者,在取得病理后都会进行分子分型检测,因为这对后期治疗非常关键。本例患者初始治疗时仅取活检,未做分型。如果早期发现是MSI-H患者,可能会考虑在放疗期间或后装时就联合免疫治疗,随后进行维持治疗,这样或许可以预防肺部病灶的进展。
关于肺部结节,从发现到明显增大不到半年,且在放疗结束后即发现增大,说明这些结节初期可能就有问题,只是太小未达到诊断标准。到2021年5月时,右肺下叶的结节已可以进行穿刺活检。建议完善这项检查,毕竟病理是金标准。患者治疗后虽然维持SD状态,某些病灶其实在缩小,应该算作PR。获取病理证据对后期治疗方案的选择和医生的自我保护都很重要。
关于靶向治疗的时机,考虑到患者的肝功能问题和肝硬化情况,在2021年5月发现肺转移进展时,选择了替雷利珠单抗联合顺铂。这时加入免疫治疗或靶向治疗(如口服安罗替尼或贝伐珠单抗)都是可行的选择。另外,考虑到患者ER、PR免疫组化阳性,可以考虑加入内分泌治疗。
关于脾抗问题,患者出诊时血小板73%,情况不算严重。如果继续下降,作为放疗科医生,我们可以通过放疗来解决血小板减少的问题,效果通常很好,无需进行介入治疗。
03 MDT小结
该病例是一位64岁的晚期结直肠癌患者,在2010年行结肠癌根治术,2021年复发肝转移。当时,经过MDT讨论,患者被诊断为初治潜在可切除,分子分型显示为RAS和BRAF基因野生型。通过西妥昔单抗联合双药化疗的转化治疗,患者达到了显著的疗效。值得称赞的是,该病例在关键治疗节点均有MDT团队的参与。
结合后期发现病灶的增大及留存的依据,当初这个病例可能是一个非转移性病变。从这个病例中,我们学到了很多知识。虽然手术是主要治疗手段,但一定要进行个体化治疗。K药联合化疗在去年才获得指南认证。虽然之前大家已在使用,但我们需要考虑有没有指南的推荐。
对于这样一个dMMR获益的患者,从其他瘤种的大型研究来看,免疫治疗效果显著。这个病例经过深思熟虑采取了的个体化治疗方案,确实取得了较好的疗效。目前的维持治疗可以继续进行,如果后期出现进展或其他问题,可以考虑转换治疗方案。主管医生可能考虑到患者的肝功能问题,因为免疫相关性肝损害比较常见,需要考虑多方面因素。目前患者处于相对稳定状态,这样的治疗方案是可以接受的。另外值得一提的是分子分型的重要性。2023年版子宫内膜癌分期已经纳入了分子分型,这将指导未来的治疗方向。
述评
西安交通大学第一附属医院-肿瘤放疗科-刘孜:从妇科肿瘤免疫治疗的角度来看,免疫治疗在子宫内膜癌的治疗中显得尤为重要,特别是在晚期及复发转移的病例中。然而,子宫内膜癌与宫颈癌的不同之处在于分子分型的重要性。无论是在早期、晚期还是复发转移阶段,分子分型对于帮助我们为患者选择最佳治疗方案,尤其是选择合适的免疫药物或激素治疗,起到了关键作用。
对于没有特殊情况的患者,按照规范化的标准处理是首要任务。而对于特殊患者,如合并其他疾病、复发转移或处于晚期(如ⅣB期)的患者,则需要进行个体化处理。在个体化治疗中,我们需要平衡疾病治疗的得与失以及患者的经济状况。在选择免疫药物时,也必须考虑到患者的经济承受能力。
在临床实践中,我们常见类似的复杂病例,如子宫内膜癌患者合并肝功能不全、肝硬化或心脏病等,这类患者的治疗相对棘手,难以完全按照指南进行。因此,对于这类患者,个体化治疗尤为重要,需要多学科协作,制定适合其身体状况和耐受能力的治疗方案,而不完全依赖规范化治疗。
关于子宫内膜癌近距离治疗的选择,我认为是不确定性的。近距离治疗相比外部照射放疗,有其独特的优势。近距离治疗不仅可以降低局部复发率,还相对安全简便,特别适用于医疗资源有限的单位。然而,目前指南尚未将调强放疗的数据纳入其中,因此在选择放疗方式时,我们需要综合考虑病理分级、分期、浸润深度、危险因素以及基因分型等多种因素。
再来说说近距离治疗的具体方案,目前我们使用的是7×3和6×4的剂量方案。实际上,这两种方案在意义上是相似的,因为一个是以粘膜参考点,一个是以粘膜下0.5公分的参考点。根据距离平方反比定律,按等效剂量(EQD2)计算,两者的等效剂量值差不多,所以在剂量选择上没有问题。但我们需要关注的问题是总剂量是否足够。
常见的问题是我们的总剂量可能不够,因为达到的总剂量往往只有40 Gy左右。40 Gy从预防治疗的角度来看肯定是不够的。因此,包括协和医学院在内,有些机构会选择6次6 Gy的方案。而对于我们来说,也是坚持这样的方案;如果不加外照射,就必须将后装的剂量推上去,否则达不到50 Gy,就无法实现预防效果。因此,从放疗剂量角度讲,我们必须讲求客观和精准。


