纳米材料免疫疗法,最新Nature系列综述!
时间:2025-03-10 12:08:54 热度:37.1℃ 作者:网络
免疫疗法,尤其是免疫检查点抑制剂(ICIs),在过去十年中彻底改变了癌症治疗的格局,但在实际应用中仍面临诸多挑战,例如对免疫“冷”肿瘤效果不佳以及可能引发免疫相关不良事件(irAEs)。与此同时,肿瘤微环境(TME)的研究逐渐深入,揭示了其在肿瘤免疫逃逸中的关键作用,包括免疫抑制细胞的存在、代谢产物的积累以及缺氧、酸性环境等特征,这些都限制了免疫疗法的效果。纳米技术在药物递送领域的应用逐渐成熟,但传统的纳米药物递送系统往往缺乏肿瘤特异性,导致药物在非肿瘤组织中的释放,限制了其临床应用。因此,开发能够响应肿瘤微环境特征的“肿瘤响应型”纳米材料成为了一个重要的发展方向。尽管肿瘤响应型纳米材料在临床前研究中显示出良好的抗肿瘤效果,但其临床转化仍面临诸多挑战,如肿瘤的异质性、临床前模型的局限性以及纳米材料的生产、质量控制和监管审批等问题。然而,随着纳米技术的不断发展以及对肿瘤微环境和免疫反应的深入理解,肿瘤响应型纳米材料有望克服这些挑战,为癌症治疗带来新的突破。
麻省理工学院Giovanni Traverso、Robert Langer等人详细分析了TME的特性,以及如何通过设计能够响应TME特征的纳米材料来实现免疫治疗药物的靶向递送和精准释放,从而提高治疗效果并降低副作用。相关内容以“Enhancing immunotherapy with tumour-responsive nanomaterials”为题发表在《Nature Reviews Clinical Oncology》上。

【主要内容】
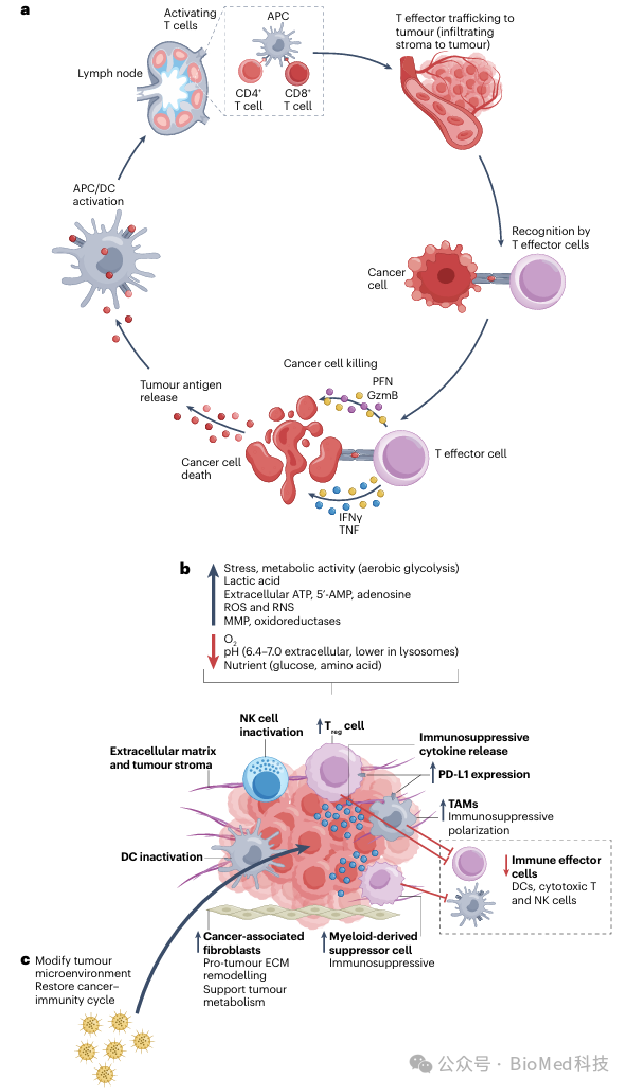
图 1 肿瘤免疫循环与免疫抑制性TME的关系
该图展示了免疫系统识别和清除肿瘤细胞的动态过程,即“癌症-免疫循环”。在正常情况下,肿瘤抗原被抗原呈递细胞(APC)捕获并激活T细胞,随后T细胞进入肿瘤组织并杀死肿瘤细胞,释放更多抗原,进一步增强免疫反应。然而, TME通过多种机制抑制这一过程。TME中存在免疫抑制细胞(如调节性T细胞、肿瘤相关巨噬细胞等)、代谢产物(如腺苷、乳酸等)以及酸性pH、缺氧等条件,这些因素共同作用,阻碍T细胞的浸润和功能发挥,导致免疫逃逸。图中还展示了纳米材料如何通过靶向TME中的特定特征(如酸性pH、酶等),实现药物的精准释放,从而改变TME的免疫抑制状态,恢复有效的癌症-免疫循环。
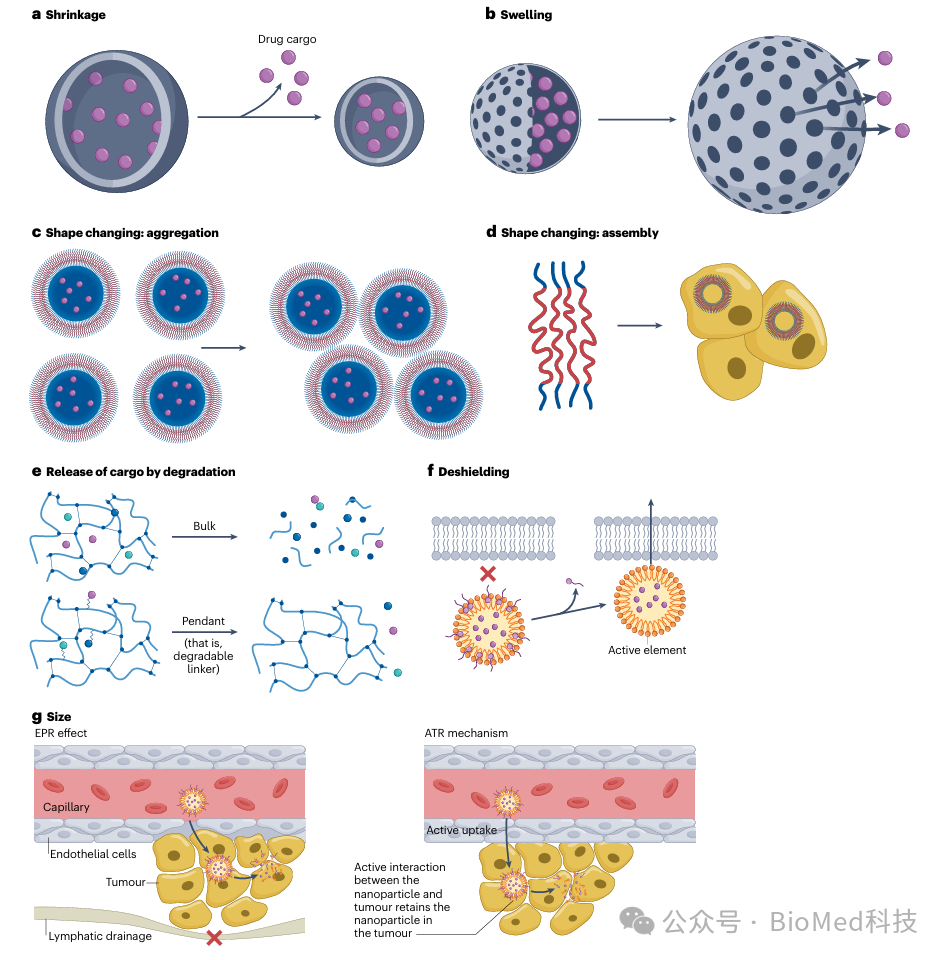
图 2 肿瘤响应型纳米材料的药物释放机制
该图总结了肿瘤响应型纳米材料在肿瘤微环境中释放药物的多种机制。这些机制包括纳米材料在肿瘤组织中的尺寸变化(如膨胀或收缩)、形状改变(如聚集或解体)、化学键断裂(如酸性或氧化还原敏感的连接键断裂)以及表面修饰的去除(如PEG层的脱除)。这些变化可以由TME中的酸性pH、高浓度的活性氧(ROS)、特定酶或高ATP水平触发,从而实现药物的靶向释放。图中还展示了这些机制如何通过增强药物在肿瘤中的积累和保留,提高治疗效果并减少全身毒性。
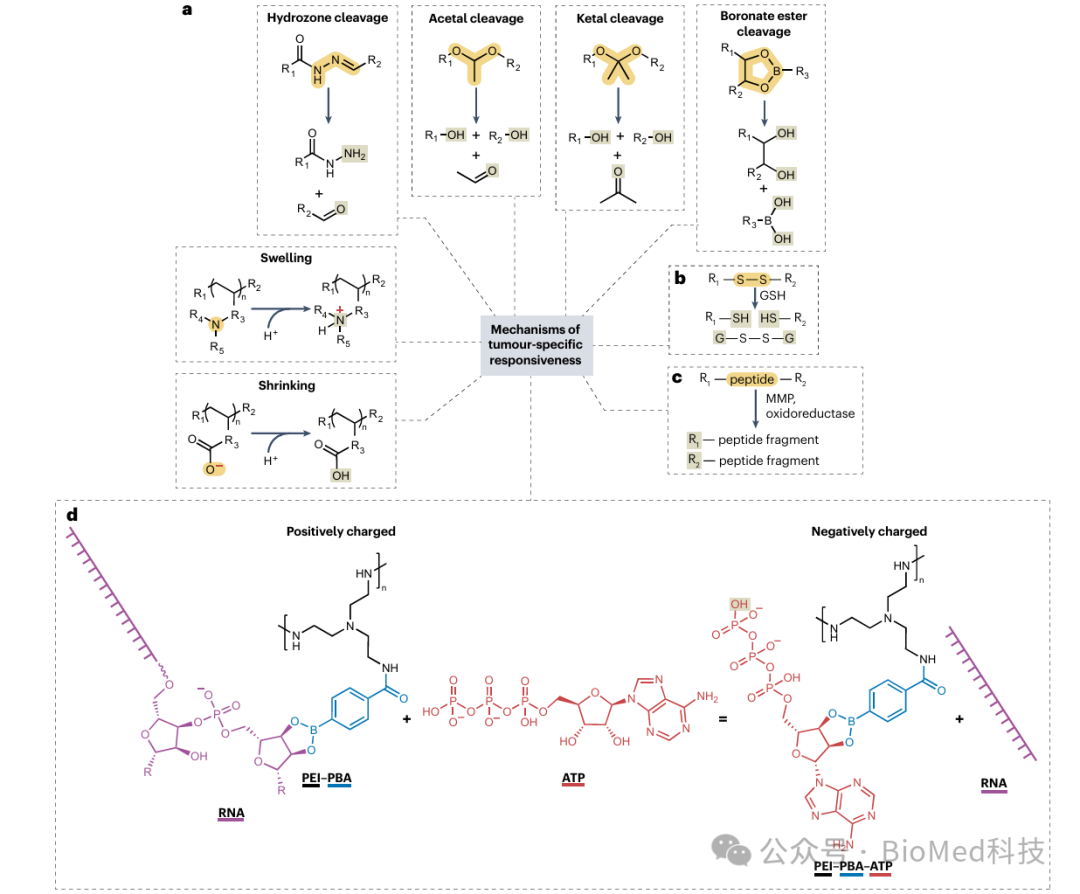
图 3 肿瘤微环境响应型纳米材料的功能基元
该图详细描述了能够赋予纳米材料肿瘤特异性响应功能的化学基元。这些基元包括:
1. pH敏感型材料:通过酸性条件下可断裂的化学键或聚合物链的膨胀/收缩,实现药物在TME中的释放。
2. 氧化还原敏感型材料:利用肿瘤细胞内高浓度的还原剂(如谷胱甘肽,GSH),设计可被还原断裂的二硫键,从而在肿瘤细胞内释放药物。
3. 酶响应型材料:将特定酶的底物序列嵌入纳米材料中,当遇到TME中的特定酶时,这些序列被酶切割,导致药物释放。
4. ATP敏感型材料:利用TME中高浓度的ATP,设计能够与ATP结合并响应其存在而释放药物的纳米材料。
这些功能基元的设计使得纳米材料能够精准地在肿瘤微环境中响应并释放药物,从而提高治疗的特异性和效果。
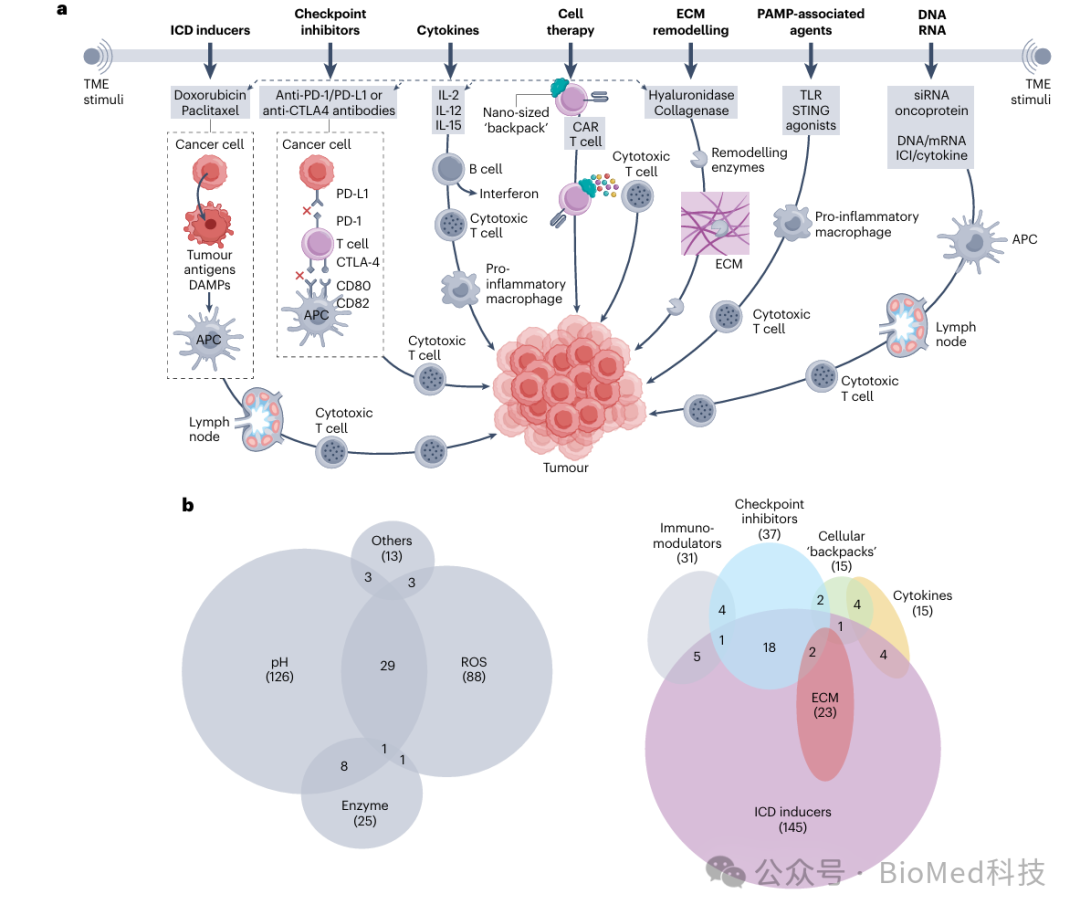
图 4 纳米材料在免疫治疗中的药物载荷应用
该图总结了肿瘤响应型纳米材料在免疫治疗中的多种应用,展示了如何将不同类型的免疫治疗药物(如化疗药物、免疫检查点抑制剂、细胞因子、核酸药物等)整合到纳米材料中。图中还展示了这些纳米材料如何通过靶向TME中的特定特征(如酸性pH、酶、ROS等),实现药物的精准释放,从而增强免疫反应并克服免疫抑制性肿瘤微环境。
【全文总结】
肿瘤响应型纳米材料为免疫疗法提供了一种新的策略,通过靶向递送药物并响应TME的特性,可以显著提高免疫疗法的效果并降低毒性。尽管面临诸多挑战,但随着纳米技术的不断发展和对TME理解的深入,肿瘤响应型纳米材料有望成为未来癌症治疗的重要工具。
原文链接:
https://doi.org/10.1038/s41571-025-01000-6


