局部使用氨甲环酸治疗黄褐斑的进展
时间:2025-02-25 12:12:20 热度:37.1℃ 作者:网络
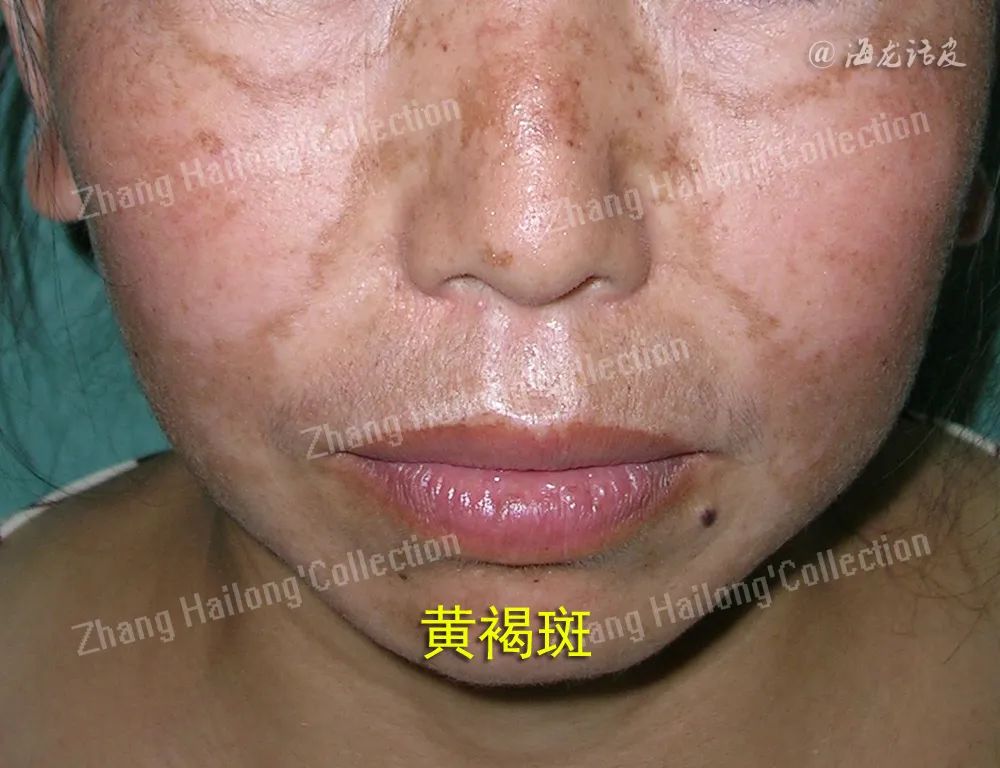
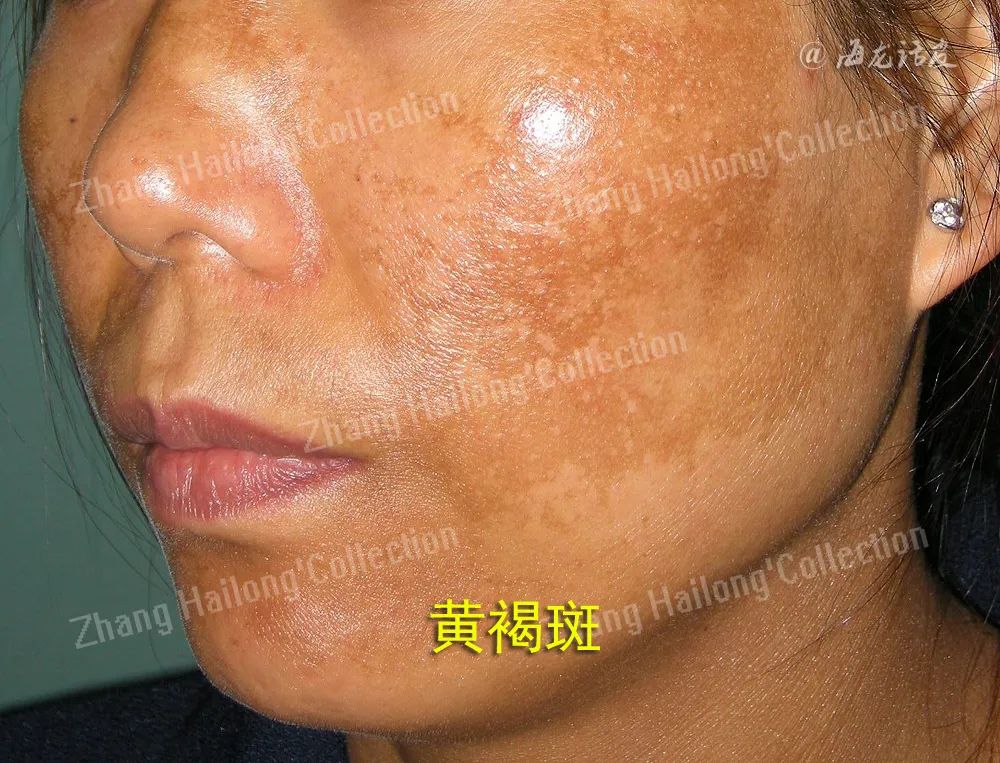
黄褐斑是一种常见的获得性色素沉着性疾病,皮损边缘不规则,呈蝶形对称分布于双颊。高发于育龄期女性,严重影响患者的面貌及心情。目前关于黄褐斑的治疗方法有很多,包括系统的药物治疗、化学换肤及激光治疗,然而这些治疗方法都有自身的局限性。
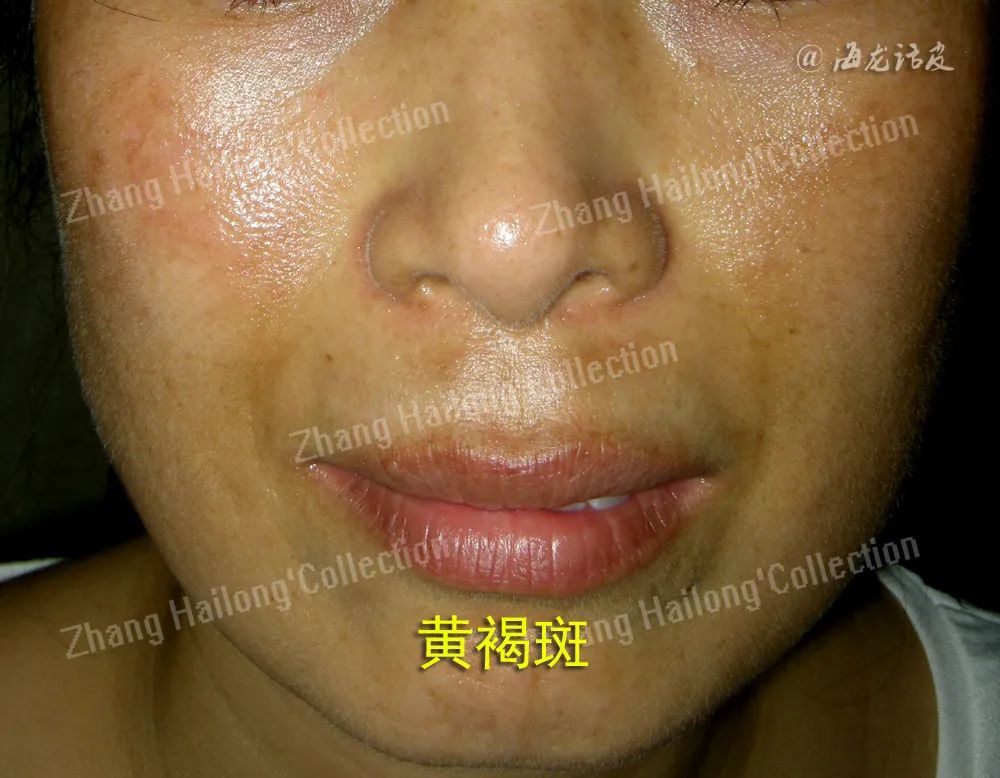
近年来许多研究证实,口服氨甲环酸对黄褐斑具有显著的治疗效果,但口服氨甲环酸有诸多不良反应和 禁忌证,致使很多患者不宜使用,而局部使用氨甲环酸可以明显减少不良反应的发生。因此,局部外用、皮内注射、联合微针或激光治疗黄褐斑表现出明显的优势。
概述
黄褐斑是一种常见的获得性色素增加性皮肤病,呈现出淡褐色至深褐色斑块。一般好发于脸颊、眼周、额部等部位,女性患病率更高,并且斑块分布具有对称性。该疾病的发病原因复杂多样,包括遗传易感性、紫外线照射、激素水平、妊娠和药物等多种危险因素。关于黄褐斑的治疗方法也有很多,包括系统药物治疗和化学换肤及激光疗法等,然而这些治疗方法都有自身的局限性,治疗无效及复发是临床常见的难题。
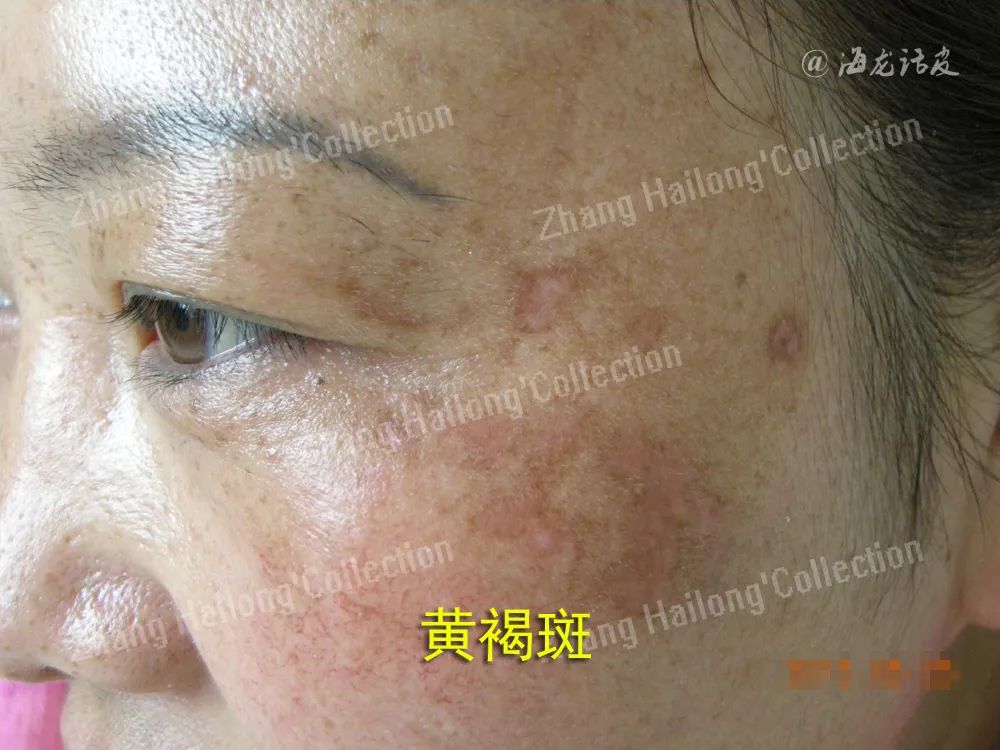
氨甲环酸(Tranexamic acid,TXA),又称传明酸,是一种纤溶酶抑制剂,通过可逆地阻断纤溶酶原分子上的赖氨酸结合位点来抑制纤溶酶原激活剂将纤溶酶原转化为纤溶酶,临床上主要用于各种情况下原发性纤维蛋白溶解所致的出血。越来越多的研究表明,口服或局部外用氨甲环酸对黄褐斑具有较好的治疗效果,目前黄褐斑在日本已被列为氨甲环酸的药物适应证。
氨甲环酸治疗黄褐斑的机制
日本学者首先发现TXA具有治疗黄褐斑的作用,TXA的化学结构为对氨甲基环己烷羧酸,与酪氨酸化学结构相似,可通过与酪氨酸竞争结合位点,阻断黑素细胞和角质形成细胞的相互作用来抑制表皮黑素细胞酪氨酸酶活性,减少黑色素生成。另有研究表明,酪氨酸酶不会受到TXA的直接作用,主要通过抑制角质形成细胞产生的单链尿激酶从而对角质形成细胞与黑素细胞之间的联系进行干扰,使得黑素颗粒转运到角质形成细胞受到明显的抑制作用。
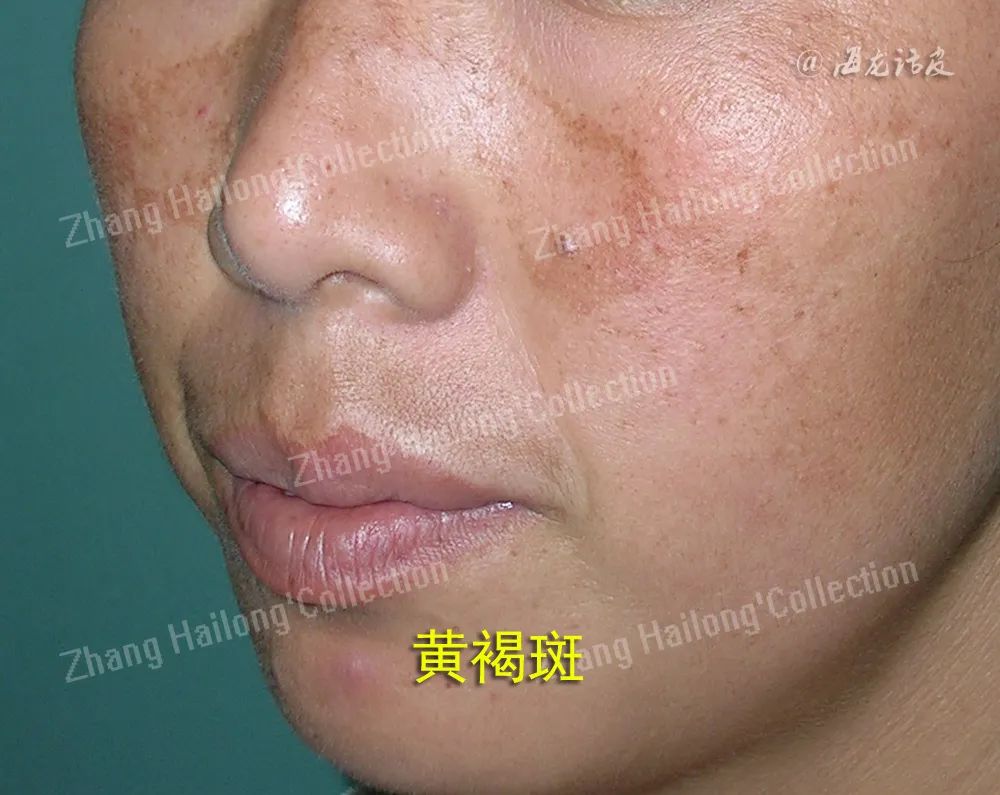
TXA是氨基酸赖氨酸的合成衍生物,通过可逆地阻断纤溶酶原分子上的赖氨酸结合位点,抑制纤溶酶原激活剂将纤溶酶原转化为纤溶酶来发挥作用。除了抗纤维蛋白溶解的作用外,TXA还被认为具有抗血管生成作用,通过抑制血管内皮生长因子受体激活,减少黑色素生成,从而改善黄褐斑。
局部外用氨甲环酸的制剂类型
注射制剂:
目前,国内已开发上市的氨甲环酸注射制剂有小容量的注射液、静脉输液、注射用无菌粉末。常用于治疗黄褐斑的TXA注射液有2ml︰0.1g,2 ml︰0.2g,5ml︰0.25g,5ml︰0.5g,10ml︰1.0g,共5种规格。
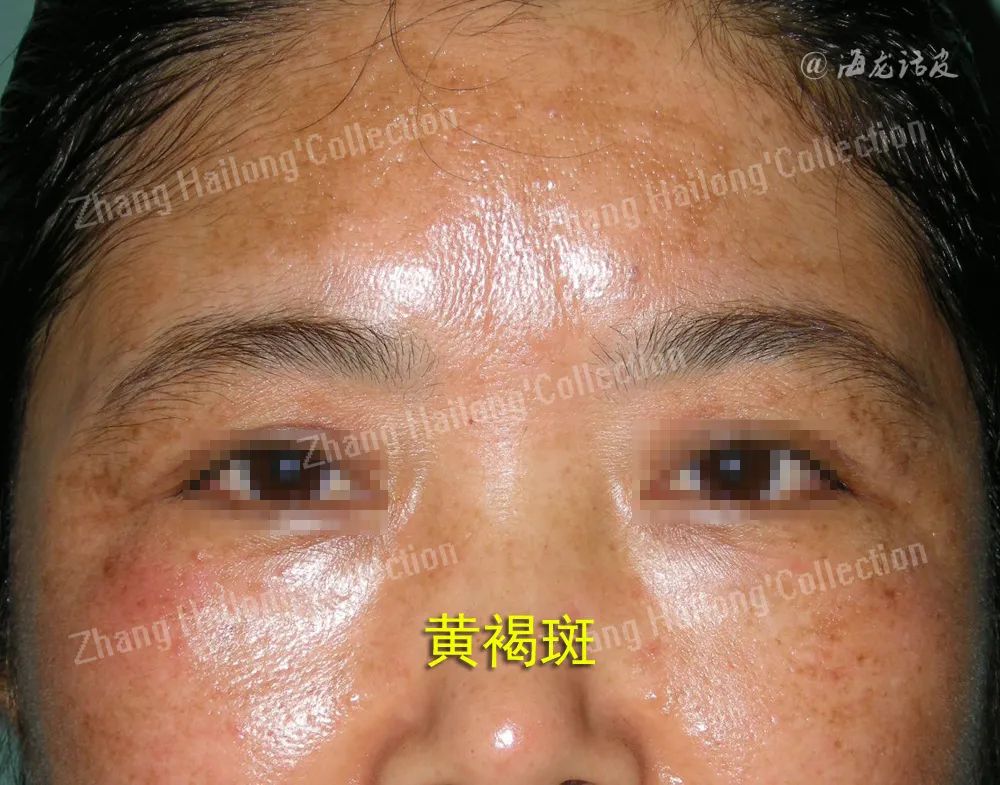
外用制剂:
目前,在化妆品市场已有各种各样的TXA专利局部给药产品。尚在研制开发的TXA外用制剂有溶液剂、乳剂、脂质体凝胶等,已使用的TXA的局部配方包括2%乳剂、3%乳膏、5%溶液和5%脂质体乳膏。
TXA水溶性和稳定性良好,可制成多种剂型,外用给药目前临床上主要是结合皮下注射后涂抹以及制备TXA脂质体的方式进行治疗黄褐斑。此种局部给药方式具有较高的生物安全性且方便患者使用。但由于TXA亲水性强,因此很难通过皮肤角质层障碍,需要通过脂质体等促渗技术对药物进行包裹从而促进经皮渗透性。如何在外用制剂中提高TXA的经皮促渗性是值得研究的课题。
局部外用氨甲环酸治疗黄褐斑的疗效
外涂TXA:
直接在患处涂抹氨甲环酸制剂,对于不能耐受口服TXA或者拒绝使用口服药物治疗黄褐斑的患者来说,是一个不错的替代选择,5%或2%为最常用的浓度。目前已有很多报道将局部TXA与传统的局部治疗进行比较。
在一项研究中,比较5%TXA乳膏和4%氢醌乳膏治疗黄褐斑的疗效和安全性试验中,MASI评分和黄褐斑生活质量评分在面部两侧均有显著改善,两侧差异无统计学意义。有一点不同的是,5%TXA乳膏的黑色素面积百分比较4%氢醌乳膏显著降低。通过 这些临床研究可以发现,TXA治疗黄褐斑具有显著疗效,从患者满意度或不良反应发生率上看,TXA的治疗效果更优于氢醌。
皮内注射TXA:
皮内注射疗法,指使用小针头将TXA溶液注射到真皮中,注射间隔1cm,最常见的浓度为4 mg/ml,一些研究已经证实皮内注射TXA治疗黄褐斑是安全有效的。在一项非随机临床实验中,通过研究比较皮内注射2mg/mlTXA和0.9%生理盐水治疗黄褐斑的疗效中发现,经过12周的持续治疗后,TXA注射半侧脸的MASI评分显著低于 生理盐水侧,并且在之后的12周随访中,依然表现这一结果。
TXA联合微针:
利用微针在皮肤上形成微伤口,配合TXA试剂更加深入地渗透到皮肤中,同时刺激皮肤胶原蛋白的产生和生长因子释放。一项双盲随机对照试验,在40例黄褐斑患者中进行治疗,对患者整个面部进行微针治疗,然后将10%TXA溶液随机应用于半侧脸,将安慰剂应用于另一侧,每隔两周进行一次。研究结果显示,TXA溶液组治疗效果显著好于安慰剂组。
TXA联合激光:
近年来,强脉冲光、染料激光(510nm)、Q开关Nd︰YAG激光(532nm)、红宝石激光(694 nm)、翠绿宝石激光器(755nm)以及剥脱性点阵激光陆续被用于黄褐斑的治疗。在既往的治疗中,常规剂量的强脉冲光和激光对于去除黑色素有较好的效果,但周围组织的热损伤会导致炎症后色素沉着。随着针对靶黑素而不破坏正常细胞或细胞内其他结构的“亚细胞选择性光热解理论”的提出,使得低能量Q开关Nd︰YAG1064 nm激光受到人们的关注。使用激光治疗黄褐斑的效果已经在多项研究中得到证实,但单纯激光治疗存在复发率高及炎症性色素沉着的问题,那么当激光联合TXA共同治疗黄褐斑是否可以减少其不良反应,增加疗效和患者满意度呢?
在一项针对中国患者的随机双盲试验中,37例患者面部随机接受半侧脸755nm翠绿宝石激光,另一侧脸激光联合TXA联合治疗,每隔4~5周治疗1次,在治疗后的第1、3、6个月进行随访。研究结果发现在随访期1~3个月,联合治疗组和单激光治疗组MASI 评分均显著降低,但联合治疗组患者的满意度显著高于单激光治疗。可见激光与TXA联合使用治疗黄褐斑的效果优于单独使用激光或者TXA治疗黄褐斑,且两者联合使用具有相加作用。
TXA联合微针与激光:
一项比较微针和QS Nd∶YAG激光与局部3% TXA凝胶联合使用治疗黄褐斑的疗效和副作用研究中60例患者被随机分为两组,A组每月接受Nd∶YAG激光治疗,每天使用3%TXA凝胶,而B组每月接受微针治疗,每天使用3%TXA凝胶。共给予治疗5次,2个月后随访,研究结果发现微针和QS Nd∶YAG激光与局部3%TXA凝胶联合治疗黄褐斑的疗效和患者满意度差异无统计学意义。
在另一项微针与点阵CO2激光联合TXA治疗黄褐斑的研究中,也得到相同的结论。30例女性患者一侧脸进行微针,另一侧脸使用点阵CO2激光,治疗结束后,两侧脸立即局部涂抹4mg/mlTXA溶液,研究结果发现微针和点阵CO2激光联合TXA治疗面部黄褐斑同样安全有效。
TXA不同给药途径治疗黄褐斑的优势与劣势
局部外用TXA乳膏或溶液治疗黄褐斑的耐受性优于其他局部治疗,患者易于使用,不需借助特殊工具,且治疗成本低。但仅皮肤外用TXA制剂,治疗效果慢,对严重黄褐斑治疗效果不佳。皮内注射TXA治疗黄褐斑,可以将浓缩药物直接运输至皮肤深层,无需全身吸收,起效快,恢复时间短。但是皮内注射的表面积毕竟有限,且该疗法考验医生的手法及熟练程度。
微针联合TXA治疗黄褐斑可以将药物均匀分布到真皮层深处,可增加药物的渗透量,使药物渗透的剂量达到未经操作皮肤剂量的1.2倍,且可维持至少48h,另外微针可引起经皮胶原感应,新生胶原蛋白,使创面有氧愈合,增生真皮层弹力纤维,维持皮肤组织弹性,达到换肤的效果。但是微针治疗需要特殊的仪器,且治疗成本增加。
激光联合TXA治疗黄褐斑不但可以通过激光的能量选择性地碎裂皮肤中的黑素颗粒治疗黄褐斑,同时还可以增加TXA的吸收,增加治疗效果。但激光治疗存在诱发炎症和刺激黑色素生成的风险,且治疗成本高昂,给患者带来巨大的经济压力。不同的治疗方式其优劣势各不相同,对不同的患者来说,也应根据黄褐斑的严重程度、自身的耐受程度及经济情况而设立个性化的治疗方案。
局部外用氨甲环酸治疗黄褐斑的安全性与不良反应
众所周知,口服TXA治疗黄褐斑的效果是确切的。尽管口服的剂量仅为常规用量的1/6,但不良反应仍然很多。常见的不良反应包括轻度胃肠道不适、月经减少、过敏性皮疹、脱发和谷丙转氨酶水平轻度升高等,严重不良反应还包括血栓栓塞风险,这些不良反应也在一定程度上限制了它的应用,而局部外用TXA在一定程度上可以大大减少此类不良反应的发生。
当然,外用TXA仍然会出现一些不良反应,轻微不良反应包括注射部位疼痛、瘙痒、烧灼感和红斑等,一般在24h后就会消退。严重不良反应包括皮内注射后色素减退、白癜风样斑疹,也有文献报道皮内注射TXA后出现视觉异常、低血压、恶心和呕吐。
小结
TXA对黄褐斑具有显著治疗效果。与口服TXA相比,局部外敷、病灶皮内注射,以及联合微针激光治疗可最大程度地减少全身副作用。
本研究的局限在于不够全面,也不是对最近的随机对照试验进行优先排序,且大多数研究没有设置阳性和阴性对照组,未来仍需要大规模的随机对照研究和长期随访研究,并将试验方法优化,以便获得更加准确的临床数据。此外,TXA没有标准剂量,每项研究使用不同的剂量和浓度,因此难以比较,需要进一步的随机和空白对照试验来 确定每种方法的长期疗效和安全性。
参考文献:
1.徐凡,龚春燕.局部使用氨甲环酸治疗黄褐斑的研究进展[J].中国美容医学,2024,11(33):189-192.
2.Perper M, Eber A E, Fayne R, et al. Tranexamic acid in the treatment of melasma: a review of the literature[J]. Am J Clin Dermatol, 2017,18(3):373-381.
3.Sheu S L. Treatment of melasma using tranexamic acid: what's known and what's next[J].Cutis, 2018,101(2):E7-E8.
4.Mahjoub T T, Milibary H H. Oral tranexamic acid in the treatment of hyperpigmentation disorder beyond melasma: A review[J]. J Cosmet Dermatol, 2023,22(4):1157-1162.
5.其他文献(略)。


