Nature Aging:肠道微生物如何揭示衰老的秘密?
时间:2025-01-14 12:15:09 热度:37.1℃ 作者:网络
引言
衰老过程复杂而多样,不仅受到遗传因素的深刻影响,也与环境、生活方式以及体内的微观生态密切相关。近年来,研究人员发现,作为“第二基因组”的肠道微生物群,在宿主健康与衰老中扮演着不可或缺的角色。这些微生物群落不仅随着年龄发生动态变化,还通过代谢活动生成大量化学信号,影响宿主的生理状态。然而,肠道微生物如何具体作用于衰老过程,以及这种作用背后的分子机制,依然是未解之谜。
1月10日Nature Aging的研究报道“Gut microbial-derived phenylacetylglutamine accelerates host cellular senescence”发现,一种由肠道微生物生成的代谢物——苯乙酰谷氨酰胺(Phenylacetylglutamine, PAGln),可能是加速宿主细胞衰老的重要因素。PAGln通过对肾上腺素受体(adrenoreceptor, ADR)-AMPK信号通路的影响,触发线粒体功能障碍和DNA损伤,最终导致细胞衰老。这一发现不仅揭示了肠道微生物与宿主衰老之间的直接联系,还为抗衰老疗法的开发提供了新的靶点。
该研究结合人类血浆代谢组学数据和动物实验,系统性地证明了PAGln水平会随年龄显著升高,这种现象主要由老年人肠道微生物的代谢特性引起。同时,实验还表明,通过阻断相关信号通路或采用“清除衰老细胞”(senolytic therapy)的方式,可以有效缓解PAGln引发的细胞衰老。该研究突破性地阐明了肠道微生物与宿主衰老之间的分子联结,为深入理解衰老机制和开发创新的抗衰老策略提供了重要启示。

揭秘衰老:隐藏在肠道微生物中的“时间密码”
衰老的脚步从未停止,但这一过程为何在不同个体中呈现出如此巨大的差异?近年来,研究人员发现,肠道微生物或许掌握着破解这一谜题的“时间密码”。作为人体内一个庞大而复杂的生态系统,肠道微生物在免疫调控、代谢平衡以及细胞功能维持中扮演着至关重要的角色。而随着年龄增长,肠道微生物群落的结构和功能会发生显著改变,这一动态过程被认为深刻影响着个体的生理衰老进程。
研究表明,衰老过程中肠道微生物的多样性显著下降,部分关键菌群比例改变,从而导致代谢产物的种类和水平随之波动。例如,苯乙酰谷氨酰胺(Phenylacetylglutamine, PAGln)这种由微生物生成的代谢物,其水平会随着年龄的增长显著升高。通过对132名22岁至104岁的健康个体进行血浆代谢组学分析,研究人员发现PAGln浓度与年龄呈强正相关(Pearson r = 0.644,P < 0.0001)。这一趋势在独立验证队列和多组学数据中也得到了进一步确认,表明PAGln可能是肠道微生物与宿主衰老之间的重要分子纽带。
然而,PAGln究竟是如何影响衰老的?研究人员提出,它可能通过促进线粒体功能障碍、加重DNA损伤,最终触发细胞衰老这一过程。这种细胞水平的改变不仅累积为器官功能的退化,更加速了整个生理系统的老化。由此,研究人员开始追问:是否存在能够调控PAGln生成的微生物群,进而影响个体的衰老轨迹?解答这些问题的关键,不仅能够帮助我们理解衰老的生物学机制,更可能为人类健康老龄化的实现带来革命性启示。
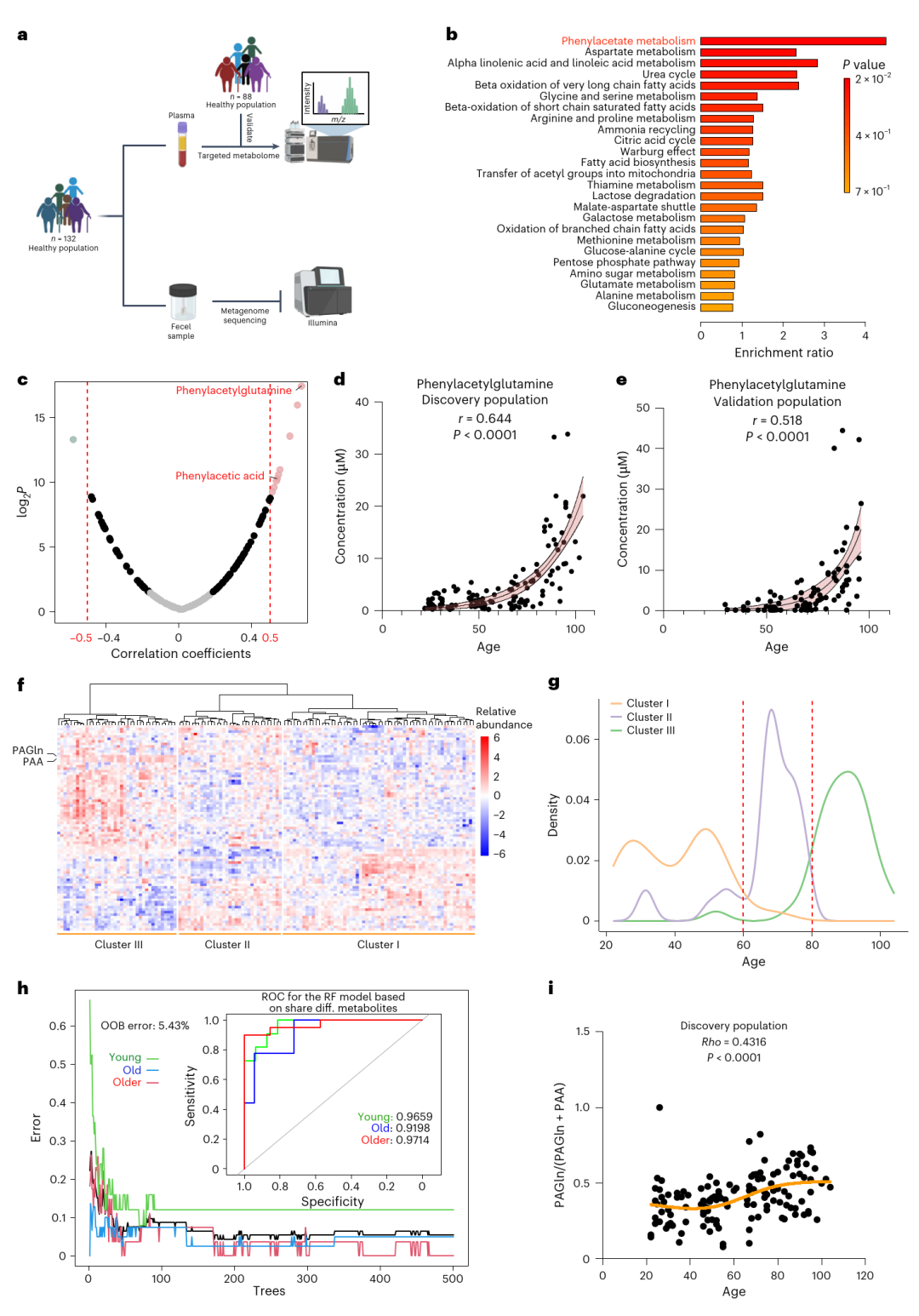
肠道微生物与宿主共代谢物PAGln与年龄的关联(Credit: Nature Aging)
a. 样本采集与分析
研究人员从132名健康个体的血浆和粪便样本中,分别进行了血浆靶向代谢组分析和粪便宏基因组测序。同时,还在一个包含80名健康个体的独立验证队列中,对血浆样本进行了靶向代谢组分析。
b. 年龄相关代谢物的富集分析
通过对血浆代谢物的富集分析,研究发现了与年龄密切相关的代谢物,并重点分析了这些代谢物在不同年龄段的变化趋势。
c. 火山图分析
火山图展示了血浆代谢物与年龄的相关性。灰色点代表无显著相关性(P ≥ 0.05);黑色点表示有弱相关性(P < 0.05 且 |r| < 0.5);红色点则表示有强相关性(P < 0.05 且 |r| > 0.5)。
d, e. PAGln与年龄的相关性
研究通过在发现队列(132名个体)和验证队列(80名个体)中分析PAGln的浓度,发现PAGln与年龄之间存在显著正相关。图中显示了PAGln浓度与年龄的相关性曲线,并给出了Pearson相关系数(r值)。
f. 与年龄相关的血浆代谢物热图
热图展示了83种与年龄相关的血浆代谢物,并通过层次聚类分析将个体进行分组,显示出不同年龄段代谢物的聚集特征。
g. 密度图
密度图展示了不同聚类中各年龄段个体的分布,帮助理解不同代谢物在年龄分布中的变化。
h. 随机森林模型
通过随机森林模型分析,基于18种差异显著的血浆代谢物,研究团队区分了年轻、老年和高龄三个年龄组。图中显示了该模型的ROC曲线,整体准确率达到81.48%。
i. PAGln与年龄的Spearman相关性
PAGln浓度与年龄的Spearman相关系数(Rho值)显示,PAGln在排除苯乙酸(PAA)影响后,仍然与年龄呈强正相关。
肠道微生物代谢物的“黑马”——苯乙酰谷氨酰胺(PAGln)
PAGln是由肠道微生物和宿主共同代谢生成的产物,其前体物质苯乙酸(Phenylacetic acid, PAA)由肠道微生物将膳食来源的L-苯丙氨酸(L-phenylalanine)转化而来。随后,这种苯乙酸进入宿主的肝脏或肾脏,与谷氨酰胺结合形成PAGln。这个过程展现了肠道微生物与宿主器官之间的巧妙协作,揭示了它们如何通过代谢网络共同塑造宿主的生理状态。
有趣的是,PAGln的生成并非恒定不变,而是随着年龄的增长而显著升高。研究人员通过对132名不同年龄个体的血浆代谢组学分析发现,PAGln浓度随着年龄增长呈现出强正相关的趋势(Pearson r = 0.644,P < 0.0001),这一结论在独立验证队列中也得到了确认。为何PAGln水平在老年人中更高?答案隐藏在肠道微生物的动态变化中。随着年龄的增长,肠道中某些特定菌群(如Clostridium scindens)的相对丰度增加,而这些菌群正是PAA生成的关键驱动者。此外,这些菌群的代谢活性显著增强,进一步提升了PAA的生成效率,为PAGln水平的升高奠定了基础。
实验显示,老年人肠道微生物在体外培养时,其将L-苯丙氨酸转化为PAA的能力显著高于年轻人组(P = 0.035)。这一发现表明,PAGln水平的升高并非单纯由年龄引发的生理变化,而是深受肠道微生物代谢特性改变的驱动。
PAGln不仅是肠道微生物代谢的“产物”,更可能是宿主衰老的“信号”。
从分子到细胞:PAGln如何驱动细胞衰老?
细胞衰老是生理衰老的核心事件,而苯乙酰谷氨酰胺(PAGln)在这一过程中展现了惊人的“破坏力”。研究发现,PAGln通过一系列分子和细胞机制,加速了宿主细胞的衰老进程。
线粒体功能的“瘫痪”:细胞能量工厂的失效
线粒体被誉为细胞的能量工厂,其功能紊乱直接威胁细胞活力。实验显示,在不同浓度PAGln处理下,细胞的线粒体膜电位(MMP)显著下降(P < 0.0001),并伴随活性氧(ROS)水平的显著升高。此外,线粒体内融合相关蛋白(MFN1、MFN2)表达减少,而分裂相关蛋白(p-DRP1/DRP1)表达增加,导致线粒体呈现出碎片化状态。这种线粒体功能障碍不仅削弱了细胞的能量供应,还引发了一系列代谢紊乱,为细胞衰老埋下隐患。
DNA损伤的累积:衰老的关键触发点
DNA的完整性是细胞维持正常功能的基石。然而,PAGln显著增加了DNA损伤标志物γ-H2AX的表达(P < 0.0001)。长期PAGln暴露下,细胞周期抑制因子p53、p21和p16的表达逐步上升,而细胞核结构蛋白Lamin B1的表达减少,进一步加剧了细胞周期停滞。这些变化是细胞进入不可逆衰老状态的标志性事件。
肾上腺素受体-AMPK信号通路:衰老的“分子开关”
深入研究揭示了PAGln诱导衰老的关键机制:肾上腺素受体(ADR)-AMPK信号通路的激活。PAGln通过刺激ADR,过度激活下游的AMPK通路,导致线粒体分裂相关蛋白的异常表达和能量代谢紊乱。更重要的是,阻断ADR或抑制AMPK活性(如通过药物Compound C),能够显著缓解PAGln引发的衰老表型,显示出这一通路作为干预靶点的潜力。
从线粒体到DNA,从分子信号到细胞衰老,PAGln通过多维破坏机制,将细胞推向衰老的深渊。
血液中的“年龄标签”:从数据中寻找答案
“数据不会说谎”,血液中的代谢组学数据正成为解码衰老过程的重要“线索”。通过对血浆样本的深入分析,研究人员发现了苯乙酰谷氨酰胺(Phenylacetylglutamine, PAGln)水平与年龄的显著关联,为理解衰老的分子机制提供了关键线索。
在该研究中,研究人员从132名年龄在22至104岁的健康个体中采集了血浆样本,并进行了针对性代谢组学分析。结果显示,PAGln浓度与年龄呈现显著正相关(Pearson r = 0.644,P < 0.0001)。这一趋势不仅在初步研究中显现,还在包含80名健康个体的独立验证队列中得到了完全一致的结果。这表明,PAGln的变化并非偶然,而是随年龄增长的可靠生物标记。此外,研究进一步结合日本多组学参考数据(2,957人)再次验证了PAGln水平的年龄依赖性,数据的普适性令人信服。
研究人员不仅依赖相关性分析,还通过大样本的细致分组和随机森林模型进行深入挖掘。他们将样本按年龄分为“年轻”(22-59岁)、“老年”(60-79岁)和“高龄”(80-104岁)三组,并利用代谢物的差异构建预测模型。结果显示,PAGln是区分不同年龄组的关键代谢物,其对模型预测的准确性贡献巨大(AUC > 0.9)。更有趣的是,即使去除了前体物质苯乙酸(PAA)的干扰,PAGln仍然显现出独立的强正相关,提示其不仅受肠道微生物的影响,还可能受到宿主生理机制的调控。
PAGln的衰老效应
PAGln与细胞衰老的关系,通过细胞模型和动物实验得到了强有力的验证。这些实验不仅揭示了PAGln如何诱导衰老,还让我们看到了其在组织层面的深远影响。
细胞模型中的证据:PAGln的“催老”表型
研究人员以人脐静脉内皮细胞(HUVECs)和胎肺成纤维细胞(IMR-90)为模型,探讨了不同浓度PAGln的长期作用。结果显示,PAGln以剂量依赖的方式抑制了细胞增殖,并导致不可逆的细胞周期停滞。这种衰老表型通过染色检测进一步证实,PAGln处理组的β-半乳糖苷酶(SA-β-gal)阳性细胞比例显著增加(P < 0.0001)。此外,DNA损伤标志物γ-H2AX、细胞周期抑制因子p16和p21的表达水平显著升高,而细胞核结构蛋白Lamin B1的表达则显著下降。所有这些变化共同指向一个明确的结论:PAGln直接诱导了细胞进入衰老状态。
动物实验的突破:PAGln对组织功能的破坏
为了验证PAGln的促衰老效应是否在体内存在,研究团队将PAGln每天腹腔注射至8周龄的健康小鼠,持续4周。结果显示,处理组小鼠的肾脏和肺组织中衰老相关蛋白(如p53、p16和p21)的表达水平显著升高,SASP(衰老相关分泌表型)标志基因的表达也出现大幅上调。更细致的单细胞RNA测序进一步揭示了特定细胞类型(如内皮细胞和巨噬细胞)对PAGln的敏感性,这些细胞表现出较高的p21和SASP表达比例。这表明,PAGln不仅影响个体细胞,还能通过局部组织内的细胞间通信加剧衰老的系统性效应。
与肠道微生物共舞:谁在掌控PAGln的生成?
肠道微生物被誉为人体的“隐形器官”,在代谢调控和宿主健康中扮演着重要角色。而PAGln的生成,更是深深地嵌套在微生物群落的复杂网络中。
不同年龄段肠道微生物的特征变化
随着年龄增长,肠道微生物的多样性显著下降,特定菌群的比例发生重组。在该研究中,研究人员利用线性判别分析效应大小(LEfSe)算法,发现了26种特异性微生物种类和27条代谢通路在年轻组(22-59岁)、老年组(60-79岁)和高龄组(80-104岁)之间存在显著差异。比如,与PAGln生成相关的苯丙氨酸代谢途径在老年和高龄组中显著富集,而年轻组的肠道代谢活性则更倾向于维持能量代谢平衡。
PAGln生成的“幕后推手”
进一步的分析揭示,某些微生物种类在PAGln生成中起到了关键作用。例如,Clostridium scindens和Gordonibacter pamelaeae在高龄个体的肠道中占比显著增加。这些菌群通过高效表达苯丙氨酸代谢相关的关键酶(如VOR和PPDC),显著提升了苯乙酸(PAA)的生成效率,进而为PAGln的积累奠定了基础。在体外实验中,高龄组肠道微生物的PAA生成能力显著高于年轻组(P = 0.035)。此外,单菌培养实验进一步确认,C. scindens和G. pamelaeae能够在厌氧条件下将L-苯丙氨酸转化为PAA,展现了强大的代谢潜力。
这些发现为我们揭示了一个清晰的画面:PAGln水平的升高并非偶然,而是由特定肠道微生物种群的代谢活性驱动的结果。
抗击PAGln的可能策略
随着对Phenylacetylglutamine, PAGln在衰老过程中的作用机制的逐步揭示,研究人员正在探索基于PAGln的抗衰老干预策略。这些方法旨在从分子信号通路和细胞层面入手,通过阻断PAGln的有害作用或直接消除受其影响的衰老细胞,为健康老龄化开辟新道路。
阻断PAGln信号通路:精准靶向的抗衰老潜力
PAGln通过激活肾上腺素受体(ADR)-AMPK信号通路,导致线粒体功能紊乱和细胞衰老,这为干预提供了明确的靶点。研究表明,使用肾上腺素受体拮抗剂(如普萘洛尔,Propranolol)或AMPK抑制剂(如Compound C)能够有效缓解PAGln引发的细胞衰老表型。这些药物干预不仅减少了活性氧(ROS)的积累,还显著改善了线粒体膜电位和能量代谢紊乱。此外,特异性调控PAGln生成的微生物代谢途径,例如通过调整肠道菌群的比例或使用靶向抑制剂,也可能成为控制PAGln水平的有效方法。这种基于代谢调控的抗衰老疗法,不仅具备良好的可行性,还能够进一步降低衰老相关疾病的风险。
清除衰老细胞:从根本上逆转衰老效应
PAGln诱导的细胞衰老以不可逆的细胞周期停滞和衰老相关分泌表型(SASP)为特征,而这些衰老细胞往往会进一步加剧组织功能的退化。因此,清除衰老细胞的“衰老清除疗法”(Senolytic Therapy)成为一种备受关注的手段。例如,利用靶向药物(如Navitoclax)能够高效消除表达p16和p21的衰老细胞,显著改善PAGln处理后的组织功能。此外,基因编辑技术如CRISPR/Cas9也显示出在清除特定衰老细胞群体中的潜力,为个性化治疗方案提供了可能。
未来,调控肠道微生物群或将成为健康管理的重要手段之一。随着技术的进步,我们有望通过微生物组测序和代谢组学,实时监测个体的肠道微生物状态和代谢产物水平。借助益生菌、饮食调整或新型微生物疗法,精准调控肠道微生物组成,进而影响PAGln等关键代谢产物的生成,或将成为实现健康老龄化的有力工具。
参考文献
Yang H, Wang T, Qian C, Wang H, Yu D, Shi M, Fu M, Liu X, Pan M, Rong X, Xiao Z, Chen X, Yeerken A, Wu Y, Zheng Y, Yang H, Zhang M, Liu T, Qiao P, Qu Y, Lin Y, Huang Y, Jin J, Liu N, Wen Y, Sun N, Zhao C. Gut microbial-derived phenylacetylglutamine accelerates host cellular senescence. Nat Aging. 2025 Jan 10. doi: 10.1038/s43587-024-00795-w. Epub ahead of print. PMID: 39794469.


