Nature Methods:Paired-Damage-seq:同步解析DNA损伤与基因表达
时间:2025-03-29 12:12:26 热度:37.1℃ 作者:网络
引言
生命体的正常运转离不开健康的基因组(genome)。基因组就像我们身体的“蓝图”,指导着细胞的生长、发育和功能。然而,随着时间的推移,各种内源性(endogenous)和环境因素(environmental factors)都会对我们的基因组造成威胁,导致DNA损伤(DNA damage)。想象一下,这份精密的“蓝图”上出现了各种各样的“划痕”和“断裂”,这无疑会对细胞的正常功能造成影响,甚至可能导致疾病的发生。
长期以来,研究人员一直在努力理解DNA损伤是如何发生的,以及它会对我们的健康产生什么样的影响。然而,由于我们身体内存在着各种各样的细胞类型,而且DNA损伤的发生又具有一定的随机性(stochasticity),想要在复杂的细胞环境中精确地分析DNA损伤及其后果一直是一个巨大的挑战。
3月24日一项发表在《Nature Methods》杂志上的创新研究“Single-cell parallel analysis of DNA damage and transcriptome reveals selective genome vulnerability”,为我们揭开了细胞基因组脆弱性的神秘面纱。研究人员开发了一种名为Paired-Damage-seq的全新技术,能够以前所未有的精度在单个细胞(single cell)水平上同时分析氧化损伤(oxidative damage)和单链DNA损伤(single-stranded DNA damage),并结合分析基因的表达情况(gene expression)。这项突破性的技术,就像给我们的细胞装上了“显微镜”和“录音机”,让我们能够清晰地看到DNA损伤发生的位置,并同时听到细胞内部基因的“声音”。
为了验证这项技术的强大之处,研究人员首先将其应用在了实验室培养的人类宫颈癌细胞系(HeLa cells)中,随后又将其应用在了小鼠的大脑(mouse brain)中。通过对这些不同类型的细胞进行深入分析,他们获得了许多令人兴奋的发现,这些发现不仅帮助我们更好地理解了DNA损伤的发生规律,也为我们揭示了细胞类型特异性的基因组脆弱性(selective genome vulnerability)。

创新技术:单细胞如何同时追踪DNA损伤和基因表达?
想要理解DNA损伤对细胞的影响,仅仅知道损伤发生了是不够的,更重要的是要了解损伤发生在基因组的哪个位置,以及它是否会影响到附近基因的表达。传统的DNA损伤分析方法往往是对大量细胞的平均结果进行分析,这就好比我们想要了解一个城市里不同区域的交通状况,却只拿到了整个城市的平均交通流量数据,而忽略了不同区域之间的差异。
Paired-Damage-seq技术的出现,彻底改变了这一局面。这项技术的巧妙之处在于,它能够在单个细胞内同时捕获并分析两种主要的DNA损伤类型——氧化损伤和单链DNA损伤,并且能够同步测量该细胞中所有基因的表达水平。这就像我们给每一个细胞都配备了一个精密的“定位系统”和“信息记录仪”,可以精确地记录下DNA损伤发生的具体位置,以及当时细胞正在“忙碌”地表达哪些基因。
具体来说,Paired-Damage-seq技术利用了化学标记的方法来特异性地标记DNA上的氧化损伤和单链断裂位点。随后,研究人员对单个细胞的基因组进行测序(sequencing),通过分析测序数据中标记的位置,他们就能够精确地定位出DNA损伤在基因组上的分布。与此同时,他们还对同一个细胞中的RNA分子进行了测序,从而获得了该细胞的基因表达谱(transcriptome)。通过将DNA损伤数据和基因表达数据进行整合分析,研究人员就能够揭示DNA损伤与基因表达之间的复杂关系。
这项技术的成功开发和应用,为我们研究DNA损伤的细胞类型特异性(cell-type-specific)和基因组区域特异性(genomic region-specific)打开了全新的大门。
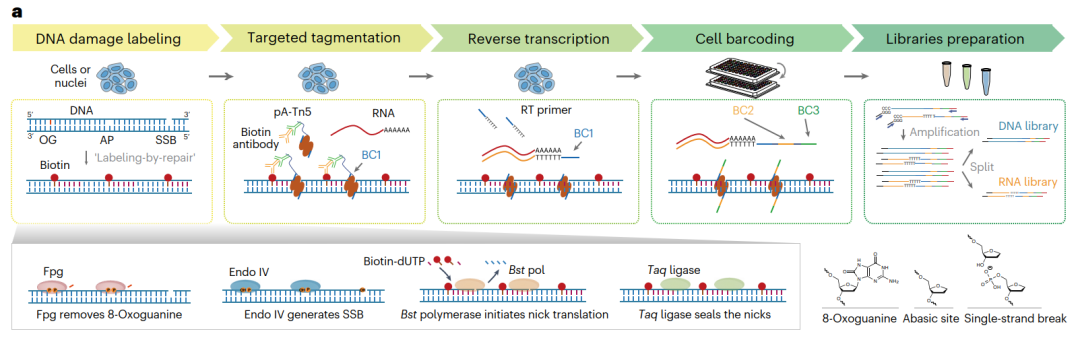
Paired-Damage-seq流程图(Credit: Nature Methods)
惊人发现:不同细胞类型拥有独特的DNA损伤“偏好”
研究人员利用Paired-Damage-seq技术,对人类宫颈癌细胞系(HeLa cells)和小鼠大脑中的多种细胞类型进行了深入分析。他们惊奇地发现,不同类型的细胞,其DNA损伤的热点区域(damage hotspots)竟然呈现出截然不同的模式。这就像我们身体的不同器官,虽然都由细胞构成,但它们的功能和特性却各不相同。这项研究表明,即使是DNA损伤,在不同的细胞类型中,也似乎有着自己独特的“偏好”。
例如,在小鼠大脑中,研究人员发现兴奋性神经元(excitatory neurons)相比于抑制性神经元(inhibitory neurons),更容易积累较高水平的氧化损伤。这提示我们,不同功能的神经元可能由于其代谢活动或其他特性的差异,而对DNA损伤的敏感性不同。这种细胞类型特异性的DNA损伤分布,暗示了某些细胞可能天生就更容易受到特定类型基因组损伤的侵袭。
更令人兴奋的是,研究人员发现,通过分析细胞中DNA损伤的热点区域的分布模式,竟然可以预测细胞的类型!这就像我们通过分析一个城市的犯罪热点区域分布图,可以初步判断出该区域的社会经济特征。这项发现表明,DNA损伤的分布模式很可能蕴含着关于细胞身份和功能的重要信息。
氧化损伤与单链断裂:基因组面临的双重“危机”
Paired-Damage-seq技术能够同时检测两种主要的DNA损伤类型:氧化损伤和单链DNA断裂。氧化损伤通常是由于细胞代谢过程中产生的活性氧(reactive oxygen species, ROS)攻击DNA分子造成的。而单链DNA断裂则可能是由于多种因素引起的,例如DNA复制错误、环境中的有害物质等。
研究人员通过Paired-Damage-seq技术发现,这两种不同类型的DNA损伤在基因组上的分布模式并不完全相同。某些基因组区域可能更容易受到氧化损伤的侵袭,而另一些区域则可能更容易发生单链断裂。这提示我们,我们的基因组在面对不同的损伤来源时,其脆弱性是不同的。
更重要的是,研究人员发现,氧化损伤的热点区域往往与基因组上一些特定的功能元件(functional elements)相关联,例如活跃的基因转录起始位点(transcription start sites, TSSs)。这意味着,DNA损伤的发生可能并非完全随机,而是受到基因组自身结构和功能状态的影响。例如,那些正在积极表达的基因区域,可能由于其开放的染色质结构(chromatin structure),更容易受到氧化损伤的攻击。
表观遗传的“秘密”:DNA损伤如何影响基因的开关?
我们的基因组并非一成不变的“死”的序列,而是受到复杂的表观遗传修饰(epigenetic modifications)的调控。这些修饰就像基因的“开关”和“调光器”,决定着哪些基因在何时、以何种强度表达。研究人员利用Paired-Damage-seq技术,深入探索了DNA损伤与表观遗传修饰之间的关系。
他们发现,DNA损伤的发生与某些特定的表观遗传标记(epigenetic marks)之间存在着显著的关联。例如,他们观察到,在某些细胞类型中,DNA损伤的热点区域往往与一些与基因激活相关的表观遗传标记(如H3K27ac)重叠。这暗示着活跃的基因区域可能更容易受到DNA损伤,而这种损伤反过来也可能进一步影响这些基因的表达。
此外,研究人员还发现,在衰老的小鼠大脑中,某些细胞类型中DNA损伤的积累与一些抑制性的表观遗传标记(如H3K9me3)的改变有关。这提示我们,随着年龄的增长,DNA损伤的模式可能会发生变化,而这种变化可能与表观遗传调控的紊乱有关,进而影响细胞的功能。
这些发现表明,DNA损伤和表观遗传修饰之间存在着复杂的相互作用。DNA损伤的发生可能会影响基因的表达调控,而表观遗传状态也可能会影响DNA损伤的易感性。理解这种相互作用,对于我们深入认识衰老和疾病的发生机制至关重要。
“基因组脆弱性”的意义:它与疾病的发生有何关联?
这项研究最重要的发现之一,就是揭示了细胞类型特异性的基因组脆弱性。这意味着,我们身体中不同的细胞类型,由于其自身的特性,对DNA损伤的易感性是不同的,而且DNA损伤在它们基因组上的分布模式也是独特的。
那么,这种细胞类型特异性的基因组脆弱性对于我们的健康又意味着什么呢?研究人员通过进一步的分析发现,那些在特定细胞类型中容易发生DNA损伤的基因组区域,往往与某些疾病的发生风险相关联。他们利用全基因组关联研究(genome-wide association studies, GWAS)的数据进行分析,发现某些疾病的遗传风险位点(genetic risk loci)与特定细胞类型中的DNA损伤热点区域存在显著的重叠。
例如,他们发现,在小胶质细胞(microglia cells)中特异性发生的DNA损伤,与一些神经退行性疾病(neurodegenerative diseases)的风险基因存在关联。小胶质细胞是大脑中的免疫细胞,它们在维持大脑健康中发挥着重要的作用。这项发现提示,小胶质细胞基因组的特定区域可能更容易受到损伤,而这种损伤的积累可能会导致其功能障碍,最终增加患神经退行性疾病的风险。
这些发现表明,细胞类型特异性的基因组脆弱性可能在疾病的发生和发展中扮演着重要的角色。了解哪些细胞类型在哪些基因组区域更容易受到损伤,将有助于我们更好地理解疾病的发生机制,并为开发更精准的疾病预防和治疗策略提供新的思路。
这项研究将如何改变我们对健康的理解?
这项开创性的研究,通过开发和应用Paired-Damage-seq技术,为我们深入理解DNA损伤的细胞类型特异性和基因组脆弱性提供了强大的工具。它不仅揭示了不同细胞类型拥有独特的DNA损伤分布模式,还阐明了DNA损伤与表观遗传修饰之间的复杂关系,并初步揭示了基因组脆弱性与疾病发生之间的潜在联系。
这项研究的意义是深远的。首先,它为我们提供了一个全新的视角来审视基因组的完整性。我们现在知道,基因组的某些区域在特定的细胞类型中可能天生就更加脆弱,更容易受到损伤。这提醒我们,在研究疾病的发生机制时,需要更加关注不同细胞类型的特性。
其次,这项技术为我们研究衰老过程中的基因组变化提供了新的手段。随着年龄的增长,我们的细胞会积累更多的DNA损伤。利用Paired-Damage-seq技术,我们可以更精确地追踪这些损伤在不同细胞类型中的分布和变化,从而更好地理解衰老的分子机制。
最后,这项研究为开发新的疾病诊断和治疗方法带来了希望。通过深入了解与特定疾病相关的细胞类型中的基因组脆弱性,我们可以开发出更具针对性的干预措施,例如,针对性地保护易受损伤的基因组区域,或者修复已经发生的DNA损伤。
当然,这项研究也仅仅是一个开始。未来,研究人员还将利用Paired-Damage-seq技术对更多不同类型的细胞和组织进行研究,以更全面地了解基因组脆弱性的规律。同时,还需要进一步探索DNA损伤与各种疾病之间的具体联系,以及如何利用这些知识来改善人类健康。
总而言之,这项研究为我们揭示了细胞基因组的“脆弱点”,也为我们理解生命体的基本运作规律和疾病的发生机制打开了新的窗口。随着研究的不断深入,我们有理由相信,在不久的将来,我们将能够更好地保护我们的基因组,远离疾病的困扰,拥有更健康、更长寿的人生。
参考文献
Bai D, Cao Z, Attada N, Song J, Zhu C. Single-cell parallel analysis of DNA damage and transcriptome reveals selective genome vulnerability. Nat Methods. 2025 Mar 24. doi: 10.1038/s41592-025-02632-3. Epub ahead of print. PMID: 40128288.

