Science Advances 浙江大学韩佩东团队发现心肌细胞张力驱动心脏发育的新机制
时间:2025-03-10 12:08:27 热度:37.1℃ 作者:网络
心脏的“雕刻”之谜:从单层心肌到复杂结构的转变
心脏是哺乳动物胚胎发育过程中最早形成的器官。心脏发育初期仅由单层心肌细胞构成,当心脏的房室结构初步建立以后,心室中部分心肌细胞会增殖并向室腔方向迁移,从而形成心肌小梁,而其余的细胞则驻留并形成心室外壁。心肌小梁的发育具有重要的生理意义,其增强了心脏的泵血功能,从而满足机体发育过程中递增的血液和氧气需求。心肌小梁的发育缺陷可导致包括扩张型心肌病在内的多种严重心脏疾病。因此,解析这一发育过程的机制具有重要的科学意义和社会价值。韩佩东团队之前发表的工作(Nature 2016),阐明了心肌细胞Notch信号介导的侧抑制(Lateral inhibition)机制调控了心肌细胞在心肌小梁和心室外壁分布的比例。然而一个悬而未决的问题是:为什么部分心肌细胞会发生定向迁移,驱动这些细胞运动的最初信号是什么?
2025年3月7日,浙江大学韩佩东研究团队在Science Advances上发表了题为“Genetically encoded tension heterogeneity sculpts cardiac trabeculation”的文章。该研究发现Erbb2在单层的心肌细胞中呈现出了异质性的表达,其通过激活PI3K-Arp2/3重构肌动蛋白网络,进而在心肌细胞产生了顶端和基底张力的差异性,驱动心肌细胞发生定向迁移形成心肌小梁,这一发现阐明了控制心肌细胞空间分布的基本规则。

心肌细胞定向迁移的起始
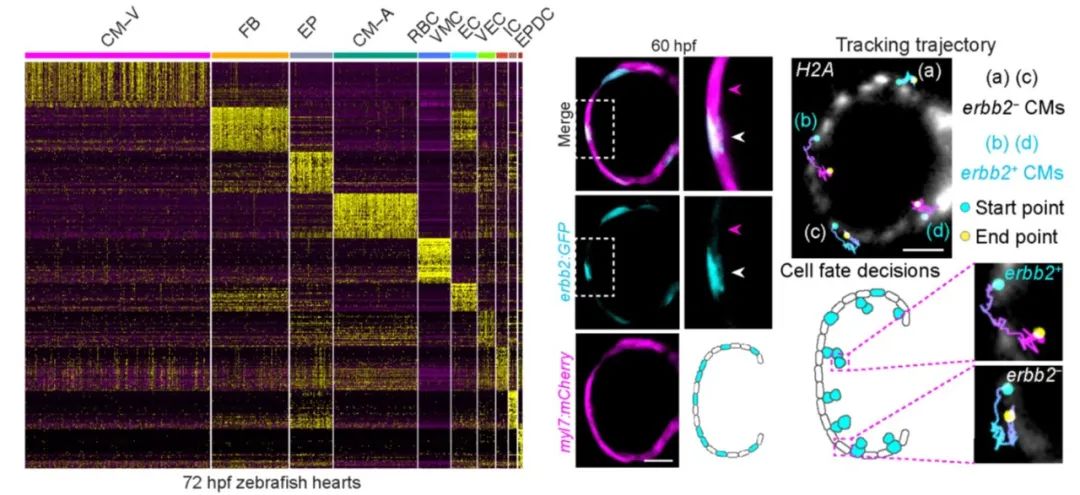
团队成员通过对斑马鱼胚胎心脏进行单细胞转录组测序分析,发现单层的心肌细胞存在显著的异质性。而有意思的是,不同心肌细胞中Erbb2的表达水平存在显著性差异。Erbb2是驱动心肌小梁形成的一个关键性基因,该基因缺失在斑马鱼和小鼠中都可以导致心肌小梁形成的缺陷。但是由于该基因表达丰度很低,目前并不清楚其在空间和时间上表达的动态过程。研究团队通过构建Erbb2:GFP基因敲入斑马鱼,发现Erbb2的表达呈现出明显的空间异质性。通过单细胞谱系示踪,发现Erbb2的表达与心肌细胞的定向迁移直接相关,其中Erbb2表达水平较高的细胞发生定向迁移形成心肌小梁,而Erbb2表达水平较低的细胞则留驻在原位并最终发育成心室外壁。通过运用高速光片显微技术与心跳同步模块分析,实现了跳动心脏的高分辨率长时程成像,直接观察到了Erbb2表达水平较高的心肌细胞的迁移过程。结合心肌细胞特异性Erbb2的抑制或激活等细胞生物学手段,证实心脏发育过程中Erbb2的异质性表达驱动了心肌细胞定向迁移。
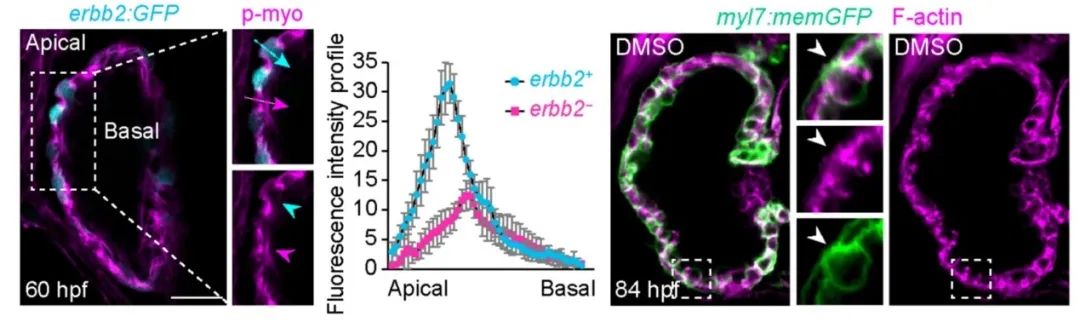
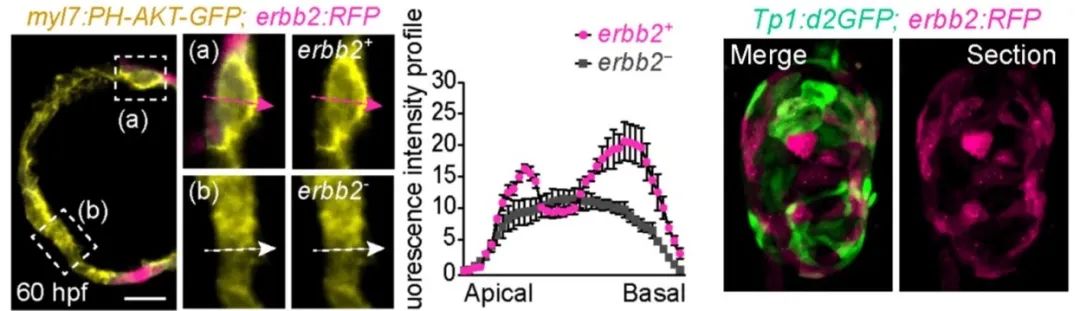
进一步研究发现,Erbb2高表达的细胞具有更高的张力水平,而抑制Erbb2则降低了心肌细胞张力。运用遗传学和分子生物学相关策略,团队成员对心肌细胞进行了张力操控和单克隆分析。结果显示,提升张力可以拯救Erbb2功能缺失对心肌细胞定向迁移,表明Erbb2通过驱动细胞张力水平,诱导心肌细胞发生定向迁移形成小梁。Erbb2属于受体酪氨酸激酶家族成员,PI3K是其下游的主要信号中枢。研究人员构建了PI3K活性荧光探针转基因斑马鱼,首次在心脏中可视化PI3K信号的空间动态。发现PI3K荧光探针在Erbb2阳性细胞中富集于细胞膜。而这种局部的PI3K活性,进一步激活了Arp2/3复合物这一调控肌动蛋白网络的核心分子机器。通过构建Arp2/3荧光融合蛋白动物模型,实时观测到了Arp2/3蛋白复合体在心肌细胞中的极性分布。综上,Erbb2通过激活PI3K信号通路,招募Arp2/3复合物重构肌动蛋白网络,进而提升张力促使心肌细胞发生定向迁移形成小梁。
有趣的是,新形成的小梁通过激活相邻细胞的Notch信号,反向抑制了其邻近细胞的Erbb2表达,形成了Notch和Erbb2空间上互斥的表达特征。Notch抑制心室外壁Erbb2后降低心肌细胞张力以维持心室外壁的稳定性。这种“此消彼长”的反馈机制,如同精密的空间规划系统,确保心肌细胞的空间分布比例,避免过度迁移导致的心肌小梁结构紊乱。总之,本研究首次解析了Erbb2-PI3K张力轴与Notch信号的协同机制,阐明了心肌细胞空间分布的基本规则,为扩张型心肌病或心肌致密化不全等先天性心脏病的早期诊断和治疗提供了新的靶点和策略。
浙江大学韩佩东研究员为本文最后通讯作者。中国科学院脑科学与智能技术卓越创新中心李佳副研究员为共同通讯作者。浙江大学助理研究员梁金秀为第一作者。该研究获得了北京大学未来技术学院何爱彬教授、熊敬维教授、浙江大学徐鹏飞教授的大力支持,浙江大学马骏教授对论文写作提供了宝贵的建议。该工作获得国家重点研发计划、国家自然科学基金项目资助。韩佩东研究员长期关注心肌细胞结构重塑在心脏发育和疾病中的作用机制。近年来以通讯作者发表研究工作:Science Advances 2025、Circulation Research 2025、Circulation 2024、Elife 2024、J Mol Cell Cardiol 2024等。
原文链接:
https://www.science.org/doi/10.1126/sciadv.ads2998


