J Clin Invest 山东大学齐鲁医院钟明/王昊教授团队揭示TRIB3调控血管钙化的新机制
时间:2025-02-27 12:26:17 热度:37.1℃ 作者:网络
慢性肾脏病(CKD)相关血管钙化是终末期肾病患者的常见并发症,其发病率随肾功能恶化显著升高。流行病学数据显示,约30-50%的CKD 3-5期患者存在血管钙化,而透析患者中这一比例可达60-80%。钙化好发于冠状动脉、主动脉及外周动脉,显著增加心血管事件风险。研究证实,血管钙化患者的心肌梗死、心力衰竭及外周动脉疾病风险较普通人群升高3-5倍,心血管死亡率提升2-3倍,是CKD患者死亡的首要原因。寻找CKD血管钙化的深层分子机制有助于开发对应的靶向治疗策略。
2025年2月11日,山东大学齐鲁医院心内科钟明教授与重症医学科王昊教授团队在Journal of Clinical Investigation杂志发表了题为“TRIB3 mediates vascular calcification through facilitating self-ubiquitination and dissociation of Smurf1 in chronic renal disease”的论文。该研究系统阐明了TRIB3-Smurf1调控轴在血管钙化中的分子机制,为CKD血管并发症的靶向治疗提供了新策略。

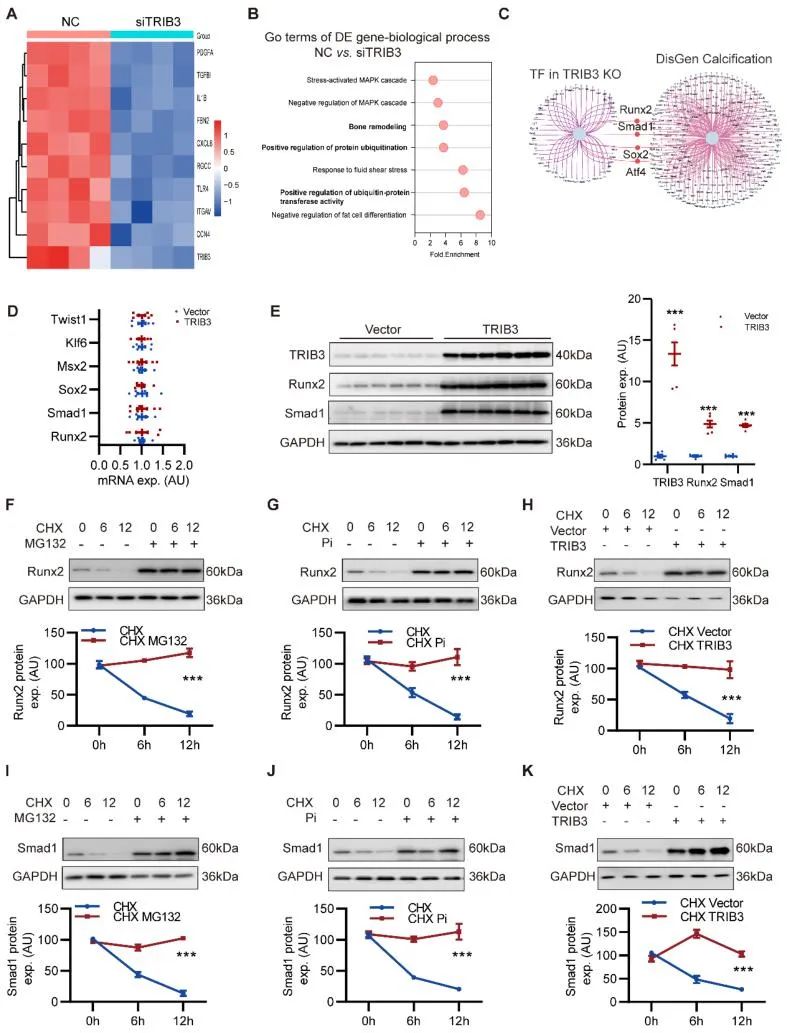
首先,课题组通过分析人及小鼠原代平滑肌细胞转录组数据发现,CKD患者及疾病动物模型的钙化血管组织中TRIB3表达显著上调,且其表达水平与内质网应激标志物呈正相关性,提示TRIB3可能通过调控内质网应激参与CKD血管钙化的病理进程。转录因子结合特征解析表明,TRIB3可调控成骨分化关键转录因子Runx2和Smad1的靶基因表达。值得注意的是,TRIB3过表达实验显示其仅能提升Runx2和Smad1蛋白水平,而不影响其mRNA表达,表明该调控发生于转录后阶段。进一步通过蛋白半衰期检测证实,钙化微环境及TRIB3过表达均可显著延长Runx2和Smad1蛋白的稳定性。
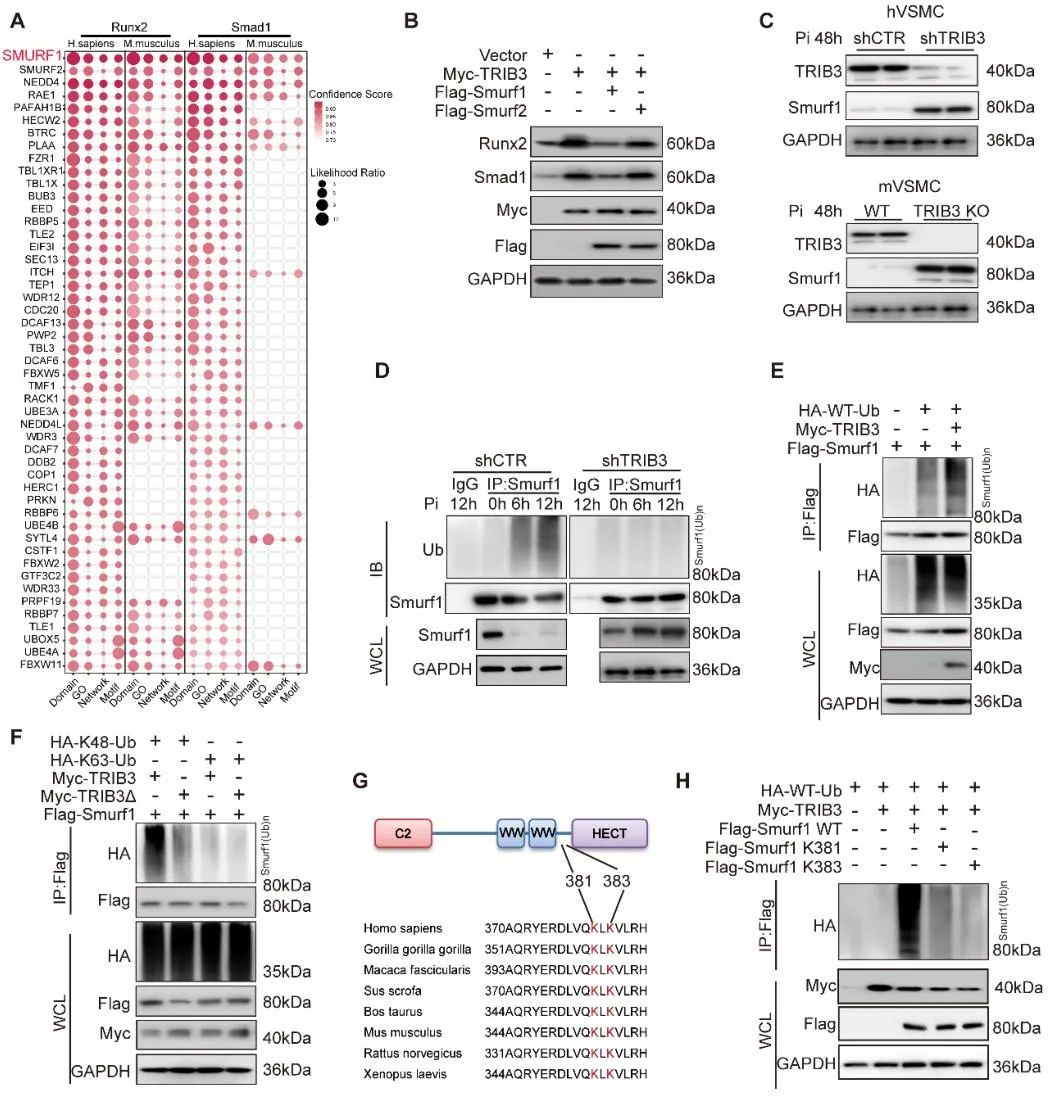
机制研究揭示,生物信息学预测结合实验验证发现Smurf1作为Runx2/Smad1共有的E3泛素连接酶,可通过K48位泛素链特异性介导自身K381和K383位点的自我泛素化。利用分子对接、分子动力学模拟、免疫共沉淀(Co-IP)及表面等离子共振(SPR)等技术,研究团队证实TRIB3通过结合Smurf1的C2结构域,促进其自我泛素化进程并改变其亚细胞定位,进而稳定钙化转录因子Runx2和Smad1。针对钙化微环境诱导TRIB3表达的上游机制,研究者运用染色质免疫沉淀测序(ChIP-seq)、双荧光素酶报告系统及FAIRE-ChIP技术,精准定位内质网应激关键转录因子ATF4与CHOP在TRIB3启动子区的结合位点。
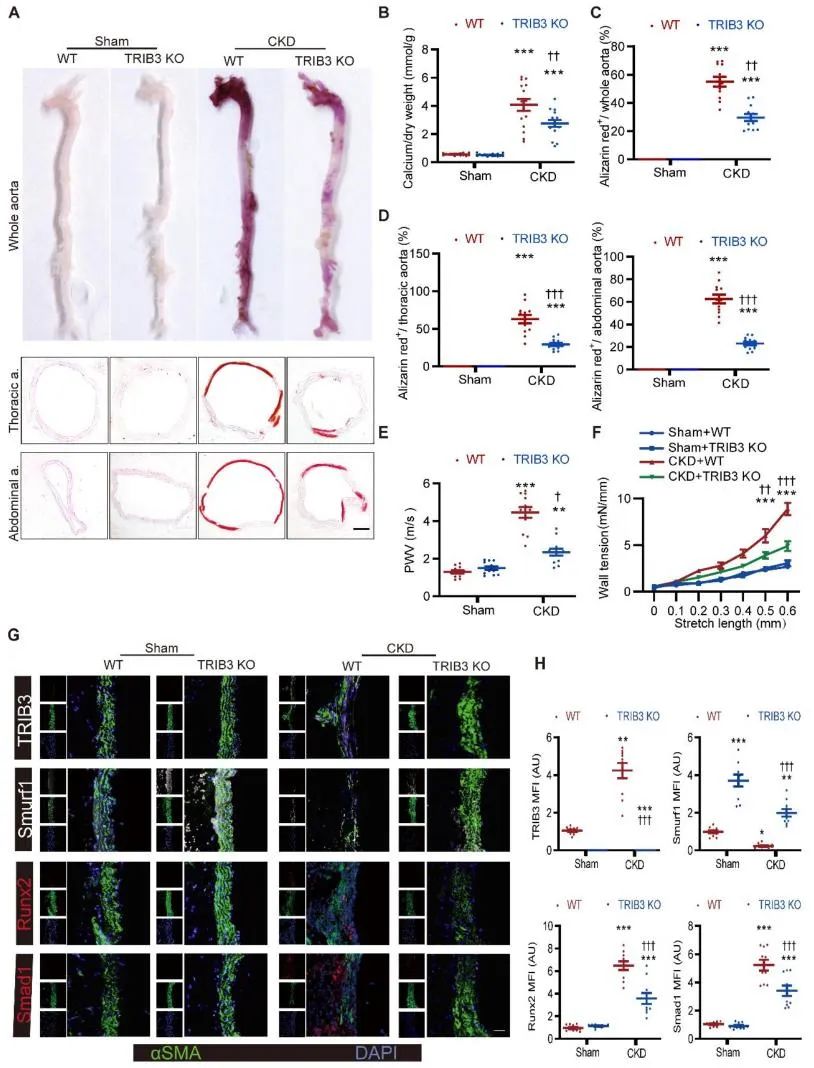
最后,体内实验表明,全身性及组织特异性TRIB3基因敲除小鼠模型均表现出对多种CKD相关血管钙化表型的显著缓解。
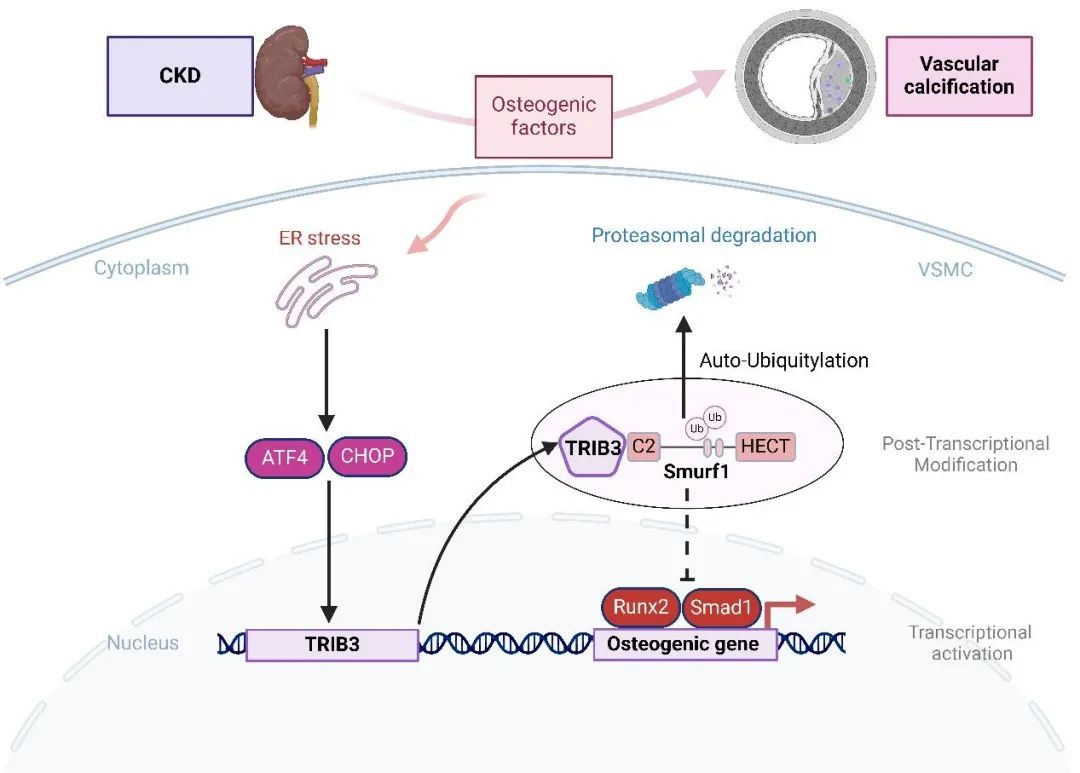
既往研究发现内质网应激促进血管钙化,但对于复杂的内质网应激病理因素如何调控血管平滑肌细胞成骨分化的机制仍缺乏了解。本研究首次发现内质网应激蛋白TRIB3调控CKD血管钙化的重要作用及分子机制,系统性地解释了TRIB3对钙化转录因子独特的转录后调节机制。这一发现拓宽了内质网应激在血管钙化中作用的理解,同时为血管钙化等CKD心血管并发症的防筛诊治康提供了新的思路和靶点。
山东大学齐鲁医院心内科钟明教授与重症医学科王昊教授为该文的通讯作者,山东大学齐鲁医院重症医学科李毅辉副研究员与心内科博士研究生马畅为该文的第一作者,山东大学齐鲁医院为该文的第一和通讯作者单位。该工作得到山东大学齐鲁医院器官移植科孙怀斌主任医师、络病理论创新转化全国重点实验室黄山英主管技师的大力支持。研究得到了国家自然科学基金、山东省自然科学基金、山东省重点研发项目、泰山学者工程以及山东大学临床项目的资助。
文章链接:
https://pubmed.ncbi.nlm.nih.gov/39932798/


