《Cell》重磅: 阿尔茨海默病有望在发病前30年被高效诊断
时间:2025-02-25 12:10:15 热度:37.1℃ 作者:网络
常染色体显性阿尔茨海默病(ADAD)约占所有AD病例的1%。ADAD的特点是在APP、PSEN1或PSEN2基因存在常染色体显性突变。这种罕见形式的AD有助于阐明其关键病理机制和大脑变化的时间进展。ADAD通常比散发形式的AD (sAD)表现得更早,症状发作通常在30-50岁。
近日,顶刊cell杂志上发表了一篇题为“CSF proteomics identifies early changes in autosomal dominant Alzheimer’s disease”的文章,且在杂志Signal Transduction and Targeted Therapy上发表了相应的评论性文章。通过研究ADAD已知突变携带者的脑脊液(CSF)蛋白质组的变化,作者鉴定出了新的早期生物标志物。并基于下面6种选定蛋白的变化,建立了疾病发生和进展的预测模型:SMOC1、SMOC2、NPTX、PEA15、GFAP和TNFRSF1B。这种改变在症状出现前长达30年的脑脊液中都可以观察到,为预测sAD的发生和发展提供了基础。

图片来源:Cell

图片来源:Signal Transduction and Targeted Therapy
主要内容
研究概述
显性遗传阿尔茨海默病网络(DIAN)研究是一项全球研究计划,重点关注有ADAD风险的个体。作者利用DIAN的数据,对ADAD患者的脑脊液和血浆蛋白质组学进行了全面分析。研究人员发现脑脊液中137个蛋白具有显著差异,227个蛋白与脑脊液中ADAD突变状态相关。相比之下,血浆中只有3种蛋白质被发现显著改变,而7种与突变状态有关。这种改变在症状出现前大约7年的血浆和长达30年的脑脊液中都可以观察到。且诸如SMOC1之类的蛋白质在Aβ和tau等传统生物标志物之前15年就已经表现出了变化。
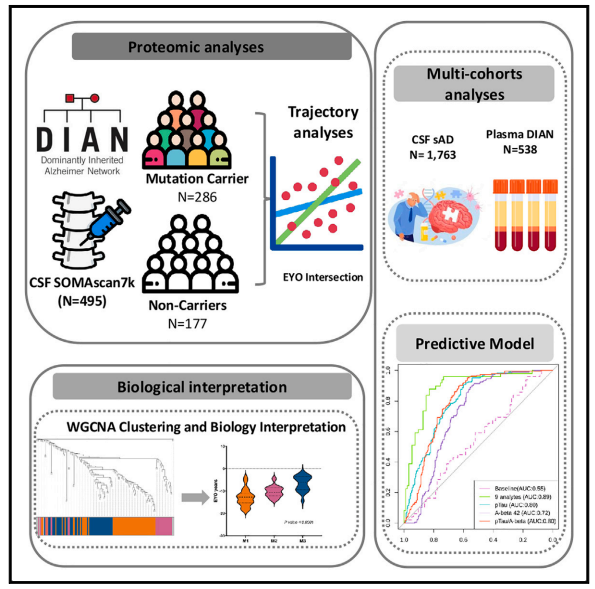
研究概述。图片来源:Cell
ADAD疾病进展的三个阶段及预测模型
通过基因集富集分析,这些蛋白质被分为三个不同的模块,代表疾病进展的不同阶段。M1模块反映了早期神经元损伤,而M2和M3模块标志着与神经炎症、免疫反应和神经元修复机制相关的进行性变化。这些发现强调了线粒体损伤、兴奋毒性和免疫过程作为ADAD病理中心特征的重要性(如下图)。
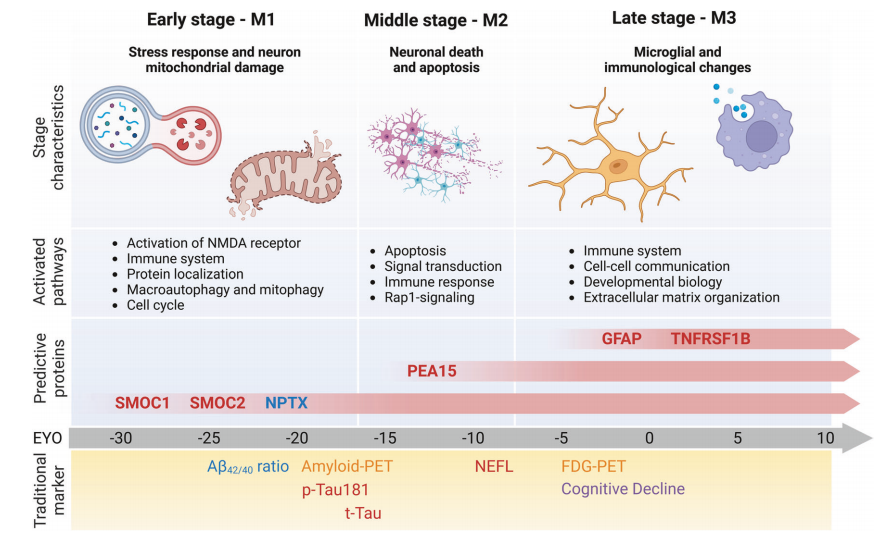
ADAD疾病进展的三个阶段及预测模型。
图片来源:Signal Transduction and Targeted Therapy
ADAD预测模型
基于所选的六种蛋白质(即SMOC1、SMOC2、NPTX、PEA15、GFAP和TNFRSF1B),建立了一个预测模型,在区分MCs和NC方面具有很高的准确性(AUC 0.911),优于传统的生物标志物,如p-Tau181 (AUC:0.755)和Aβ42 (AUC:0.709)(如下图)。在疾病发病前几十年识别蛋白质组变化代表了早期ADAD诊断的重大进步。

ADAD预测模型。图片来源:Cell
对AD病因和进展的启示
虽然对ADAD的研究已经对AD的分子和临床基础产生了实质性的见解,但将这些发现直接转化为sAD存在相当大的挑战。虽然ADAD和sAD具有共同的标志性神经病理特征,如β斑块、tau缠结和进行性神经变性。然而病因和时间进展可能存在很大差异。ADAD研究揭示的生物标志物,在更广泛的sAD人群中可能缺乏敏感性或特异性。ADAD候选生物标志物如SMOC1和GFAP可以在sAD患者中进行测试以评估其相关性。此外,单细胞测序研究可以深入了解ADAD和sAD是否有类似的蛋白质组学途径。这将弥合ADAD和sAD之间的差距,推进个性化的治疗策略。
总结与讨论
本研究为ADAD研究提供了重要的贡献。在症状出现前30年识别蛋白质组变化强调了早期诊断的重要性。针对症状前阶段可以改善生活质量,并显著延缓疾病的发生和进展。此外,新生物标志物的鉴定为治疗开发创造了新的机会。最后,使用蛋白质组伪轨迹为预测sAD的发生和发展提供了基础。
展望未来,结合蛋白质组学、基因组学、转录组学和代谢组学等多组学方法,可以全面了解ADAD和sAD的分子基础和相关病理途径。从临床角度来看,需要在更大的队列中进行验证,并随后在已建立的诊断中实施。最后,治疗探索应优先考虑针对线粒体功能障碍和突触信号中断的早期干预。


