Blood:II期临床试验揭示西米普利单抗和艾沙妥昔单抗联合治疗在复发/难治性NK/T细胞淋巴瘤中的疗效
时间:2025-03-24 12:09:39 热度:37.1℃ 作者:网络
外周自然杀伤(NK)/T细胞淋巴瘤(ENKTL)是一种罕见的侵袭性非霍奇金淋巴瘤(NHL),通常与EB病毒感染相关。ENKTL主要发生在东亚和中南美洲,其恶性程度高,预后不良。由于ENKTL对基于蒽环类的化疗具有固有的耐药性,目前的治疗指南推荐采用非蒽环类药物方案,如包含L-天冬酰胺酶和同步放化疗的新诊断患者治疗方案。然而,对于复发或难治性ENKTL(R/R ENKTL)患者,即使在初始治疗后采用挽救性治疗,包括异基因干细胞移植(SCT),预后仍然较差。免疫检查点抑制剂(ICIs)因其能够激活T细胞介导的抗肿瘤反应,已被提出作为R/R ENKTL的潜在挽救治疗。程序性死亡配体1(PD-L1)在EBV感染的肿瘤细胞上表达,与T细胞上的程序性细胞死亡蛋白1(PD-1)结合,从而抑制T细胞的抗肿瘤活性。初步研究表明,PD-1抑制剂如帕博利珠单抗在R/R ENKTL中显示出显著的单药活性。
然而,帕博利珠单抗的临床活性并不理想,其完全缓解(CR)率约为30%。其他PD-1抑制剂,如信迪利单抗和卡瑞利珠单抗,报告的CR率分别为15.4%,中位无进展生存期(PFS)和总生存期(OS)分别为6.5个月和13.3个月。PD-L1抑制剂如阿维鲁单抗和舒格利单抗的CR率分别为23.8%和35.9%。这些结果表明,尽管ICIs在R/R ENKTL中显示出一定的疗效,但仍需开发新的治疗策略以提高治疗效果。CD38是一种在肿瘤细胞和调节性T细胞(Tregs)上表达的跨膜糖蛋白。CD38的阻断被认为可以通过减少Tregs介导的抑制来增强免疫反应,从而增加CD8+ T细胞介导的肿瘤细胞裂解。基于这些发现,研究者们假设CD38阻断可以增强PD-1抑制剂的抗肿瘤活性。之前的研究表明,CD38介导的免疫抑制可能是肿瘤细胞逃避PD-1/PD-L1阻断的原因之一。因此,本研究旨在评估西米普利单抗(一种抗PD-1抗体)与艾沙妥昔单抗(一种抗CD38抗体)联合治疗在R/R ENKTL中的疗效和安全性。

方法
本研究是一项II期、单臂临床试验,评估西米普利单抗联合艾沙妥昔单抗在R/R ENKTL患者中的疗效。研究在2021年至2024年间在六个研究中心进行,共招募了37名患者。患者入选标准包括:病理学确诊为ENKTL;在至少一种化疗方案后复发或难治;东部肿瘤协作组(ECOG)体能状态评分为2分或更好;年龄在18岁或以上;在CT或PET/CT扫描上有可测量病灶;血清肌酐水平低于正常上限的两倍,转氨酶低于正常上限的三倍,胆红素水平低于正常上限的两倍。排除标准包括中枢神经系统受累和既往接受过异基因干细胞移植的患者。治疗方案包括静脉注射西米普利单抗和艾沙妥昔单抗。西米普利单抗在第1和第15天给药,每28天为一个周期,前六个周期剂量为250 mg,后续剂量增加到350 mg,每三周一次。艾沙妥昔单抗在第2和第16天给药,每28天为一个周期,剂量为10 mg/kg,前六个周期后调整为每四周一次。治疗持续至患者撤回同意书、出现不可接受的不良事件、疾病进展或研究者决定停止治疗,最长治疗期限为两年。主要终点为完全缓解(CR)率,次要终点为总体缓解率(ORR)、总生存期(OS)、无进展生存期(PFS)和安全性。
研究结果
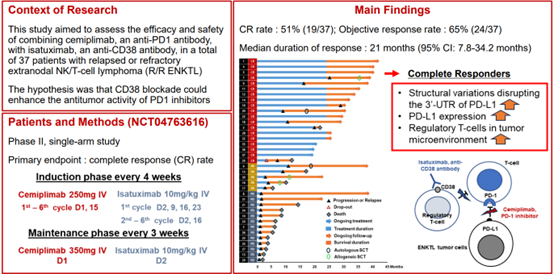
在37名患者中,CR率为51%(19/37),超过了研究的主要终点40%的目标。客观缓解率(ORR)为65%(24/37)。在中位随访30.2个月(95% CI: 25.6-34.8个月)后,中位无进展生存期(PFS)为9.5个月(95% CI: 1.4-17.6个月),而中位总生存期(OS)尚未达到。达到CR的患者接受了中位28个周期的治疗(范围:4-33),响应者的中位响应持续时间为29.4个月(95% CI: 15.4-43.4个月)。结构变异破坏PD-L1的3'-UTR和高PD-L1表达在响应者中被观察到。
安全性分析
大多数治疗相关的不良事件(AEs)为轻度至中度,等级为1或2,无4级AEs报告。最常见的AE是输注相关反应,发生在15名患者(41%)中,特别是在诱导期的第一个或第二个治疗周期。这些反应是可控的,没有患者因AE而停药。在诱导期,一名患者因3级肺炎和另一名患者因3级面部蜂窝织炎而延迟治疗,但均在恢复后继续治疗。一名患者在接受第二个周期治疗后出现3级脓毒症休克,随后退出研究。另一名患者在治疗期间出现小肠穿孔,但在恢复后继续治疗。一名患者在CR状态下出现脑梗死,尽管如此,该患者最终因疾病复发而死亡。
结论
本研究表明,西米普利单抗和艾沙妥昔单抗联合治疗在R/R ENKTL中显示出持久且可管理的抗肿瘤活性。CR率为51%,ORR为65%,中位响应持续时间为29.4个月。大多数治疗相关的不良事件为轻度至中度,无治疗相关死亡。结构变异破坏PD-L1的3'-UTR和高PD-L1表达与治疗响应相关。这些结果支持联合PD-1和CD38抑制作为一种有前景的治疗策略,特别是在R/R ENKTL患者中。然而,未来研究需要进一步验证这些结果,并优化治疗策略,特别是在肿瘤负荷高和广泛结外受累的患者中,这些患者仍面临较差的预后。
原始出处
Kim SJ, Lim JQ, Yoon SE, et al. Efficacy of Combined CD38 and PD1 Inhibition with Isatuximab and Cemiplimab in Relapsed/Refractory NK/T-Cell Lymphoma. Blood. 2025.


