Molecular cancer:罕见儿童肝癌案例:一种新的治疗突破
时间:2025-01-12 12:11:32 热度:37.1℃ 作者:网络
在儿童肿瘤中,原发性肝癌(PLC)相对罕见,仅占所有儿童癌症的0.5%至1.5%。主要包括肝母细胞瘤(HB)和肝细胞癌(HCC)。而一种名为复合型肝细胞胆管癌(Combined Hepatocellular-Cholangiocarcinoma, cHCC-CCA)的亚型更加罕见,既包含HCC的特性,又具有胆管癌(Cholangiocarcinoma, CCA)的特征,其诊断和治疗面临重大挑战。
cHCC-CCA的儿童病例极少,预后通常比HCC和CCA更差。由于其包含两种不同癌症的成分,病理诊断困难,需要结合多种技术。更复杂的是,大多数cHCC-CCA患者确诊时已处于晚期,无法手术切除,而针对不可切除病例的标准治疗方案尚未确立。
近日,由 Xia Guo 和 Guo-qian He 团队发表于 Molecular cancer 题为 Persistent response to combination therapy of pemigatinib and chemotherapy in a child of combined hepatocellular-cholangiocarcinoma with FGFR2 fusion的文章,这例罕见的cHCC-CCA病例展示了个体化治疗和联合用药的可能性,为未来制定针对性治疗方案提供了宝贵线索。
本文介绍了一例14岁女童的罕见cHCC-CCA病例。患者因持续性上腹部疼痛就医,影像检查发现肝脏多发性肿块,并伴随肺部、淋巴结和腹膜转移。肿瘤标志物甲胎蛋白(AFP)和糖链抗原19-9(CA19-9)均显著升高。初步病理诊断为肝母细胞瘤(HB),但进一步的病理分析和基因检测发现患者肿瘤中存在FGFR2-PRDM16融合基因,这是首次在cHCC-CCA中发现的特定融合基因。
在确诊后,患者接受了以选择性FGFR抑制剂pemigatinib为核心的联合治疗方案,包括Gemcitabine(吉西他滨)和Cisplatin(顺铂)。治疗周期如下:
-
初始三周期后,患者的肿瘤标志物水平恢复正常,并显示部分缓解。
-
七周期后,疾病稳定,患者表现出显著的症状改善。
-
最终,患者持续接受pemigatinib和化疗组合治疗,目前生存已超过26个月。

本病例的时间线。术前和术后肿瘤标志物(CA19-9 和 AFP)的变化。介入化疗为 DSA 引导下经导管肝动脉灌注和表柔比星化疗栓塞。AFP,甲胎蛋白;CA19-9,碳水化合物抗原 19-9;GC,吉西他滨;DDP,顺铂;CT,计算机断层扫描。
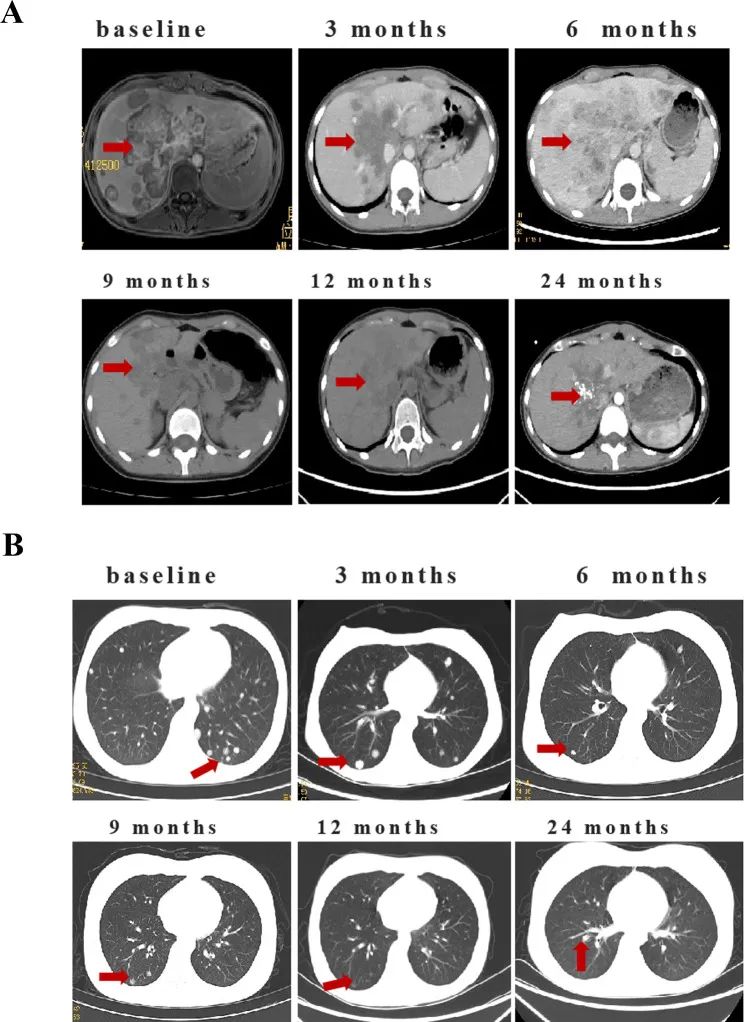
A. 腹部MRI显示,在治疗开始时(基线),肝脏内存在多个肿块,最大为9.2 × 9.8厘米(红色箭头所示)。腹部CT低信号区域显示,在治疗后3个月、6个月、9个月、12个月和24个月,肿瘤逐渐缩小。
B. 胸部CT显示,在治疗开始时(基线),肺部存在多发性转移灶(红色箭头所示)。在早期阶段,肺部病灶的高信号强度逐渐消失。
cHCC-CCA的治疗通常借鉴HCC或CCA的标准方案,但针对儿童病例的研究数据极为有限。本例的成功治疗为探索新的治疗方法提供了宝贵经验:
-
基因检测的重要性:通过新一代测序技术(NGS),发现了FGFR2-PRDM16融合基因,这为个体化治疗提供了依据。
-
靶向治疗的潜力:Pemigatinib作为一种选择性FGFR抑制剂,在成人CCA治疗中已显示出良好的效果,本例首次证明其在儿童cHCC-CCA中的应用潜力。
-
联合治疗的策略:Gemcitabine和Cisplatin的联合化疗是治疗胆管癌的标准方案,与靶向药物联合使用进一步提高了疗效。
尽管本例取得了显著的治疗效果,但cHCC-CCA仍面临以下挑战:
-
早期诊断困难:由于影像学和临床表现与HCC或CCA重叠,准确诊断依赖于病理和分子检测。
-
标准治疗方案缺乏:大多数治疗策略基于成人研究数据,儿童患者亟需更多的临床研究。
-
分子靶向治疗拓展:FGFR2融合基因虽少见,但其靶向药物显示了显著潜力,为进一步研究提供了方向。


