J Clin Oncol:Mirdametinib治疗神经纤维瘤病1型相关丛状神经纤维瘤的II期临床试验
时间:2025-03-07 12:08:52 热度:37.1℃ 作者:网络
神经纤维瘤病1型(NF1)是一种常染色体显性遗传性疾病,由NF1基因突变导致MAPK通路持续激活,引发丛状神经纤维瘤(PN)等病变。约30%-50%的NF1患者受PN困扰,表现为疼痛、器官压迫、功能障碍及生活质量严重下降。现有疗法以手术为主,但存在复发率高、创伤大等局限。MEK抑制剂通过靶向MAPK通路成为潜在治疗选择,其中selumetinib已被批准用于儿童,但对成人无效且存在吞咽限制。本研究旨在评估新型MEK抑制剂mirdametinib在成人和儿童NF1-PN患者中的疗效、安全性及生活质量改善,探索其作为新型治疗方案的潜力。

ReNeu为一项开放标签、多中心、II期临床试验,纳入58名成人(≥18岁)和56名儿童(2-17岁)NF1-PN患者。试验采用间歇给药方案(2 mg/m²口服,每日两次,最大剂量4 mg,3周用药/1周停药),疗程共24周,后续可延长至长期随访。主要终点为盲法独立中央审查(BICR)确认的客观缓解率(ORR,定义为连续两次扫描显示靶PN体积较基线减少≥20%);次要终点包括疼痛程度、疼痛干扰及健康相关生活质量(HRQOL)的改善。安全性通过监测不良事件(AEs)及实验室指标进行评估。研究同时纳入历史对照数据,比较mirdametinib与自然病程或安慰剂组的肿瘤进展风险。
在24周治疗期内,成人组41%(24/58)和儿童组52%(29/56)达到BICR确认的ORR,且额外2例成人和1例儿童在随访中获响应。成人靶PN体积中位降幅为-41%(-90至13),儿童为-42%(-91至48),超半数患者(成人62%、儿童52%)实现>50%的体积减少。疼痛及HRQOL显著改善:NRS-11评分(最差疼痛)和PPI(疼痛干扰)从基线分别下降1.3和0.7(P<0.001),PedsQL总分提高3.9(P=0.02)。缓解持续时间长,中位响应时间7.8-7.9个月,且84%(成人)和85%(儿童)完成治疗者选择继续随访。安全性方面,成人及儿童均以1级或2级AE为主,最常见为痤疮样皮炎(成人78%、儿童43%)、腹泻(48%、38%)及恶心(36%、21%)。仅1例成人发生3级视网膜静脉阻塞,无严重AE或肿瘤恶性转化。
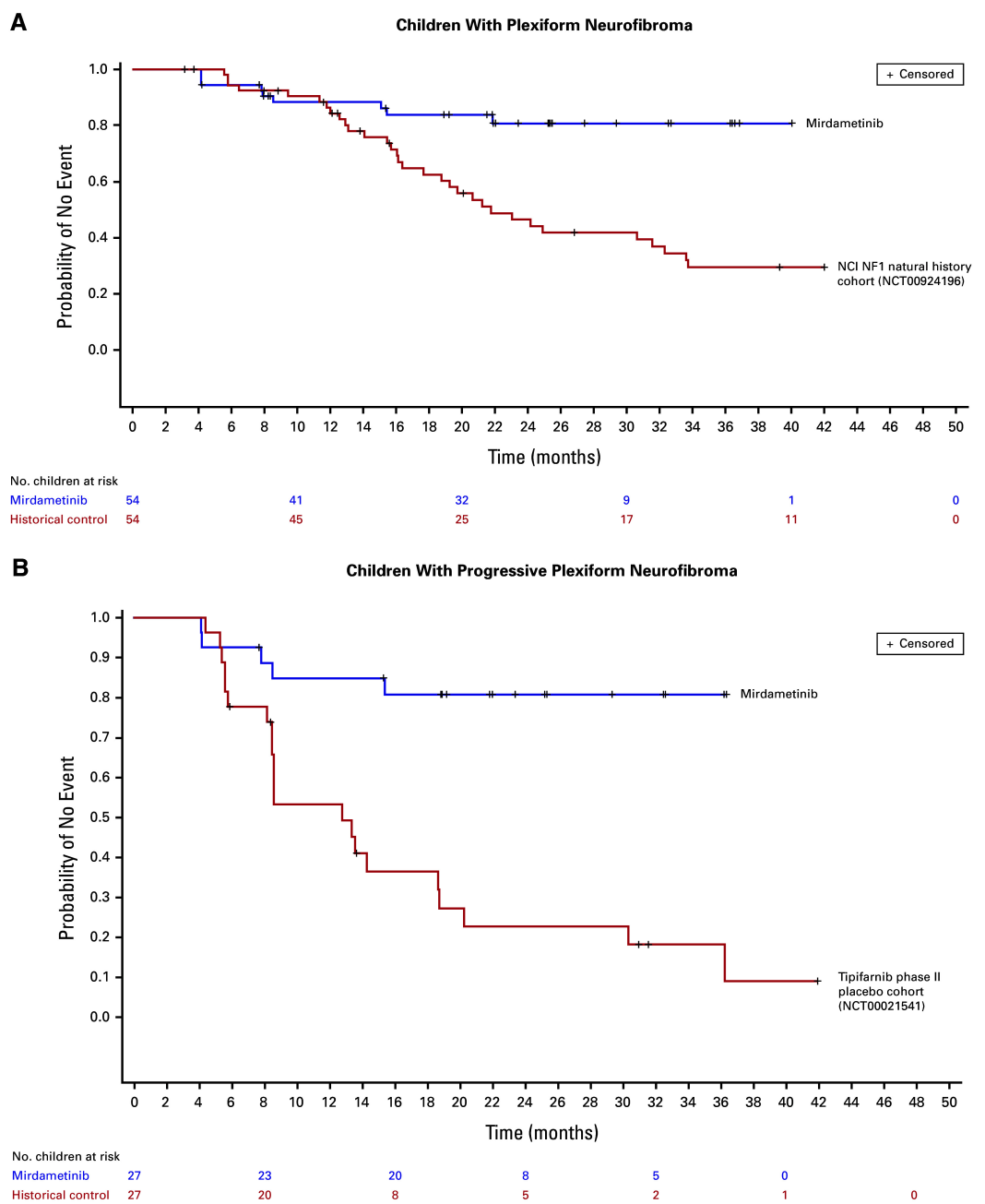
标丛状神经纤维瘤的无进展生存期:mirdametinib治疗组儿童与历史对照组的比较
ReNeu试验表明,mirdametinib在成人和儿童NF1-PN患者中展现出显著疗效,兼具深度肿瘤缓解(中位体积减少>40%)和持久性,同时显著改善疼痛及生活质量。其口服悬浮剂型便于吞咽困难患者使用,且安全性可控。相较于历史对照,mirdametinib显著延缓疾病进展并降低年体积增长率,为NF1-PN提供了首个获批适应症的成人靶向治疗方案。未来需进一步探索长期疗效、最优剂量及预防新发PN的作用。
原始出处:
ReNeu: A Pivotal, Phase IIb Trial of Mirdametinib in Adults and Children With Symptomatic Neurofibromatosis Type 1-Associated Plexiform Neurofibroma. J Clin Oncol. 2025 Feb 20;43(6):716-729. doi: 10.1200/JCO.24.01034. Epub 2024 Nov 8. Erratum in: J Clin Oncol. 2025 Jan 10;43(2):239. doi: 10.1200/JCO-24-02561. PMID: 39514826; PMCID: PMC11825507.


