【JCO】异基因CAR-T cema-cel治疗R/R LBCL的1期研究结果
时间:2025-02-24 12:10:35 热度:37.1℃ 作者:网络
异基因CAR-T
大B细胞淋巴瘤(LBCL)是成人非霍奇金淋巴瘤(NHL)中最常见的侵袭性亚型,约60%的患者可通过一线治疗治愈,但仍有部分患者会出现复发或难治性疾病。自体CD19 CAR-T细胞疗法虽对复发难治性(R/R)LBCL患者有显著疗效,但存在诸多限制,如患者需等待细胞制备、可能需要桥接治疗、治疗中心有限等。
Cemacabtagene Ansegedleucel(cema-cel)/ALLO-501是一种现货型异基因CAR-T细胞产品,通过健康供者制备,可克服自体CAR-T细胞产品的局限性,实现快速治疗,并减少对患者自身T细胞的要求。学者开展研究评估了cema-cel/ALLO-501治疗R/R LBCL的安全性、有效性和药代动力学特性。近日发表于《Journal of Clinical Oncology》。

研究方法
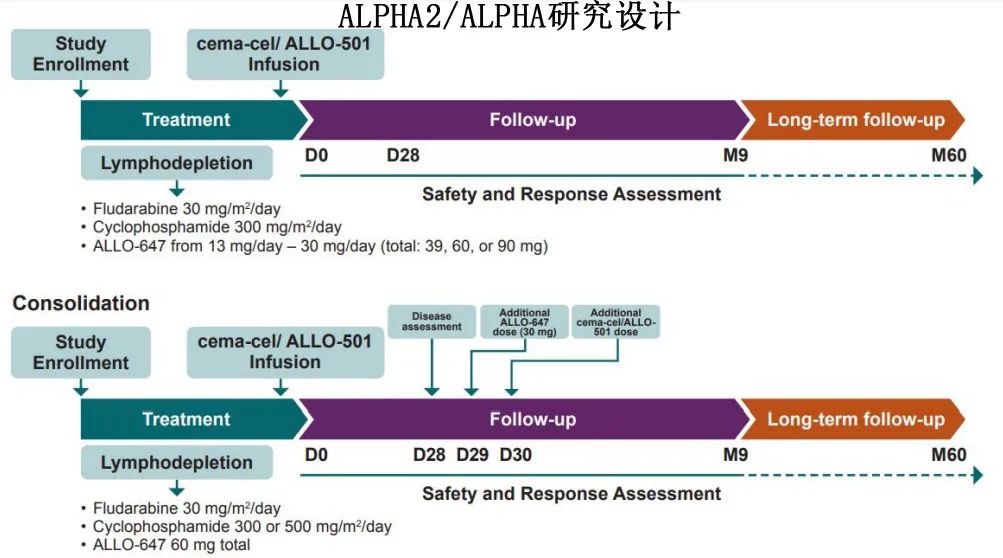
ALPHA2和ALPHA研究:为单臂、多中心、开放标签I/II期(ALPHA2)或I期(ALPHA2)研究,旨在评估cema-cel/ALLO-501的安全性、有效性和药代动力学特性。
患者选择:本次分析纳入既往≥2线治疗、未接受过CD19 CAR-T细胞治疗的R/R LBCL患者。
治疗方案:患者接受包含不同剂量ALLO-647(抗CD52单克隆抗体)的3天氟达拉滨+环磷酰胺清淋方案,随后输注健康供者来源的cema-cel/ALLO-501。
主要终点:确定最大耐受剂量和推荐II期剂量方案,评估安全性和耐受性。
次要终点:不良事件(AE)发生率、药代动力学/药效学(PK/PD)特性,通过研究者评估的总缓解率(ORR)。
研究结果
患者
共纳入33例例患者,中位年龄66岁,中位既往治疗线数为3线。中位随访10.1个月,
安全性:
未报告剂量限制性毒性。
最常见治疗相关不良事件(TEAE)包括中性粒细胞减少(85%)、贫血(67%)、血小板减少(58%)等。94%的患者发生≥3级TEAE,最常见的≥3级TEAE(≥25%)为中性粒细胞减少症(82%)、贫血(46%)、血小板减少(42%)、淋巴细胞减少(33%)和白细胞计数减少(30%)。
未报告移植物抗宿主病(GvHD)、免疫效应细胞相关神经毒性综合征(ICANS)或≥3级细胞因子释放综合征(CRS)。
感染发生率为58%,其中巨细胞病毒(CMV)再激活最常见(30%),但无致命感染。机会性感染罕见。
2期方案为120×106 CAR+细胞单次输注。
有效性:
ORR为58%,CR为42%。在接受90mg ALLO-647剂量清淋及2期剂量输注的患者中,ORR为67%,CR为58%。基线肿瘤负荷<1000 mm²的患者(通过最长径乘积之和SPD衡量)的ORR高于>1000 mm²的患者(100% vs 50%),基线乳酸脱氢酶(LDH)水平低于正常上限(ULN)的患者ORR也高于LDH高于ULN的患者(91% vs 41%)。此外,携带双打击/三打击的患者ORR高于无双打击/三打击的患者(75% vs 52%)。基线肿瘤负荷小于1000 mm²的患者CR率更高(100% vs 31%,P=0.0033),且基线LDH水平≤ULN的患者CR更高(82% vs 23%,P=0.0023)。
所有患者和CR患者中位缓解持续时间(DOR)分别为11.1个月和23.1个月,中位总生存期(OS)分别为14.4个月和未达到,中位无进展生存期(PFS)分别为3.9个月和24.0个月。在达到CR的患者中,大多数缓解持续时间超过12个月。接受2期剂量的患者中,中位DOR为23.1个月,中位OS未达到。
药代动力学和免疫重建:
CAR-T细胞在输注后观察到扩增,持续时间长达4个月。
患者中位绝对中性粒细胞计数(ANC)和绝对淋巴细胞计数(ALC)恢复时间分别为7天和17.5天。
B细胞在治疗后4个月开始在反应者中可检测到,T细胞计数在治疗后6至9个月恢复到基线水平。
总结
cema-cel/ALLO-501在R/R LBCL患者中显示出有前景的总体和持久的完全缓解率,并且具有可控的安全性特征。
异基因CAR-T细胞产品为LBCL患者提供了一种新的治疗选择,支持进一步评估其在LBCL患者中的应用。
该研究是首次展示异基因CAR-T细胞产品在治疗弥漫性大B细胞淋巴瘤患者中的安全性和有效性,并支持正在进行的随机试验,测试cema-cel作为巩固治疗在标准化疗免疫治疗后有微小残留病的患者中的应用。
作为非直接对比,下图为自体CAR-T治疗类似患者的结果。
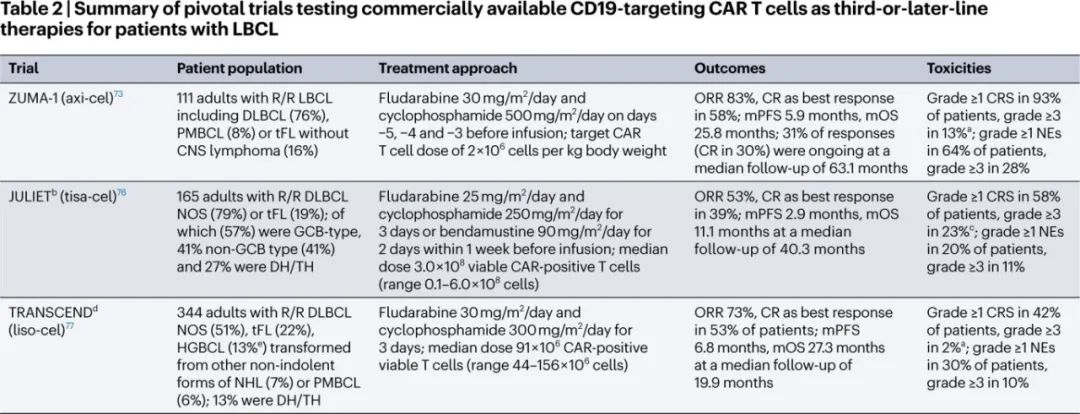
参考文献
Frederick L. Locke et al., Allogeneic CAR T Cell Products Cemacabtagene Ansegedleucel/ALLO-501 in Relapsed/Refractory Large B-Cell Lymphoma: Phase 1 Experience From the ALPHA2/ALPHA Clinical Studies. JCO 0, 10.1200/JCO-24-01933 DOI:10.1200/JCO-24-01933
Bock, T.J., Colonne, C.K., Fiorenza, S. et al. Outcome correlates of approved CD19-targeted CAR T cells for large B cell lymphoma. Nat Rev Clin Oncol (2025). https://doi.org/10.1038/s41571-025-00992-5


