Nat Commun:中山大学高艳锋/周秀曼合作研究提出用于癌症免疫治疗的基于共价肽的溶酶体靶向蛋白降解平台
时间:2025-02-13 12:09:36 热度:37.1℃ 作者:网络
溶酶体靶向嵌合体(LYTAC)策略为膜蛋白的降解提供了非常强大的工具。然而,LYTACs(抗体小分子偶联物)的合成具有挑战性。基于抗体的LYTAC穿透实体瘤的能力也很有限,尤其是穿过血脑屏障(BBB)的能力。
2025年2月6日,中山大学药学院高艳锋、周秀曼共同通讯在Nature communications 上在线发表题为“A covalent peptide-based lysosome-targeting protein degradation platform for cancer immunotherapy”的研究论文。研究提出了一种基于共价嵌合肽的靶向降解平台(Pep-TAC),通过引入一个长而灵活的芳基磺酰氟基团,该平台允许在与目标蛋白质结合时进行邻近交联。
Pep-TACs平台通过循环转铁蛋白受体(TFRC)介导的溶酶体靶向内吞机制促进靶蛋白的降解。生物学实验表明,共价Pep-TACs可显著降低肿瘤细胞、树突状细胞和巨噬细胞表面PD-L1的表达,尤其是在酸性条件下,并显著增强T细胞的功能和巨噬细胞对肿瘤的吞噬作用。此外,在抗PD-1应答和耐药的肿瘤模型中,Pep-TACs均发挥了显著的抗肿瘤免疫应答。Pep-TACs可以穿过血脑屏障,延长原位脑肿瘤小鼠的生存期。作为概念验证,本研究介绍了一种基于TRFC的模块化共价肽降解平台,用于膜蛋白的降解,特别是用于脑肿瘤的免疫治疗。

最近,靶向蛋白质降解(TPD)技术已成为一种有前途的治疗方法,它依赖于泛素蛋白酶体系统(UPS)的激活来降解细胞内蛋白质。然而,很大一部分膜蛋白(占编码基因的40%)和细胞外分泌蛋白目前不太适合现有TPD方法的范围。
2020年,Bertozzi等人报道了溶酶体靶向嵌合体(LYTAC)是获得膜蛋白降解的重要方法。LYTAC通过聚糖抗体生物偶联靶向细胞膜上的目标蛋白(POI)和溶酶体穿梭蛋白。然而,目前基于抗体的LYTAC形式存在合成困难和肿瘤穿透能力差等缺点。与抗体、融合蛋白和适配体TPD技术相比,基于小肽的TPD更直接、更具成本效益,具有更好的肿瘤穿透能力。
另一方面,溶酶体内吞受体,如ASGPR和M6PR,容易被影响POI降解的内源性配体占据。此外,尽管这些LYTAC的有限效率可以通过破坏逆转录复合体来实现,但只有极小部分受体循环回质膜,这导致无法实现POI的持久降解。为了克服这些挑战,关键在于确定TPD技术的优势靶点。转铁蛋白受体TFRC对细胞铁的摄取至关重要,是具有高回收效率的受体之一。TFRC在肿瘤细胞上过表达,并且无论周围配体的丰度如何,都保持相对稳定,这使其成为实现膜蛋白高效和持久降解的理想靶标。Nie等人最近使用与PD-L1抗体融合的基因编码的TFRC靶向肽开发了一种基于TFRC的LYTAC。然而,采用L肽的基于TFRC的LYTAC的半衰期有限且结合不理想,严重阻碍了其降解POI的功效。此外,肽与TFRC的结合稳定性差只会导致瞬时蛋白质降解。
为了提高肽在体内的稳定性并避免蛋白水解降解的快速清除,共价标记技术已被证明是有效的策略。此外,随着下一代点击化学硫(VI)氟化物交换(SuFEx)反应的发展,能够靶向包括Lys、Tyr和His在内的多种亲核残基的芳基磺酰氟(ASF)因其高稳定性和高反应速率而备受关注。因此,研究提出利用共价ASF修饰的肽作为TPD平台将大大提高肽对靶蛋白的结合能力和降解效率。不幸的是,缺乏灵活的长侧链和ASF与经典氨基酸相似的长度,限制了其交联更远靶残基的反应半径。因此,添加柔性长侧链的ASF衍生物的设计可能提供一种方便的方法,可以大大提高肽的结合耐久性和稳定性。
在这里,研究开发了一种基于模块化共价肽的溶酶体靶向降解平台(称为Pep-TAC),以促进靶蛋白的有效降解。TFRC特异性靶向D型肽DT7,其特点是结构稳定和高亲和力,占据与转铁蛋白不同的结合口袋与靶向POI蛋白结合共价肽偶联形成嵌合肽,称为Pep-TAC。作为概念验证,PD-L1是一种介导肿瘤免疫逃逸的关键免疫检查点被选中以展示Pep-TACs降解平台的实用性。研究设计并引入了一种灵活的非天然氨基酸,名为k-ASF,具有SuFEx反应特性,以提高与POI的结合稳定性,从而显着提高转运到溶酶体的可能性。这个方便的Pep-TACs平台将为高效膜蛋白降解工具的开发提供指导。
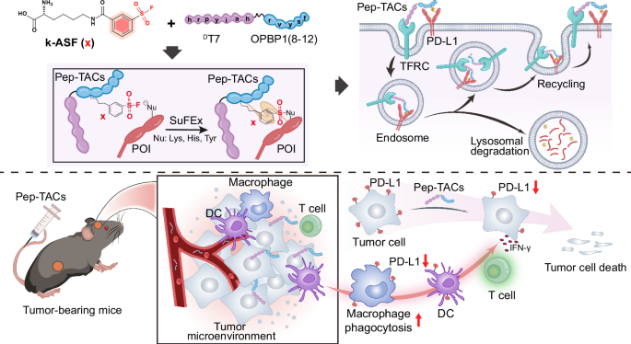
图1研究方案(摘自Nature communications )
参考消息:
https://doi.org/10.1038/s41467-025-56648-6


