Cell子刊:清华大学王一国等揭示了“肠促生存素-胰高血糖素轴”稳糖作用!
时间:2024-12-21 18:00:21 热度:37.1℃ 作者:网络
胰高血糖素对葡萄糖稳态至关重要,其失调与糖尿病有关。尽管有广泛的研究,控制胰高血糖素分泌的机制仍然不完全清楚。
2024年12月19日,清华大学王一国、上海交通大学王计秋、浙江大学孟卓贤共同通讯在Cell Metabolism在线发表题为“A famsin-glucagon axis mediates glucose homeostasis”的研究论文,该研究发现揭肠促生存素(famsin),一种肠道分泌的激素,促进胰高血糖素的释放和调节葡萄糖稳态。
从机制上讲,在小鼠中,famsin与其受体OLFR796结合(在人类中为OR10P1),启动胰岛细胞内质网中的钙释放。这个过程触发胰高血糖素分泌,从而通过胰高血糖素信号传导促进肝脏葡萄糖生成。此外,饥饿素信号的缺乏减少了肝脏葡萄糖的产生并降低了血糖水平,强调了肠促生存素-胰高血糖素轴在葡萄糖稳态中的重要性。因此,该研究结果确定了肠促生存素是胰高血糖素分泌的关键调节因子,并为维持葡萄糖稳态的复杂的肠-胰岛-肝脏器官间串扰提供了有价值的见解。

血糖的调节涉及精确的机制,以在进食、禁食、运动和应激反应中将其维持在一个狭窄的范围内。胰高血糖素(Glucagon,GCG)起源于胰腺α细胞,是一种重要的高血糖激素。在禁食期间,GCG与GCG受体(GCGR)结合,激活环AMP (cAMP)-蛋白激酶A(PKA)途径或细胞内Ca2+动员等途径,从而促进肝脏葡萄糖的产生。2型糖尿病(T2DM)患者经常表现为空腹GCG水平升高,导致血糖调节受损。GCG分泌的增加与糖尿病的发展有关,导致肝脏糖异生增高。虽然已经努力将GCGR作为控制血糖的目标,但不良的副作用阻碍了其广泛的临床应用。一种新兴的方法侧重于靶向调节GCG分泌的信号来干预高胰高血糖素血症。
血浆GCG在空腹和低血糖时升高,而在血糖正常情况下则受到抑制。GCG分泌的控制涉及多种因素的复杂相互作用。葡萄糖和旁分泌因子,由β细胞(包括胰岛素、锌、胰淀素和血清素)和δ细胞(生长抑素)分泌,在基础非禁食状态下协调抑制GCG分泌。低血糖状态下,中枢神经系统通过副交感神经系统直接输入、肾上腺素介导的交感神经系统间接作用和精氨酸加压素促进的垂体作用刺激GCG分泌。此外,氨基酸和肠道激素如葡萄糖依赖性胰岛素样肽(GIP)、胃饥饿素(ghrelin)和神经紧张素(neurotensin)对GCG分泌有积极作用,而肠促胰岛素激素GCG样肽1 (GLP1)被认为是GCG分泌的抑制剂。尽管有这些见解,空腹和T2DM期间GCG水平升高的确切机制仍不完全清楚。
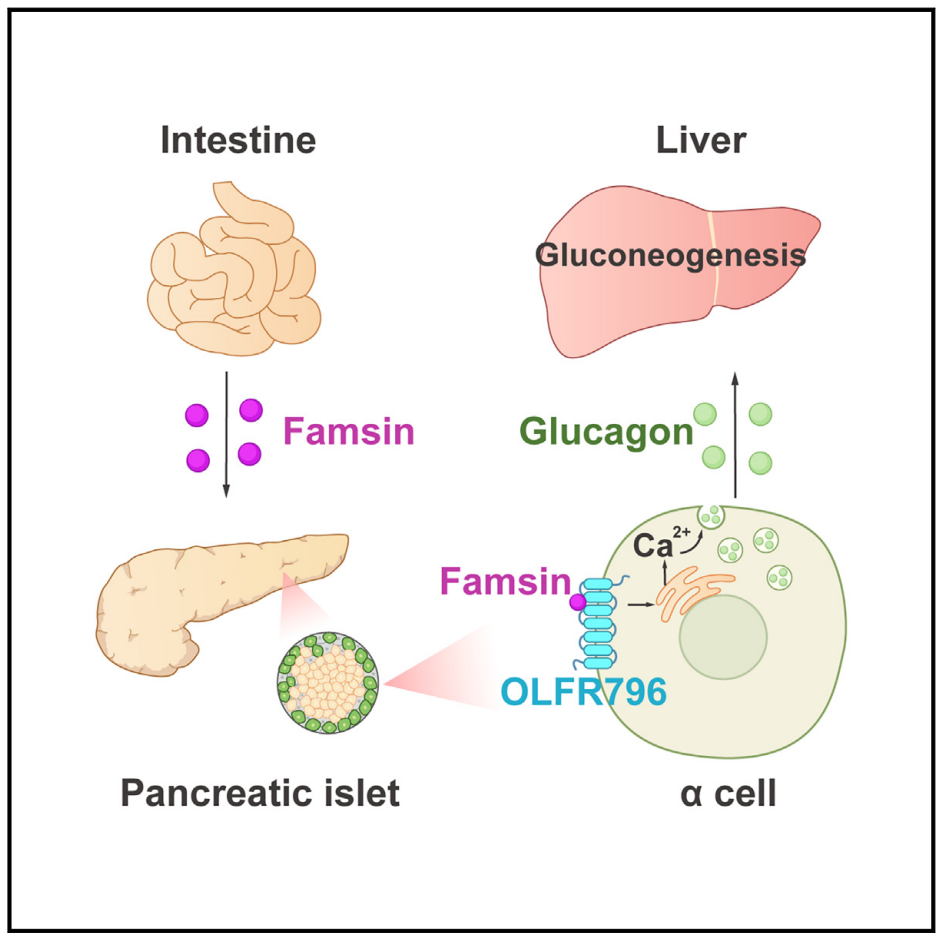
肠促生存素(Famsin)促进胰高血糖素释放并增强肝脏糖异生(图源自Cell Metabolism)
在该研究中,研究人员首次发现,Famsin可与受体OLFR796(在小鼠中)或OR10P1(在人类中)结合,激活胰岛α细胞中的内质网钙释放,从而促进胰高血糖素的分泌。这一过程对于维持肝脏葡萄糖生成及血糖平衡至关重要。小鼠实验和人群队列遗传研究表明,2型糖尿病中Famsin信号的过度激活导致了高胰高血糖素血症。在糖尿病患者中,OR10P1基因的罕见变异(如rs1472465081或rs140357644)会导致OR10P1蛋白的翻译提前终止,从而阻断其与Famsin的结合,显著降低胰高血糖素的分泌水平。这项研究揭示了空腹状态下由“肠促生存素-胰高血糖素轴”介导的肠道-胰岛器官间通信在血糖动态调节中的重要作用,进一步丰富了对肠道在2型糖尿病发生发展中重要作用的理解,并为开发新型降糖药提供潜在靶点。
参考消息:
https://www.cell.com/cell-metabolism/fulltext/S1550-4131(24)00454-6


