五年磨一剑!《ACS Nano》:微创精准空间可控中枢神经系统药物递送新技术
时间:2024-12-13 06:03:36 热度:37.1℃ 作者:网络
摘要
血-脊髓屏障(blood–spinal cord barrier: BSCB)严格调节分子从血液到脊髓的运输。团队提出了一种暂时调节BSCB通透性的方法,并将肽递送到脊髓中特定的局部区域,以高空间分辨率进行行为调节。该方法利用中枢靶向神经系统(Central nervous system: CNS)血管内壁结合分子受体的纳米颗粒的光学刺激,允许无显著胶质细胞激活或动物运动行为影响的情况下,将BSCB不透过的分子递送到脊髓。团队展示了使用微米级光纤将光微创性地通过腰椎区域递送到脊髓,实现了对BSCB通透性调节。该方法允许将一种中枢作用和引起瘙痒的肽(bombesin)递送到脊髓中的靶向区域,并诱导小鼠经历迅速和暂时地瘙痒行为。这种微创的方法使得在不进行基因修改的情况下进行行为调节成为可能,并且对以高时空分辨率将各种生物制剂分子递送到脊髓的潜在疗法具有前景。
该研究以题目:“Spatially precise and minimally invasive delivery of peptides to the spinal cord for behavior modulation”发表在ACS Nano, 2024, in press (DOI: 10.1021/acsnano.4c06030) 。
论文的预印本:“Minimally invasive delivery of peptides to the spinal cord for behavior modulation.” Zhenghong Gao, et al., bioRxiv 2022, 2022.05.20.492752 (DOI: 10.1101/2022.05.20.492752)。
技术展望以题目:“Strategies for enhanced gene delivery to the central nervous system” Zhenghong Gao, 发表在Nanoscale Adv., 2024,6, 3009-3028 (DOI: 10.1039/D3NA01125A)。
扩展性技术评论:“Ultrasound-enabled delivery of drugs to the brain: thinking outside the blood–brain barrier” Zhenghong Gao,发表在Brain-X., 2024; 2:e73. (DOI: 10.1002/brx2.73)。


【背景简介】
脊髓损伤或疾病导致的障碍可以显著降低患者的生活质量,降低患者的运动能力和基本功能控制,如排尿。不同的治疗方法可以用于治疗脊髓疾病,包括神经保护、干细胞治疗、促生长和再生治疗,以及神经回路康复。然而,血-脊髓屏障(BSCB)显著降低了对脊髓组织的治疗药物递送。BSCB的结构与血-脑屏障(Blood-Brain Barrier: BBB)相似,由内皮细胞、紧密连接、基底膜和星形胶质细胞末端组成一个功能性神经血管单元和高度调节的屏障。BSCB保护脊髓免受血液中危险循环物质的影响;然而,BSCB也显著阻碍了对脊髓疾病的有益药物治疗,因为它只允许特定分子(如水、小离子、气体和小或脂溶性分子)通过。已知BBB和BSCB阻止约98%的小分子药物和几乎所有大分子通过中枢神经系统(CNS)。因此,规避BSCB的技术将为增强对脊髓的治疗递送打开许多机会。
多种技术可能帮助绕过CNS血液屏障,如微泡(Microbubbles: MBs)增强的聚焦超声(Focused Ultrasound: FUS)或鞘内递送到脑脊液(Cerebrospinal fluid: CSF),但这些方法在脊髓内的应用有限。基于在大脑中获得的良好结果,通过FUS和充气微泡介导的BSCB调节,可能在改善脊髓递送方面具有一定的前景,然而,脊髓管内的超声由于反射脊椎骨和复杂的脊柱几何形状而产生驻波,FUS可能导致超声波在骨骼中的声热沉积,复杂化了该技术在BSCB调节中的应用。鞘内递送到脑脊液(CSF)已经被用于对于软膜病的药物治疗。然而,由于胶质极限的屏障特性,脑脊液中的药物无法自由地与脑和脊髓中的细胞间质空间有有效的物质传输,这些胶质极限是由围绕内皮细胞的星形胶质细胞末端形成的,具有相对坚硬致密的组织结构和复杂的微环境。因此,通过这种方法递送治疗药物在脊髓实质中的渗透性有限,且无法实现针对特定位置的空间分辨率。因此,局部递送治疗药物到脊髓以治疗疾病仍然是一个挑战。
光具有优异的时空控制特性,可以选择性的照射并作用于感兴趣的组织区域。例如,最近的研究设计了在小鼠中植入的硬膜外光电系统,以光刺激脊髓进行光遗传学应用。此外,Busch等人开发了光纤方法,通过侧向照明监测猪模型中的脊髓血流动力学,从而实现对大多数脊髓区域的微创访问。此外,在人类中,直径小于2.5毫米的内窥镜可以在脊髓管的蛛网膜下腔内移动。临床医生还将低强度激光热疗(LITT)用于治疗人类患者脊髓中的肿瘤。团队的研究表明,通过针对血管的金纳米颗粒和短脉冲激光光的光学刺激,可以调节血-脑屏障(BBB)并将分子递送到脑组织。短脉冲激励等离子体金纳米颗粒会诱发光机械效应,释放机械波能量影响内皮细胞中的信号通路。反过来,在体外条件下,这种BBB调节与激光激发后Ca2+的瞬时升高相关,并传播到相邻的内皮细胞,扩展BBB开放的区域,涉及内部Ca2+耗竭和Ca2+内流。此外,肌动蛋白聚合和Ca2+依赖的ERK1/2磷酸化的参与导致细胞骨架激活,增加了细胞间渗透性。这些研究证明了激发针对内皮的金纳米颗粒如何导致血-脑屏障通透性增加的可行性,并提供了机制上的见解。
【研究概况】
在本报告中,团队专注于对脊髓的精确和微创光递送,并展示了通过光学改变BSCB局部通透性(以下简称为optoBSCB),将系统性给药的生物制剂(以肽为代表)递送到脊髓并进行瘙痒调节。肽代表了一类多样的神经调节剂,对神经元产生特异性的功能调节作用。团队在一种啮齿动物模型中使用微创光纤(BSCB-Fiber)绕过脊椎,直接将光递送到脊髓以调节BSCB通透性,而没有显著影响正常运动行为,因此,团队预计该技术将为局部递送广泛的神经调节剂提供有效和安全的工具。该技术拓宽了许多不同分子和治疗药物以高时空精度微创递送到脊髓的途径。
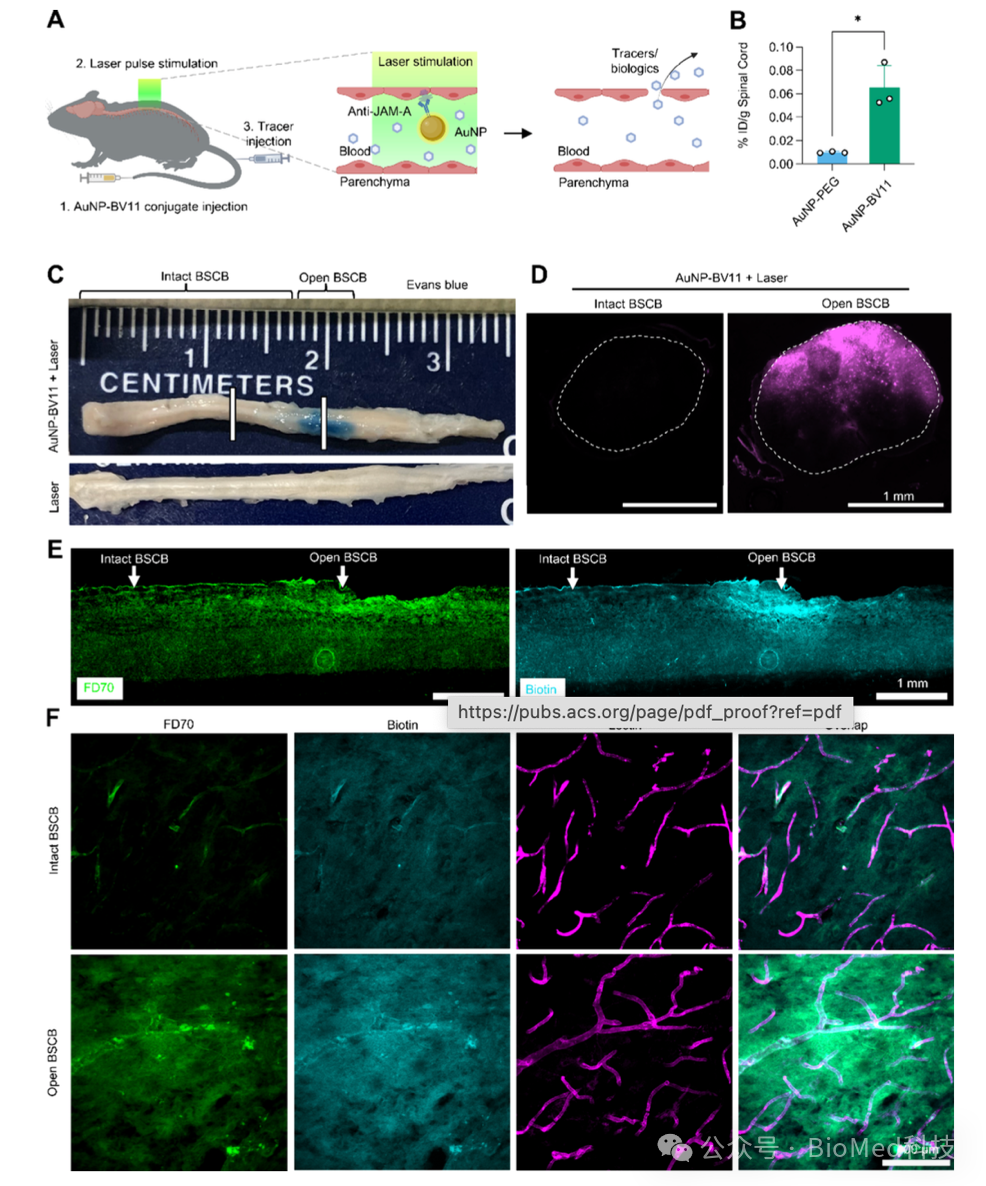
图1. BSCB调节。 (A) 激光和等离子体纳米颗粒驱动的血-脊髓屏障调节示意图(optoBSCB)。当前示意图用于(C)和(D)中的结果,其中应用了自由空间的皮秒激光脉冲。激光条件:10脉冲,频率为5 Hz,激光能量密度为20-25 mJ/cm²。(B) AuNP-BV11和AuNP-PEG在脊髓中的生物分布比较(注射后1小时)。动物被静脉注射了18.5 mg/kg的AuNP-BV11或AuNP-PEG(N=3,*P<0.05,t检验)。(C) 提取的脊髓的照片和 (D) 小鼠脊髓切片的荧光图像(在C中用白线指示)显示在用AuNP-BV11 + 激光处理的脊髓组织区域中,Evans蓝染料的渗透(上图),而单独使用激光的区域没有染料渗透(下图)。比例尺:1 mm。(E) 概述图(比例尺:1 mm)和 (F) 高分辨率图像,显示在脊髓中从Dylight 649-lectin、可固定的荧光素葡聚糖(FD70,70 kDa)和生物素(约600 Da,使用Cy3标记的链霉亲和素染色)发出的荧光信号,比较了应用激光与未应用激光的区域的小鼠脊髓。比例尺:100 μm。

图2. 空间精确的BSCB调节及其随时间的恢复。 (A) BSCB-Fiber调节的光纤光输送示意图及实验方案。对麻醉的小鼠使用异氟烷进行静脉注射和光刺激。(B) 在激光刺激后1小时、24小时和72小时的BSCB通透性与未进行激光刺激的区域进行比较。显示了Dylight 649-lectin、可固定的荧光素葡聚糖(70 kDa)和生物素(600 Da)的叠加图像。比例尺:100 μm。(C) 在BSCB开启后1小时、24小时和72小时的生物素和荧光素葡聚糖区域的定量比较,相对于lectin区域进行标准化(N=3只小鼠,每只小鼠3张图像,*P<0.05,**P<0.01,***P<0.001,****P<0.0001,使用Mann−Whitney U检验)。

图3. BSCB-Fiber对脊髓通透性和安全性的影响,实验后72小时。 (A) BSCB-Fiber调节的光纤光输送示意图及实验方案:25 mJ/cm²,10脉冲(5 Hz)。(B) 使用DAPI(细胞核)、NeuN(神经元)、GFAP(星形胶质细胞)和Iba1(小胶质细胞)对脊髓组织进行的免疫组化(IHC)染色。比例尺:100 μm。(C) 使用NeuN(神经元)、CGRP(CGRP+神经元)和IB4(IB4+神经纤维)对脊髓组织进行的IHC染色,合并成叠加图像。比例尺:100 μm。(D) (C)中白色框内区域的高分辨率放大图像,显示CGRP+和IB4+纤维的分离。比例尺:50 μm。(E) 对IHC染色组织中NeuN、GFAP和Iba1的荧光强度进行定量比较。荧光以均值±标准差(SD)表示,相对于实验后3天各自DAPI信号的荧光强度进行标准化,N=3只小鼠,每只小鼠3对图像,完整BSCB与开放BSCB进行比较;n.s.,无显著性差异,t检验。带有彩色轮廓的空白条:完整BSCB,未施加激光。彩色条:开放BSCB,施加激光。(F) 对脊髓区域的组织进行定量,比较完整BSCB(带有彩色轮廓的空白条)与开放BSCB(彩色条)区域的IB4和CGRP,标准化至各自的DAPI信号,实验后3天;N=3只小鼠,每只小鼠3对图像,完整与开放BSCB进行比较;n.s.,无显著性差异,t检验或Mann-Whitney U检验,具体取决于正态性。
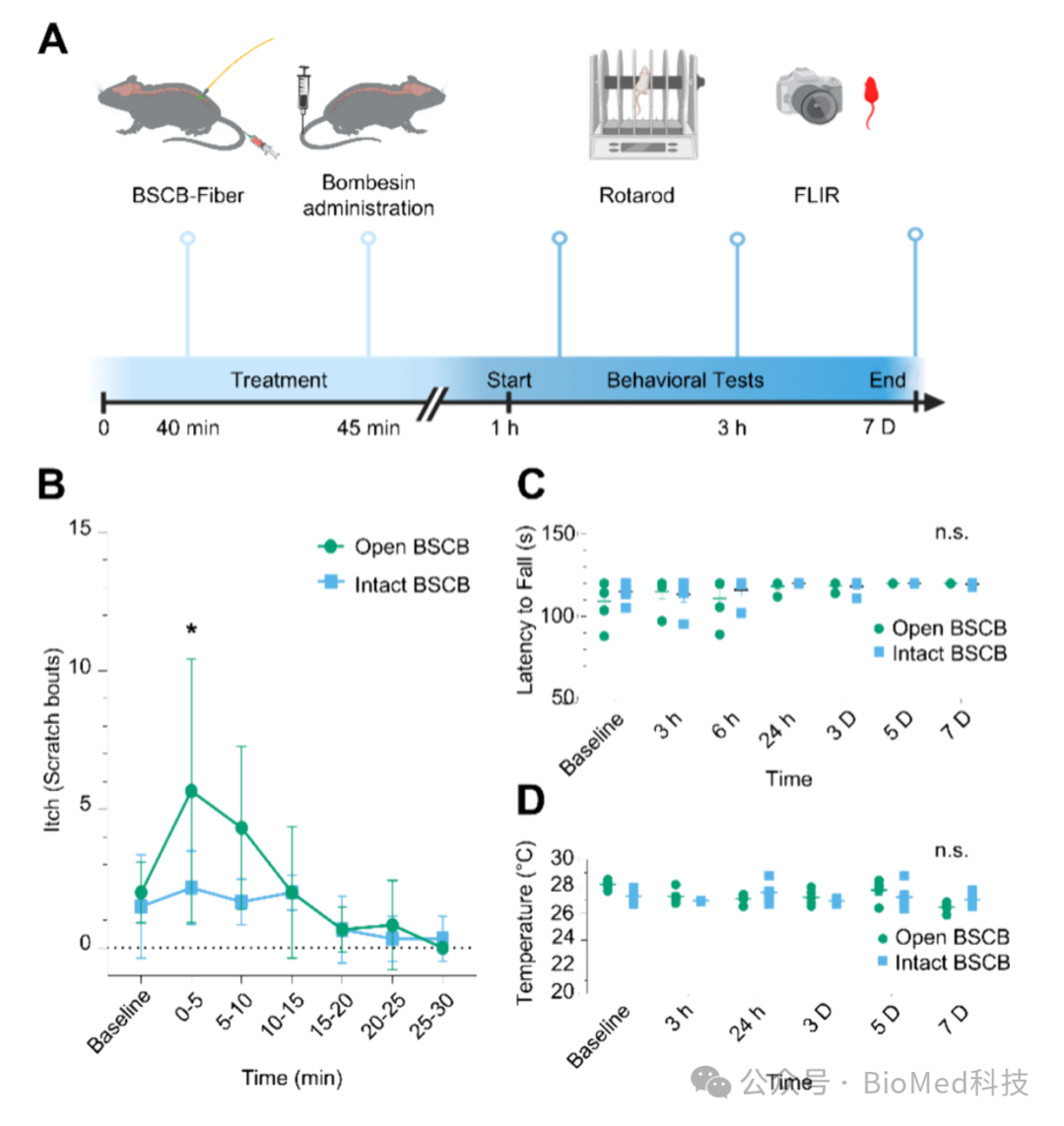
图4. 通过BSCB-Fiber进行局部肽递送到脊髓及行为调节。 (A) BSCB-Fiber调节的肽递送示意图和实验流程。(B) 与完整BSCB的对照小鼠相比,开放BSCB的小鼠表现出增加的瘙痒行为。每组N=4。*P < 0.05(调整后),开放与完整BSCB组在0−5分钟时间段的比较。0−5分钟时间点的值显示出较大的标准误差(SEM),这是由于行为数据的高度变异性。(C, D) BSCB调节对运动协调性和后爪温度的影响。每组N=5;n.s.,无显著性差异。数据以均值±标准误差(SEM)表示。使用双向ANOVA和Bonferroni校正进行多重比较。
【总结和讨论】
optoBSCB和BSCB-Fiber都有潜力提高脊髓中的药物递送效率,有希望用于基础研究和临床应用。BSCB-Fiber绕过脊椎,直接将光递送到脊髓表面的特定区域,从而安全有效地局部递送多种不同的分子。团队假设等离子体纳米颗粒和光刺激的结合会对内皮细胞和紧密连接产生光声效应,这影响钙的摄取并暂时增强通透性。
在人类中,矢状脊髓硬膜外腔的宽度在2.20到5.15毫米之间(取决于脊髓区域),而硬膜外腔的宽度在3到6毫米之间,这对于在硬膜外腔内放置导管来说足够大。因此,可以使用更大的光纤将光递送到患者的脊髓。基于光纤的探针不仅在临床前测试中具有先例,例如在猪模型中监测脊髓血流动力学,这可以接触到脊髓的大多数颈椎到腰椎区域,而且在患者的脊髓肿瘤治疗中也应用了脊髓激光热疗。在临床上,使用光学技术识别硬膜外针头通过的组织,可以减少误差性判断,从而正确识别针头是否插入硬膜外腔或硬膜下腔。硬膜外探针对脊髓组织的风险较小,而穿透硬脊膜的探针风险更高。在进一步的研究中,该技术有希望可以与光纤结合用于治疗过程中的功能监测,从而在单一光纤中实现微创的治疗诊断。BSCB-Fiber可以与磁共振成像(MRI)、微型CT和先进的脊髓内窥镜(白光和荧光)结合使用,以实现图像引导的递送。
BSCB-Fiber的一个限制是由于脊髓外白质中轴突的复杂排列,导致在可见光谱(380−700nm)中的光散射,光的穿透能力较低。为了解决这个问题,可以使用近红外激光脉冲以更深入地穿透组织。具有近红外光吸收的纳米颗粒,如金纳米棒、纳米海胆和纳米星,也可以替代本研究中使用的纳米颗粒,以调节脊髓更深区域的BSCB。此外,本研究中使用的光纤小直径也限制了光的穿透;更大的光束可以以更大的面积和深度打开BSCB。因此,团队预见到使用大直径光纤和具有近红外吸收的等离子体纳米颗粒将在大型动物和人类脊髓中实现更深的调节。另一个值得关注点是BSCB-Fiber调节后可能出现的胶质瘢痕。根据团队比较GFAP和Iba1在免疫组化染色中的荧光结果以及之前的研究。参考血-脑屏障(BBB)调节的实验,团队不认为会有显著的胶质瘢痕形成并影响治疗药物的递送。目前,BBB或BSCB的调控更适合于单次给药或不频繁的治疗给药。鉴于CGRP免疫反应性和IB4结合的变化不大,团队也预计这种方法对从形态和突触完整性角度结束于浅背角的神经末梢的影响有限。
综上所述,团队提出了一种有效的微创光学方法来调节脊髓中的BSCB通透性及其促进生物肽分子递送效率。与当前的方法(如超声和硬膜外递送)相比,这种方法提供了卓越的时空分辨率和灵活性,能够以最小的侵入性实现脊髓的局部递送。此外,BSCB-Fiber能够递送生物制剂,而不对局部细胞和行为产生负面影响。团队将诱发瘙痒的肽递送到小鼠的脊髓中,并诱导了短暂的瘙痒行为,而没有损害运动功能。在动物实验中,验证了该技术的有效性和安全性。团队展示了一种新型的血-脊髓屏障调节方法,应用于增加大分子递送效率的可行性和灵活性。
高正宏博士与主要作者共同发明了BSCB-Fiber 系统和方法。德克萨斯大学达拉斯分校已提交了一项美国专利申请。该研究得到了以下机构的资助:美国国防部,国家卫生研究院,美国医院协会,以及德克萨斯州癌症预防与研究所。
原文链接:
https://doi.org/10.1021/acsnano.4c06030


