吉林大学陈芳芳教授《自然·通讯》:神奇纳米材料——开启白血病免疫治疗新征程
时间:2024-12-02 15:01:07 热度:37.1℃ 作者:网络
一、当纳米材料 “邂逅” 抗白血病免疫:一场微观世界的变革
急性髓系白血病 (AML)是一种预后不良的异质性疾病, 5年相对生存率仅为 29.5%。传统疗法常伴有心脏毒性、骨髓抑制和易感染等副作用,导致治疗失败或复发,最终因疾病而死亡。尽管在病理生物学和新治疗靶点的识别方面取得了进展,但遗憾的是,回溯过往数十年,AML的标准治疗方法总体依旧维持旧貌,未能取得实质性革新。鉴于此,亟待探索、研发全新且行之有效的治疗策略。
纳米材料为基础的免疫疗法:抗肿瘤免疫的新机遇
纳米材料免疫疗法在白血病治疗中逐渐成为一个备受关注的领域。作为一种创新的治疗手段,纳米材料能够通过靶向特定细胞或组织,增强药物递送效果并激活免疫系统的抗肿瘤反应。随着纳米技术的不断进步,研究者逐渐认识到,纳米材料与生物体的相互作用不仅依赖于其本身的物理化学性质,还受到其表面所形成的蛋白冠的显著影响。蛋白冠决定了纳米材料在体内的分布、代谢、清除过程,并通过与免疫细胞的受体结合,激活免疫信号通路,从而推动免疫反应的发生。
过去,关于蛋白冠的研究大多集中在通过化学修饰等手段避免蛋白冠的形成,降低纳米材料免疫原性。然而,由于人体内存在成千上万种蛋白质,这种避免蛋白冠形成的策略往往效果有限。实际上,蛋白质冠中的许多成分作为天然配体,能够与免疫细胞上的特定受体结合,从而激活免疫反应。许多研究表明,适当的蛋白质冠能够引导免疫细胞的识别和吞噬,增强治疗效果。因此,理解和调控蛋白质冠的形成和性质,尤其是通过选择合适的纳米材料表面修饰,是实现高效靶向免疫疗法的关键。
二、免疫蛋白质冠调控氧化铁纳米材料免疫效能:针对急性髓系白血病的免疫疗法探索
近日,吉林大学陈芳芳教授团队系统性研究了六种精确表征的葡聚糖涂层氧化铁纳米材料(IONPs),并探讨了它们蛋白冠形成与免疫激活的完整过程,以及AML模型中的免疫治疗效果。相关工作以“Specific surface-modified iron oxide nanoparticles trigger complement-dependent innate and adaptive antileukaemia immunity”为题发表在Nature Communications。吉林大学博士生李媛媛、武文和刘起会副教授为共同第一作者,陈芳芳教授为独立通讯作者。
研究结果表明,表面修饰为羧基(IONPs-COOH)的氧化铁纳米材料能够通过补体蛋白冠增强巨噬细胞介导的肿瘤细胞吞噬作用,进而发挥抗白血病效果,此外,还能呈递肿瘤抗原并启动适应性抗肿瘤免疫反应。而氨基(IONPs-NH2)和羟基(IONPs-OH)功能化的氧化铁纳米材料未表现出类似的抗白血病效果。该差异主要来源于补体蛋白冠的形成与激活途径的不同。不同的补体蛋白冠不仅决定了纳米材料的半衰期,还深刻影响了它们与免疫系统的相互作用,从而引发不同的免疫反应。这些发现为开发更具靶向性的免疫疗法提供了重要的理论依据,也进一步认识了蛋白质冠对纳米材料免疫效能的深远影响,为纳米材料在免疫治疗中的应用提供了新的视角。
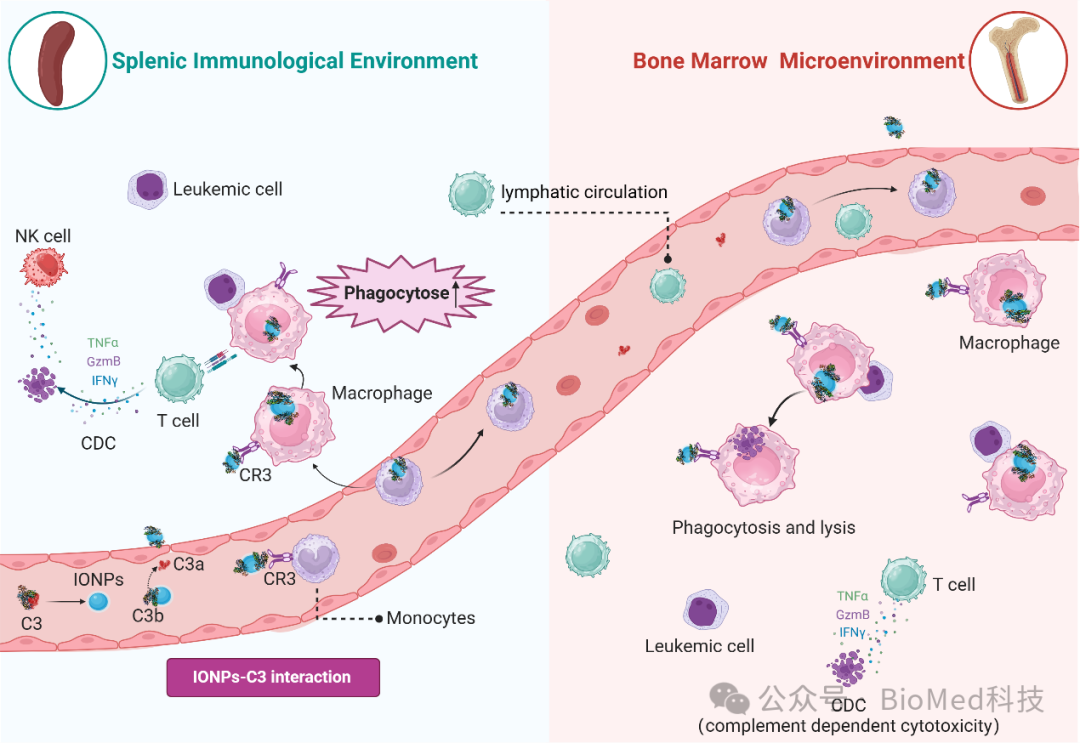
图1 | 纳米材料通过补体冠与免疫细胞动态相互作用,发挥抗白血病疗效。IONPs与补体C3b结合,形成补体冠,并通过C3受体(CR3)与循环单核细胞结合。活化后的单核细胞迁移至免疫器官并分化为常驻巨噬细胞,同时IONPs-C3b复合物增强巨噬细胞对白血病细胞的吞噬作用。巨噬细胞能够将肿瘤抗原呈递给T细胞,激活适应性免疫反应。补体的参与不仅增强巨噬细胞的吞噬作用,还可能促进其他免疫细胞的活化,进一步加强抗白血病免疫反应。
三、解锁纳米材料抗白血病 “密码”,深挖背后作用机制
研究人员首先利用体外实验验证材料对白血病细胞的直接杀伤作用,将小鼠来源的白血病细胞与IONP-COOH-21 共孵育 24 小时,通过 Annexin-V/7AAD 染色测量细胞凋亡情况。结果显示,即使在高浓度下,IONP-COOH-21 也未增加白血病细胞的凋亡率,且未影响肿瘤细胞的增殖。但在人类 AML 异种移植模型中,注射IONP-COOH-21能显著减少骨髓和脾脏中的白血病细胞,延长小鼠总体生存期。
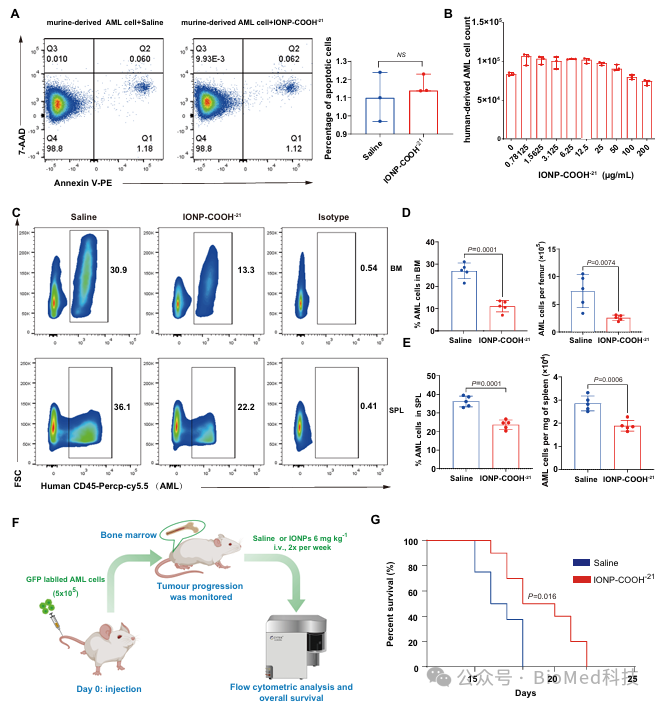
图2 | 羧基化纳米材料IONP-COOH-21在NSG AML动物模型中展现良好治疗效果,但在体外对白血病细胞未显示直接杀伤作用。
为进一步究其原因,研究人员使用具有健全免疫系统的白血病C57小鼠模型。结果显示,IONP-COOH-21 同样具有治疗作用。由于NSG 小鼠缺乏淋巴细胞,与C57小鼠模型的共同点是单核巨噬细胞和中性粒细胞系统,且先前研究表明 IONP-COOH-21 与巨噬细胞有特定的相互作用,因此研究人员将注意力转向探索巨噬细胞的潜在作用。通过腹腔注射氯膦酸盐脂质体耗尽巨噬细胞后,IONP-COOH-21 不再降低骨髓、脾脏和外周血中的肿瘤负荷,这明确表明了巨噬细胞在 IONP-COOH-21 抗白血病疗效中的关键作用。巨噬细胞作为免疫细胞,在抗白血病过程中起着重要作用。巨噬细胞来源于单核细胞,分布于全身各处组织当中,可辅助提高身体的免疫能力,具有趋化性定向运动以及吞噬的作用。当机体受到病毒或异物颗粒的威胁时,巨噬细胞可以起到吞噬异物的作用,从而使机体免疫异物的攻击。在机体创伤修复过程中,巨噬细胞能大量分泌多种生物活性物质以及多种酶类物质,引导机体修复的整个进程,还负责清除机体损伤处组织和细胞的坏死碎片以及病原体等,对创伤愈合过程有重要的调控作用。为了探索 IONP-COOH-21 与巨噬细胞之间的相互作用机制,研究人员进行了小鼠来源的白血病细胞吞噬实验。结果表明,用正常血浆预孵育的 IONP-COOH-21 可增加巨噬细胞的吞噬作用,而用 C3 耗尽的血浆则不影响吞噬作用。此外,使用 C3 KO 小鼠进行实验,发现耗尽 C3 会导致 IONP-COOH-21 完全丧失抗白血病效果,并且 IONP-COOH-21 显著增加了 NK、CD4+T 和 CD8+T 细胞中 Granzyme B 和 IFN-γ 的百分比,而在 C3 KO 小鼠中这些增加被消除。这些结果表明,IONP-COOH-21 可以通过补体依赖性方式引发先天和适应性免疫来抗白血病。
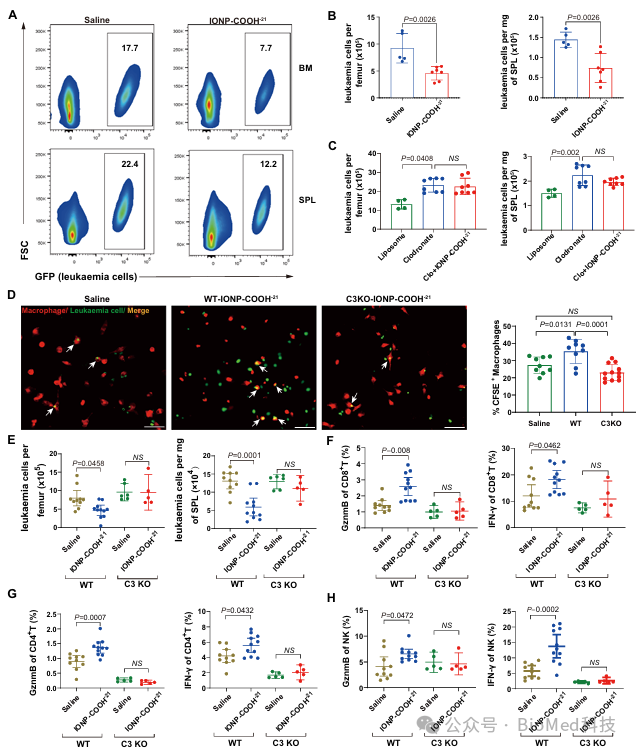
图3 | 羧基化纳米材料IONP-COOH-21通过补体蛋白冠激活抗白血病免疫。
为了研究IONP-COOH-21的免疫激活效应与机制是否适用于其他氧化铁纳米材料,研究人员采用尺寸相同,仅表面官能团修饰不同的(羟基,氨基和羧基)氧化铁纳米材料进行系统筛选和验证。
物理化学本征与抗白血病效果差异
研究人员采用多种技术对不同表面修饰的氧化铁纳米材料进行分析。通过透射电子显微镜(TEM)、动态光散射(DLS)和 X 射线光电子能谱(XPS)等技术,研究人员深入了解了这些纳米材料的形态、结构、尺寸和表面电位等特性。结果显示,所有的纳米材料均具有磁铁矿(Fe₃O₄)核心,内部铁核心大小约为 6 - 8nm,每个粒子的铁核心含量约为 0.05 - 0.06pg。同时,傅里叶变换红外光谱(FTIR)验证官能团修饰。这些结果为深入理解不同表面修饰的氧化铁纳米材料的特性提供了重要依据。为了探索不同表面修饰的氧化铁纳米材料在抗白血病方面的效果,研究人员筛选了一系列具有不同表面官能团的纳米材料,并在AML小鼠模型中进行了测试。结果发现,并非所有的纳米材料对 AML 都具有同样的治疗效果,治疗效果与纳米材料的表面官能团密切相关。具体而言,IONP-COOH-21 在 AML 小鼠模型中表现出了显著的抗白血病效果。通过抑制白血病细胞的进展和延长小鼠的生存期。然而,IONPs-OH 和 IONPs-NH2 等其他纳米材料则没有显示出明显的治疗效果。
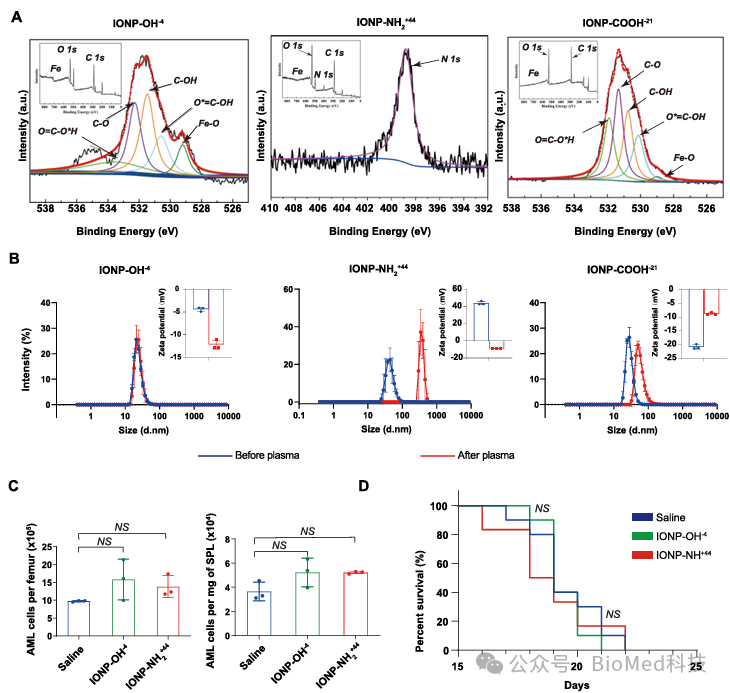
图4 |不同官能团修饰的氧化铁纳米材料的物理化学特性及其抗白血病效应。
五、纳米材料 “改头换面”:不同官能团修饰下,激活补体蛋白冠暗藏 “别样乾坤”
通过对纳米材料表面的蛋白质冠进行分析,研究人员发现不同的纳米材料吸附了不同的血浆成分,这可能是导致其免疫治疗潜力差异的关键因素。主要以补体蛋白差异最为显著,生物信息学途径分析同样表明三种纳米材料的补体途径存在差异。进一步实验验证羧基修饰的 IONP-COOH-21 通过替代途径高效激活补体,其表面结合的 Bb 水平显著高于其他两种纳米材料,当用 Bb 抗体阻断替代途径激活时,IONP-COOH-21 表面结合的 C3b 显著减少;羟基和氨基修饰的 IONP 主要通过凝集素途径激活补体,导致血浆中 MASP-1/C1-INH 水平显著增加(2 - 3 倍)。
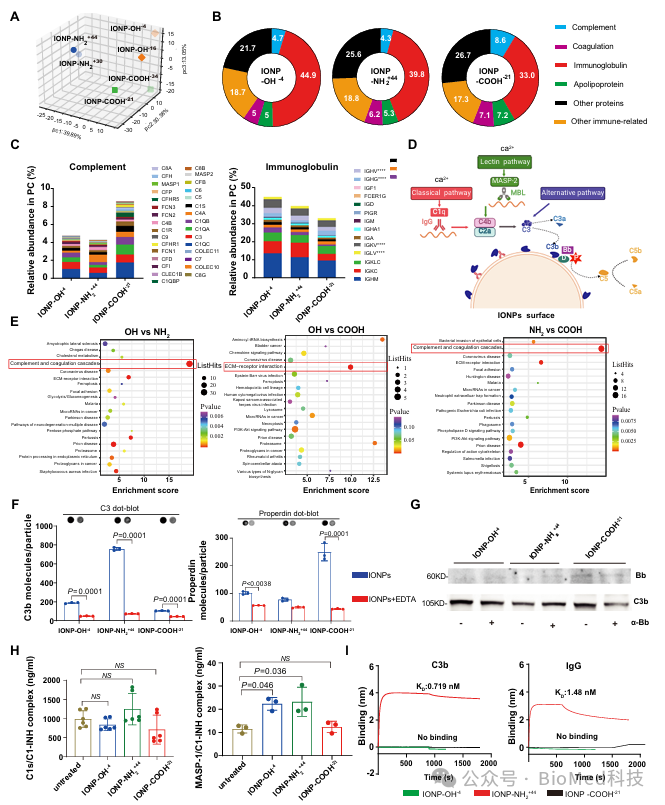
图5 |不同官能团修饰的氧化铁纳米材料补体蛋白冠形成与激活途径不同。
六.纳米材料的 “神奇变身” 密码:表面官能团如何改写药代动力学与细胞内吞轨迹
纳米材料激活补体系统的途径不同,可能会导致不同的免疫反应和生物学效应。研究人员通过电感耦合等离子体质谱法(ICP-MS)、铁定量、HE染色及流式细胞术等多种方式检测其药代动力学参数及对免疫细胞的影响。结果表明不同官能团修饰的纳米材料的半衰期和生物分布不同。IONP-COOH-21 半衰期最长,IONP-NH₂半衰期最短。这与体外实验结果一致,IONP-NH₂在与血浆孵育后具有最高的 C3b 沉积和最大的粒径,从而加速了其清除。此外,通过ICP-MS对纳米材料的生物分布进行分析。结果表明,所有三种纳米材料在注射后 24 小时主要积累在肝脏(56 - 80%)和脾脏(5 - 8%),这一结果通过普鲁士蓝染色的组织切片得到了验证。
此外,不同纳米材料影响免疫细胞在小鼠体内的分布。IONP-COOH-21 选择性被中性粒细胞和单核细胞摄取,IONP-NH₂被各种免疫细胞非选择性摄取,IONP-OH-4 几乎不被任何免疫细胞摄取。此外,在存在 EDTA 的情况下,IONP-NH₂⁺⁴⁴和 IONP-COOH-21 的 C3b 调理作用减少了 30% - 80%,这表明补体冠在这个过程中起着重要作用。研究人员进一步研究了纳米材料对小鼠免疫细胞分布的影响。结果显示,IONP-COOH-21 处理能够维持外周血中的单核细胞,而 IONP-OH-4 与生理盐水组无明显差异。值得注意的是,IONP-NH₂组表现出独特的特征,在纳米材料刺激下,CFSE⁺细胞主要向骨髓迁移,其中中性粒细胞和单核细胞的迁移尤为明显。通过分析了三种纳米材料的 C3b 质量、循环半衰期和免疫细胞摄取之间的相关性。结果显示,C3b 质量与免疫细胞摄取之间存在强烈、显著的正相关,而与循环半衰期之间存在强烈的负相关。综上所述,不同表面修饰的纳米材料可以部分解释不同白细胞类别的选择性反应及其优先再循环或迁移模式。这些结果为进一步研究纳米材料的表面性质对其免疫调节作用的影响提供了有价值的线索,也为开发抗肿瘤和抗感染治疗的纳米材料临床应用提供了新的思路。
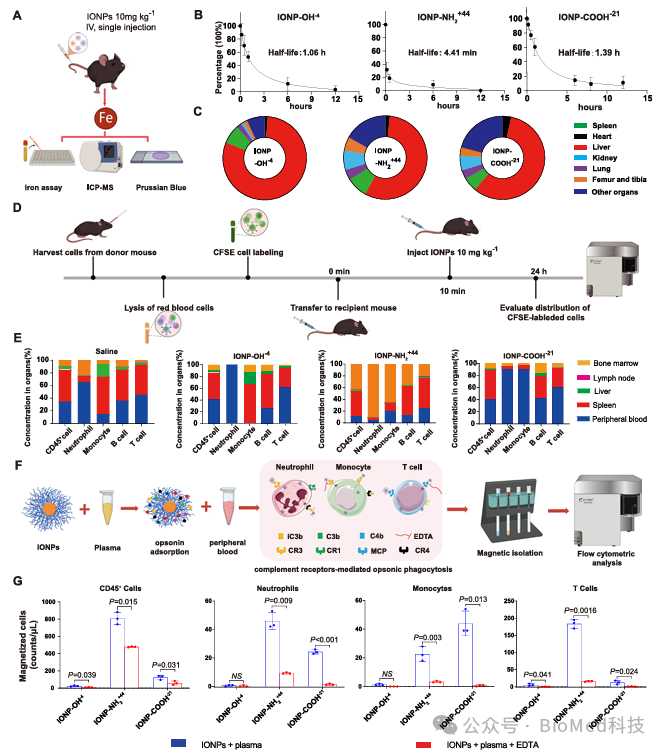
图6 |不同官能团修饰的氧化铁纳米材料的药代动力学和细胞内化的关系。
七、“魔法秀”:不同官能团纳米材料,如何导演免疫反应 “个性大戏”?
给予不同纳米材料后,小鼠免疫器官中免疫系统产生不同反应。具体而言,羧基修饰的 IONP-COOH-21 通过激活补体替代途径,增强巨噬细胞的吞噬作用,触发先天和适应性免疫来抗白血病;而 IONP-NH₂触发凝集素途径,导致免疫细胞耗竭;IONP-OH 则几乎没有明显的免疫调节作用。这些结果为调节纳米材料的免疫特性以应用于抗肿瘤和抗感染治疗提供了思路。可以根据不同的治疗需求,设计具有特定表面修饰的纳米材料,以精准调控其与免疫系统的相互作用。
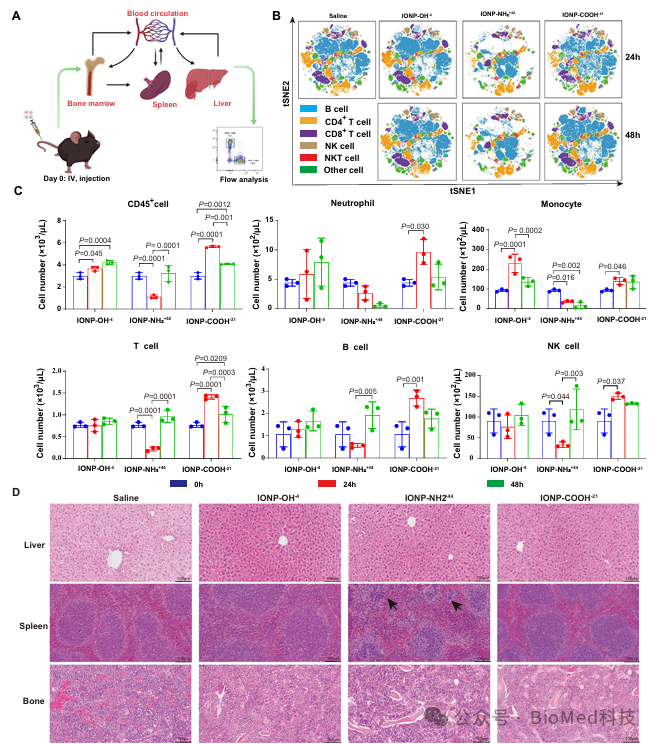
图7 |不同官能团修饰的氧化铁纳米材料诱导的免疫应答不同。
结论
特定表面修饰的氧化铁纳米材料在抗白血病免疫中具有重要作用,充分理解纳米材料理化性质,预测其个性化免疫应答规律,结合疾病个体化免疫病理特征,才能够最终实现患者的个体化、高效、安全治疗。IONP-COOH-21 通过补体依赖性方式增强巨噬细胞的吞噬作用,触发先天和适应性免疫,为急性髓系白血病的治疗提供了新的途径。不同表面修饰的纳米材料在抗白血病效果、补体系统激活途径、药代动力学和免疫细胞分布等方面存在差异,通过深入研究纳米材料的合成特性和神给特性,可以进一步优化纳米材料的设计,提高其在抗肿瘤和抗感染治疗中的效果,为医学领域的发展做出更大的贡献。
原文链接:
https://www.nature.com/articles/s41467-024-54810-0


