NEJM:2年无进展生存率72%!一线双重免疫疗法大幅改善结直肠癌疗效
时间:2024-11-29 06:00:25 热度:37.1℃ 作者:网络
结直肠癌是全球第三大常见癌症和第二大癌症相关死亡原因,每年导致近百万人死亡。约4%~7%的转移性结直肠癌患者存在DNA修复缺陷,包括微卫星高度不稳定性(MSI-H)或错配修复缺陷(dMMR)。对这些患者而言,标准化疗(无论是否联合靶向疗法)治疗后普遍预后不佳,PD-1抑制剂纳武利尤单抗(nivolumab)联合CTLA-4抑制剂伊匹木单抗(ipilimumab)是更具前景的治疗策略,这两款免疫检查点抑制剂作用机制互补,联合治疗已在多项非随机研究中显示出临床益处。
全球3期随机试验CheckMate 8HW进一步评估了这一联合治疗策略的疗效和安全性。日前,其中期分析结果发表于《新英格兰医学杂志》(NEJM)。试验结果显示,纳武利尤单抗联合伊匹木单抗一线治疗MSI-H/dMMR转移性结直肠癌患者,2年无进展生存(PFS)率72%,远高于化疗组的14%。

截图来源:The New England Journal of Medicine
CheckMate 8HW是一项3期开放标签、随机试验,评估纳武利尤单抗联合伊匹木单抗治疗、纳武利尤单抗单药治疗或化疗(联合或不联合靶向治疗)对于MSI-H/dMMR不可切除或转移性结直肠癌的效果。此次分析聚焦于一线双重免疫联合治疗方案和化疗的比较。
此次分析纳入来自全球23个国家的121个研究中心的303名患者,这些患者在当地检测出MSI-H/dMMR的不可切除或转移性结直肠癌,且未接受过针对不可切除或转移性结直肠癌的全身治疗。其中202人接受了纳武利尤单抗联合伊匹木单抗,101人接受化疗;两组分别有171人(85%)和84人(83%)后续被研究团队统一确认为MSI-H/dMMR患者。
截至分析,中位随访时间为31.5个月。主要终点针对255名统一确认为MSI-H/dMMR的患者进行评估,纳武利尤单抗联合伊匹木单抗组的PFS显著优于化疗组,12个月PFS率(79% vs 21%)和24个月PFS率(72% vs 14%)均显著更高。联合治疗组患者的PFS中位值尚未出现,而化疗组的中位PFS仅5.9个月。联合治疗的PFS获益在约3个月时就开始出现,且优势持续保持。
在所有预设的患者亚组中,包括携带RAS或BRAF突变的患者、基线肝脏、肺或腹膜转移的患者、以及林奇综合征(一种遗传性疾病,更易罹患结直肠癌等癌症)患者中,联合治疗组的PFS都更长,且12个月PFS率更高。
24个月时,纳武利尤单抗联合伊匹木单抗组的限制性平均生存时间(在一个预设时间范围内,通过统计学方法量化的平均生存时间)比化疗组长10.6个月(19.2个月 vs 8.6个月),与PFS的主要分析结果一致。
在所有303名患者中,同样观察到联合治疗组的PFS结果优于化疗组。
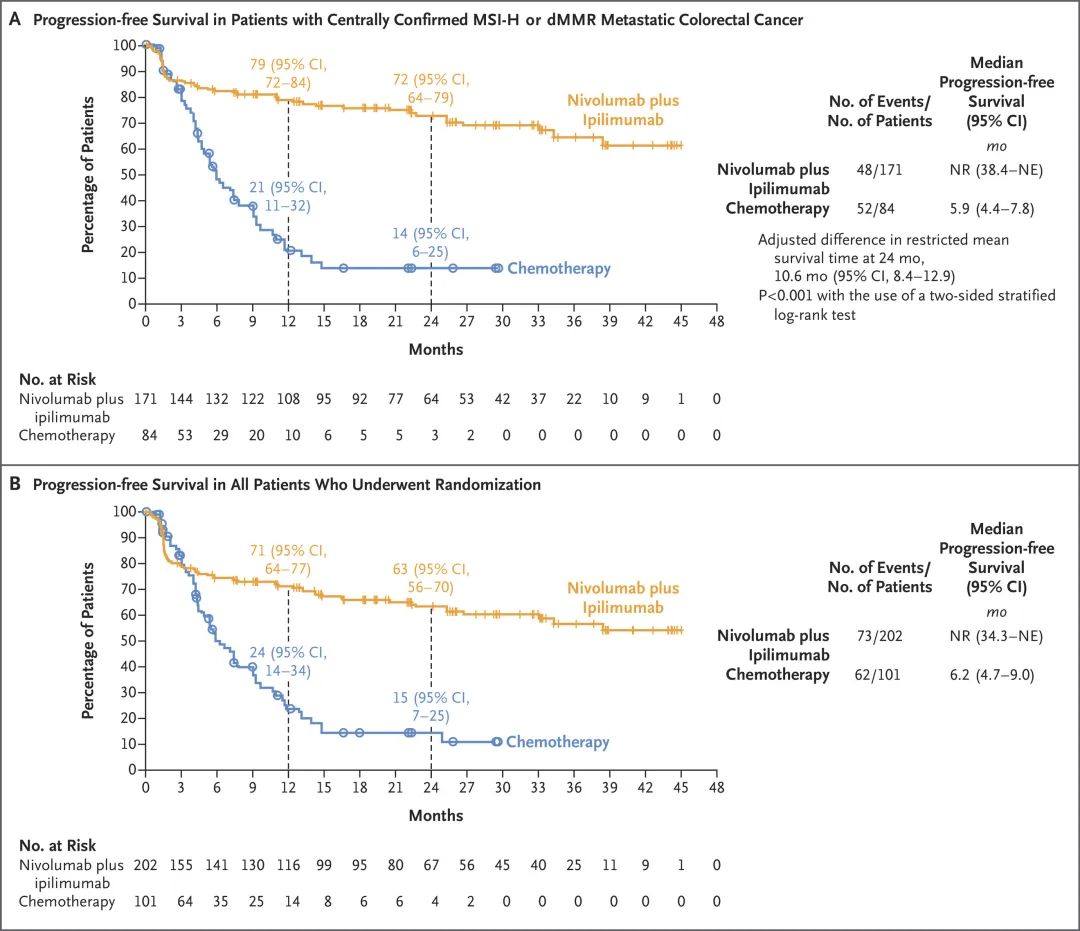
▲在255名统一确认MSI-H/dMMR的患者(图A)和所有303名在当地检测出MSI-H/dMMR的患者(图B)中,纳武利尤单抗联合伊匹木单抗组(橙色)和化疗组(蓝色)的PFS情况(图片来源:参考资料[1])
联合治疗组患者不仅生存期更长,生活质量也更好。从第13周起,纳武利尤单抗联合伊匹木单抗组相较于化疗组的健康相关生活质量具有显著获益(基于QLQ-C30量表进行评估,两组得分差异超过预先设定的有意义变化的阈值)。具体来看,从第13周开始,联合治疗组的生活质量相比研究开始时明显改善(变化幅度超过预先设定的有意义改善阈值),化疗组的生活质量变化则在前期保持稳定,到第29周时还明显下降(变化幅度低于预先设定的阈值)。
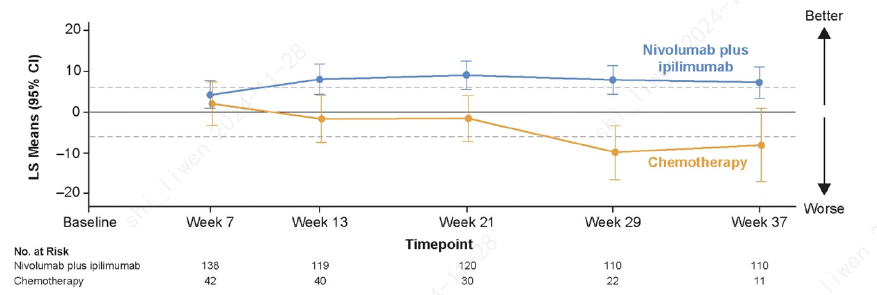
▲纳武利尤单抗联合伊匹木单抗组(蓝色)和化疗组(橙色)的健康相关生活质量得分变化(图片来源:参考资料[1])
安全性方面,纳武利尤单抗联合伊匹木单抗组23%的患者和化疗组48%的患者发生了3级或4级治疗相关不良事件。
论文在讨论中指出两点洞见。
-
这项试验中纳武利尤单抗联合伊匹木单抗的整体PFS数据,以及各患者亚组获益的一致性,均优于既往其他PD-1抑制剂单药的数据,这提示双重免疫疗法可能提高疗效。
-
其次,准确诊断MSI-H/dMMR对于筛选患者非常重要。既往PD-1抑制剂单药研究中,患者的MSI-H/dMMR状态仅由就诊当地检测,在前6个月PD-1抑制剂治疗的PFS获益都不明显;而此次研究中,在所有当地检测出MSI-H/dMMR的患者中,前3个月联合治疗的PFS获益同样不明显。进一步分析发现,此次研究当地检测为MSI-H/dMMR的患者中,有13%在后续统一检测中发现实际是微卫星稳定或错配修复功能正常的患者,而大多数微卫星稳定或错配修复功能正常的转移性结直肠癌病例对免疫检查点抑制剂具有耐药性。
总体而言,这些结果支持在MSI-H/dMMR转移性结直肠癌患者中使用纳武利尤单抗联合伊匹木单抗的治疗方案。
参考资料
[1] Thierry Andre, et al., (2024). Nivolumab plus Ipilimumab in Microsatellite-Instability–High Metastatic Colorectal Cancer. The N Engl J Med, DOI: 10.1056/NEJMoa2402141


