原发性纵隔大B细胞淋巴瘤的生物学特征、临床特征和治疗策略
时间:2025-04-02 12:09:23 热度:37.1℃ 作者:网络
PMBCL
原发性纵隔大 B 细胞淋巴瘤(PMBCL)是一种独特的 B 细胞淋巴瘤亚型,通常起源于纵隔的胸腺髓质 B 细胞,因其独特的临床表现、免疫表型、组织病理学、基因型、分子特征和治疗反应,给临床治疗带来了挑战。该病主要影响年轻成人,女性患者明显多于男性,其特征是出现巨大的前纵隔肿块,导致压迫症状。尽管 PMBCL 具有侵袭性,但患者预后良好,一线治疗早期缓解的患者 5 年生存率超过 80%。
近年来PMBCL的治疗方面取得重大进展,含蒽环类药物和利妥昔单抗的方案是一线治疗的主要手段,通常序贯纵隔放疗。然而鉴于对长期毒性的担忧,治疗方案已重新调整为根据PET引导,诱导治疗后达到完全代谢缓解的患者可以安全地省略放疗。此外,PD-1 抑制剂和 CAR-T 细胞免疫疗法等新型靶向疗法在难治性或复发性(R/R)PMBCL的治疗中也显示出令人鼓舞的效果。
《Cancer Treatment Reviews》近日发表综述,阐述了PMBCL的生物学特征、临床特征和治疗策略。

流行病学和预后
PMBCL占 B 细胞淋巴瘤的 3%,在大 B 细胞淋巴瘤(LBCL)中所占比例不足 10%。该病主要影响年轻人,且在年轻女性患者中显著多见,男女比例为1:3。PMBCL 的发病高峰在 30 至 40 岁,中位发病年龄为 37 岁。
PMBCL患者预后良好,5 年生存率超过 80%,但>60 岁患者预后较差,其 5 年生存率较低,>60岁患者的死亡率较18-39岁患者高3.5倍。
PMBCL患者如果一线治疗能迅速缓解,则预后良好。然而一旦疾病复发,控制起来就相当困难,R/R PMBCL 患者存在真正的未被满足的医疗需求。此外疾病进展通常发生于早期(18 个月内),从而反映出该病的化疗耐药性。
临床特征
PMBCL通常表现为直径>10 厘米的前纵隔巨大肿块(图 1),该肿块可浸润肺、胸壁、胸膜和心包,常导致局部压迫症状,如胸膜心包积液、呼吸困难、咳嗽和吞咽困难。此外肿块还可能压迫气道或大血管,约 50% 的患者可能会出现临床急症,如上腔静脉综合征(SCVS)。在诊断为前纵隔巨大肿块的患者中,血栓并发症常见,发生率约为 30% - 40%。多达半数患者会出现常见症状,包括胸部和颈部静脉曲张、面部水肿、结膜水肿,偶见手臂水肿。

约 80% 的PMBCL在初诊时表现为局限性 I-II 期疾病。PMBCL 在发病初期的特征通常为局部肿瘤侵袭性较强,远处转移的概率较低。在初诊时,锁骨上淋巴结受侵并非罕见,而膈下淋巴结则未见受累,骨髓或脑脊液受累的情况较为少见,但结外部位也可能受累,尤其是在疾病复发的情况下,肾脏、肾上腺、肝脏、卵巢、胰腺和中枢神经系统(CNS)受累的可能性较大。
纵隔灰区淋巴瘤(MGZL)具有与PMBCL相似的临床特征,但前者更常见于年轻男性患者,结外受累和 B 症状的发生率更高,预后明显更差。
诊断
PMBCL的诊断依据为组织病理学和生物学特征,结合该病的典型临床表现,包括患者年龄较小、女性居多以及存在较大的孤立性前纵隔肿块。
由于肿瘤肿块相关的严重临床表现和症状,PMBCL的诊断通常是在紧急情况下做出的,此时需要进行纵隔镜检查,这是一种在全身麻醉下对纵隔进行检查的侵入性胸部手术。在该过程中会采集组织样本进行组织学分析。纵隔镜检查相关的风险包括出血、感染、喉返神经暂时或永久性麻痹、气胸、皮下气肿以及食管或气管穿孔。
生物学特征
通过组织病理学检查诊断PMBCL需要综合考虑多种形态学特征以及与其相关的独特免疫表型。
组织病理学和免疫表型
PMBCL的特征为中等至大型多形性B细胞的弥漫性增殖,伴有显著的硬化和残留的胸腺结构,提示其可能起源于胸腺髓质B细胞(见图2)。其形态学特征为在不同程度的肺泡纤维化背景下呈现弥漫性生长模式,肿瘤细胞呈扁平状和/或分隔状分布。肿瘤细胞的呈圆形、多叶形或不规则形,胞质外观各异(透明或轻度嗜碱性)。透明细胞形态(与胞质水肿有关)是PMBCL病例的常见特征。在某些情况下,淋巴瘤细胞可能类似于Reed-Sternberg细胞,从而引起怀疑霍奇金淋巴瘤。PMBCL在不同病例中表现出广泛的形态学和细胞学变异。在利妥昔单抗引入之前进行的一项大型回顾性研究发现,PMBCL中观察到的不同形态学模式与预后之间并无相关性。

PMBCL淋巴瘤细胞的免疫表型特征为表达B细胞系抗原,特别是CD19、CD20、CD22和CD79a,以及转录因子如PAX5。CD30在超过80%的病例中表达,但染色强度较弱且呈异质性,与经典型霍奇金淋巴瘤(cHL)不同,而CD15表达通常缺失,但在多达6%的患者中可以观察到。CD23在70%的病例中表达,PD-L1/PD-L2在50%至70%的病例中表达,BCL2阳性率在55%至80%之间,BCL6在45%至100%之间,MUM1/IRF4在75%至90%的病例中呈阳性。MAL抗原表达是区分侵袭性B细胞淋巴瘤的标志物,有助于在疑难病例中识别PMBCL,但在常规实践中使用抗MAL抗体仍需改进。PMBCL细胞通常缺乏HLA I类和/或II类分子,这与免疫逃逸表型一致。PMBCL通常不表达免疫球蛋白,尽管其具有功能性的免疫球蛋白基因重排。此外,PMBCL还常表达OCT-2、BOB.1和PU.1。
鉴别诊断(表 1)

cHL可以通过其丰富的粒细胞、淋巴细胞和组织细胞浸润等组织学特征与PMBCL相区分。尽管这两种淋巴瘤具有不同的组织病理学特征,但它们可能表现出相似的临床特征,例如在年轻患者中出现大型纵隔肿块(≥10 cm),并且在生物学和分子特征上也有相似之处。尽管PMBCL与cHL细胞系之间存在密切关系,但在许多B细胞系标志物的表达上仍存在差异。cHL细胞系中通常检测不到完整的B细胞标志物(CD19、CD20、CD22和CD79a),而在PMBCL中则可检测到。CD30在大多数PMBCL病例中(约80%)呈阳性,但较cHL的染色强度较弱且不均匀。与PMBCL相比,cHL几乎总是表达CD15,但缺乏OCT-2和BOB.1的表达。
区分PMBCL和MGZL至关重要。MGZL曾被WHO-HAEM4R定义为“B细胞淋巴瘤,无法分类,具有介于DLBCL和cHL之间的特征”。MGZL兼具PMBCL和结节硬化型经典霍奇金淋巴瘤(NS-cHL)的特征,是一种特发于纵隔的淋巴瘤,其形态学和免疫表型特征介于cHL和PMBCL之间。MGZL的细胞学表现与免疫表型之间存在差异,可能在形态学上呈现PMBCL的特征,而在免疫表型上呈现cHL的特征,反之亦然。形态学上,MGZL的细胞通常比PMBCL的细胞更大且更不规则,类似于lacunar细胞和HL细胞;其特征为肿瘤不同区域呈广泛谱系,某些区域更接近cHL,而另一些区域则更类似于PMBCL或DLBCL。肿瘤细胞多表达CD45,当细胞学表现提示cHL时,B细胞倾向得以保留,表现为CD20和CD79a的强阳性。CD30通常呈阳性,CD15也可能表达。当组织学表现提示PMBCL时,B细胞抗原丢失,但CD30和CD15呈阳性。此外,转录因子PAX-5、OCT-2和BOB.1通常也表达。
与淋巴结DLBCL的鉴别诊断可能具有挑战性。PMBCL的特征性形态学表现(如透明细胞增殖和硬化)在小活检标本中可能难以评估,且目前缺乏可供常规应用的明确诊断标准。在这种情况下,PMBCL中CD23的表达可能具有辅助诊断价值。
分子学特征
在考虑PMBCL的鉴别诊断时,白血病/淋巴瘤分子分型项目(LLMPP)及法国基因表达检测方法的贡献值得重视。这些研究率先将基因表达谱(GEP)作为诊断工具,用于区分 PMBCL 与DLBCL、cHL和MGZL。在识别 PMBCL 特征性基因表达谱方面的进展也使其在当前的淋巴瘤分类中归类为一种独特的淋巴瘤类型,该特征性基因表达谱与 cHL(尤其是NS-cHL)的相似性高于其他类型LBCL,表明其诊断和治疗方式应有别于其他类型。
具体来说,位于染色体9p24带的JAK2、PDL1、PDL2和SMARCA2基因在PMBCL中表现出显著的高表达水平,并且PMBCL病例中常出现9p染色体的重复gain。
PMBCL的显著特征为 JAK-STAT 信号通路失调,这会导致 PDL1 和 PDL2 的表达上调(图 3)。当 PDL1 或 PDL2 与微环境中反应性 T 细胞上的 PD1 受体结合时,会增强由 PD1 介导的抑制信号,从而降低 T 细胞的细胞毒性。该活动为淋巴瘤细胞提供了一条免疫逃逸路径。大约 40% 的PMBCL病例涉及 CIITA(MHC II 类基因的转录激活因子)的易位,这是其第二种免疫逃逸机制。CIITA 易位将 CIITA 的 N 端与各种其他基因融合,因此CIITA 的一个拷贝失活,融合蛋白以显性负性的方式抑制 MHC II 类分子的表达,该过程限制了 T 细胞与肿瘤细胞的相互作用。

一线治疗
初始治疗及其效果在PMBCL的治疗中至关重要,而挽救治疗对于疾病复发或进展的疗效有限,从而凸显了在一线治疗中实现缓解的迫切需求。PMBCL 的一线治疗方案在国际上存在差异,关于最佳治疗策略的讨论仍在进行中。关键考虑因素包括初始化疗方案的选择,,纵隔区巩固放疗(RT)的适用性以及功能性成像(PET 扫描)在指导治疗决策方面的潜在作用也值得仔细斟酌。因此对于这一年轻患者群体,一线治疗需要在实现最高治愈率和最小化长期毒性之间找到平衡。
利妥昔单抗时代的化疗方案
在LBCL的化疗方案中加入利妥昔单抗显著提高了各期疾病的完全缓解(CR)率和生存率,且在PMBCL中也观察到类似效果(表 2)。
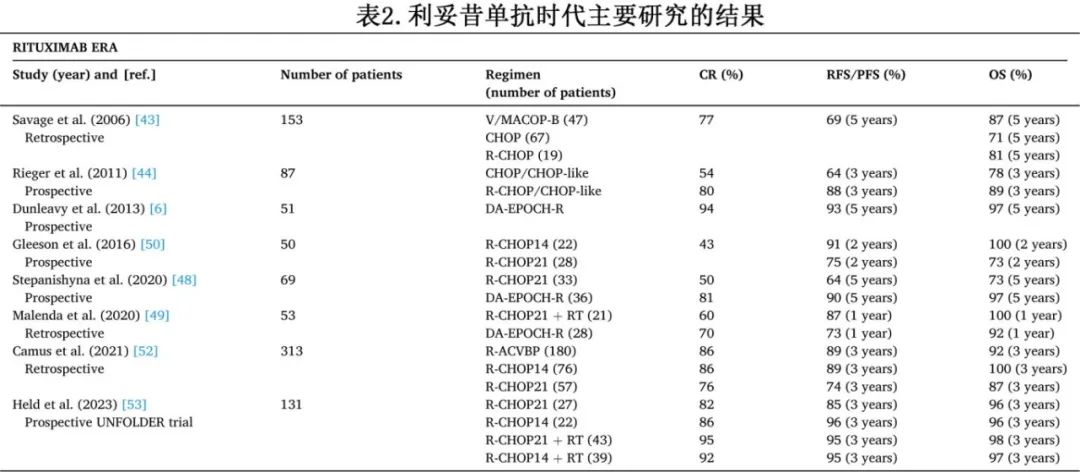
BCCA的一项回顾性调查研究了 153 例 PMBCL 患者的治疗结果,治疗方案根据特定时期的指南进行分类。V/MACOP-B(依托泊苷/甲氨蝶呤、多柔比星、环磷酰胺、长春新碱、泼尼松和博来霉素)、R-CHOP(利妥昔单抗、环磷酰胺、多柔比星、长春新碱和泼尼松龙)和 CHOP 样治疗5 年OS分别为 87%、81%和 71%(p=0.048)。
几年后,MabThera 国际试验(MiNT)对 824 例DLBCL的患者的结果进行比较,随机分为CHOP 或CHOP样化疗联合/不联合利妥昔单抗,分析还包括了 87 例 PMBCL 患者的特定亚组。接受 R-CHOP/CHOP 样方案治疗的PMBCL患者CR率更高(80% vs 54%;p=0.015),早期进展率更低(2.5% vs 24%;p<0.001),3 年无事件生存率(EFS)更高(78% vs 52%;p=0.012),但OS相似(89% vs 78%;p=0.158)。在 PMBCL 亚组中,由于样本量较小,总生存率的差异无统计学意义,但其趋势与整个研究人群的总体发现一致(85% vs 93%;p<0.001)。
上述证据支持一个共识,即在PMBCL的治疗方案中加入利妥昔单抗可以显著提高治疗效果。总体而言,利妥昔单抗的加入显著统一了不同化疗策略的疗效,并使R-CHOP方案成为最广泛使用的治疗方案。然而值得注意的是,在PMBCL中,更密集的每周化疗方案(如V/MACOP-B)或利妥昔单抗联合剂量密集型CHOP(CHOP14)相较于标准R-CHOP21方案可改善临床反应质量和PFS(这一点与DLBCL有所不同)。
在利妥昔单抗时代,DA-EPOCH-R方案的引入使得化疗敏感PMBCL患者不再需要巩固放疗,目前DA-EPOCH-R的使用显著增加,同时巩固放疗的使用也大幅减少。尽管DA-EPOCH-R具有显著的疗效,但由于其复杂性且毒性高于R-CHOP14/21和R-MACOP-B,它并未被广泛采用。R-CHOP和DA-EPOCH-R的药物成分部分相同,但DA-EPOCH-R增加了依托泊苷。接受DA-EPOCH-R治疗的患者需要住院,因为依托泊苷、长春新碱和阿霉素的给药需要持续输注96小时。与门诊治疗的R-CHOP14和R-MACOP-B不同,反复住院会显著增加治疗成本。此外,DA-EPOCH-R通过根据每个周期的造血最低点调整依托泊苷、环磷酰胺和阿霉素的剂量来增强剂量强度,从而增加了治疗方案的管理复杂性。
2016年一项纳入69例患者的前瞻性随机研究中,DA-EPOCH的疗效优于R-CHOP21,但血液学毒性有所增加。而另一项研究显示,在53例接受一线治疗的PMBCL患者中,R-CHOP21和DA-EPOCH-R的疗效结果相似且均非常出色。在该研究中,R-CHOP21组中有76%的患者接受了RT,而DA-EPOCH-R组只有59.3%的患者接受RT;此外,R-CHOP21组有40%的患者接受了自体干细胞移植(ASCT)巩固,而DA-EPOCH-R组没有患者移植。
鉴于单独采用强化免疫化疗已取得积极成果,在一线治疗中将ASCT作为巩固强化治疗的标准手段已不再必要。
总之,近期研究表明,采用基于利妥昔单抗和蒽环类药物的密集剂量免疫化疗方案治疗的患者取得极佳效果,R-CHOP14、DA-EPOCH-R 和 R-V/MACOP-B 方案的疗效相当。
NCRI开展了一项纳入 50 例患者的探索性前瞻性亚组分析,R-CHOP14 较R-CHOP21在OS和PFS方面有改善的趋势,但未达到统计学差异。IELSG开展的前瞻性 IELSG37 研究纳入 545 例患者,分别接受 R-V/MACOP-B(168 例,31%)、R-CHOP14(146 例,27%)、R-CHOP21(98 例,18%)、DA-EPOCH-R(88 例,16%)、R-megaCHOP(19 例,3%)及其他强化剂量方案(26 例,5%)治疗,各方案的CR率(Deauville 评分 1 - 3 分)无显著差异;然而Deauville 评分分布并不均衡,似乎是因为 CHOP21 方案中 Deauville 评分为 5 分的患者比例明显高于其他方案(约两倍)。此外,在法国和比利时 25 个中心开展的一项回顾性多中心研究共纳入 313 例患者,其中 180 例接受 R-ACVBP(利妥昔单抗、多柔比星、环磷酰胺、长春地辛、博来霉素和泼尼松)作为一线治疗,76 例接受 R-CHOP14 治疗,57 例接受 R-CHOP21 治疗。治疗结束时,R-ACVBP、R-CHOP14 和 R-CHOP21 的完全代谢缓解率分别为 86.3%、86.8% 和 76.6%;中位随访 44 个月,3年PFS率和OS率分别为 89.4%、89.4%、74.7% 和 92.4%、100%、87.5%。然而由于是回顾性分析,该结果受到选择偏倚的影响:R-ACVBP、R-CHOP14 和 R-CHOP21 组分别有 46 例(25.6%)、24 例(31.6%)和 1 例(1.8%)患者接受了移植巩固,分别有 4 例(2.2%)、11 例(14.5%)和 2 例(3.5%)患者接受了放疗。
在 3 期随机 UNFOLDER 研究中,131 例PMBCL患者被随机分配接受 R-CHOP14 或 R-CHOP21 治疗。随后,所有达到未确认完全缓解(CRu)或部分缓解(PR)(根据 1999 年国际标准化反应标准)的患者分配接受放疗(82 例患者)或观察(49 例患者)。R-CHOP14 ±放疗和 R-CHOP21 ±放疗的PFS和OS均无显著差异。然而治疗结束时的反应评估使用的是较旧标准,未包含FDG-PET。
最后,近期一项系统性综述和荟萃分析纳入 4068 例PMBCL患者,比较了强化免疫化疗(DI-CIT)与标准化疗(S-CIT)作为PMBCL一线治疗。S-CIT 方案包括 R-CHOP21/CHOP21 方案,联合或不联合放疗;而 DI-CIT 方案包括频率更高、剂量更大和/或系统用药种类更多的方案(如 DA-EPOCH-R、V/MACOP-B、R-CHOP14 等)。DI-CIT 的OS为 88%,而 S-CIT 为 80%。
总之,目前比较 R-CHOP14 与 R-CHOP21 治疗PMBCL的研究数量有限,且样本量较小、设计欠佳。总体而言,2 周方案在短期终点(缓解率)和疾病特异性结局(EFS、PFS)方面效果更佳,但由于接受 R-CHOP21治疗的患者中RT及挽救治疗使用率更高,因此在OS方面的优势有所减弱。由于缺乏 R-CHOP14 与 R-CHOP21 之间高质量的随机对照试验,鉴于 R-CHOP14 的疗效、耐受性以及对放疗和挽救治疗需求的减少,可将其视为首选。
PET扫描在PMBCL中的作用
免疫化疗后的PET扫描及疗效评估
PET 扫描是评估PMBCL初始疾病扩散情况以及监测治疗反应的有效工具,然而由于 PET 扫描常出现假阳性结果,表现为纵隔炎症性残留摄取,而活检发现并非活动性病变,因此依靠 PET 扫描评估治疗效果存在困难。因此,应在一线免疫化疗结束后 5-6 周进行 PET 扫描。
免疫化疗后 PET 阴性与良好的预后及更长的PFS显著相关。在此背景下,IELSG开展的前瞻性 IELSG-26 研究起到了关键作用,该研究旨在确定一线免疫化疗后 PET 的反应率。该研究显示,治疗结束时 PET 结果阳性(残留摄取量大于纵隔,依据之前的IHP标准]) PMBCL 患者与 PET阴性(残留摄取量小于或等于纵隔:Deauville 评分 ≤2))患者的 5 年PFS率分别为 82% 和 98%,具有统计学差异。
在 2014 年Lugano发布以及 IELSG-26 研究结果公布之后,完全代谢缓解(CMR)的定义标准从 Deauville 评分 2 分调整至 3 分,且判定 CMR 的基准从纵隔血池(MBP)活性变更为正常肝组织活性。此外,IELSG-26 研究表明,以肝脏摄取作为PET阳性的cutoff值能最有效地区分复发或进展的高危或低危人群,5 年PFS率分别为 99% 和 68%(p<0.001),5 年OS率分别为 100% 和 83%(p<0.001)。因此,肝脏摄取比 MBP 更适合作为cutoff,以识别出复发或疾病进展风险显著增加的患者。
IELSG-26 研究还表明,治疗结束时PET具有较高的阴性预测值(所有获得 Deauville 评分 ≤3 的患者在 5 年内均无疾病进展),但阳性预测值较低;治疗结束时 Deauville 评分为 4 分的患者预后明显优于评分为 5 分的患者。该结果表明,在没有临床疾病进展指征的情况下,仅依据 PET 阳性结果推荐挽救性化疗和/或巩固治疗时应采取更为谨慎的态度。
一线免疫化疗后PET的作用及巩固放疗
如前所述,挽救性治疗对于疾病复发或进展的疗效有限,从而凸显了一线治疗对于提高治愈率的重要性,并引发了有关其范围的重要问题,尤其是纵隔巩固RT是否总是必需,以及PET摄取值能否用于指导该决策。
部分中心将免疫化疗后的放疗作为初始治疗的常规部分,回顾性研究也表明,对纵隔进行巩固放疗可取得最佳疗效。尽管该方案与积极结果相关,但在年轻患者群体中,其与长期并发症(尤其是心脏疾病和继发性治疗)的较高风险有关。近年来,成像技术、RT计划以及RT的精确性和给药方式的重大进步彻底改变了这一领域。现代RT应导致极少的急性或迟发性副作用,但该做法正越来越多地受到挑战,特别是考虑到接受上述DA-EPOCH-R方案治疗的小型患者队列的结果。
关于PMBCL患者是否可以省略RT的问题,IELSG37 研究给出了答案,其旨在探究在常规一线免疫化疗后达到CMR(Deauville 评分 1-3 分)的患者中,省略纵隔RT的可行性。IELSG37 研究是迄今为止针对 PMBCL 最大规模的随机研究,是一项 3 期、随机、开放标签、多中心(13 个国家的 74 个中心)两臂对照研究,旨在评估放疗在 PMBCL 中的作用。试验结果表明达到 CMR 的患者预后良好,省略RT不会影响生存率。入组的545例患者中,268例在诱导治疗后达到 CMR 的患者纳入观察组(n=132)或RT组(n=136)。观察组的 30 个月PFS率为 96.2%,放疗组为 98.5%,分层风险比为 1.47,绝对风险差异为 0.68%;两组的 5 年OS率均为 99%。
IELSG37 研究还证实,治疗结束时 Deauville 评分为 4 分的患者预后明显优于5 分患者,后者 5 年PFS和OS显著更低(分别为 60.3% 和 74.6%),而4 分患者分别为 95.8% 和 97.5%,与达到CMR的患者无显著差异。该结果表明,至少部分 4 分患者可能存在化疗后假阳性炎症病变,或者在RT后从PR转为 CMR(因为 86% 的患者接受了巩固RT)。对于一线免疫化疗后达到 Deauville 4 分的患者,虽然部分研究者主张进行巩固RT,但也有研究者建议采取更保守的策略,即在开始放疗前 4 至 6 周进行重复PET监测,标准摄取值(SUV)降低可能表明可以省去放疗。
鉴于这些结果,可以得出结论:对于一线免疫化疗后达到CMR(Deauville 评分 1 - 3 分)的患者,采用PET驱动的方法可安全地省略纵隔放疗。
PET扫描的预后特征
有研究旨在寻找新的定量功能PET参数(QPM),以识别极高危患者,并将其作为接受更强化疗方案(如DA-EPOCH-R)的候选对象。在IELSG26研究中,对103例PMBCL患者的基线PET扫描中,根据标准方案测量了代谢活性,包括最大标准化摄取值(SUVmax)、代谢肿瘤体积(MTV)和总病变糖酵解(TLG)。在单因素分析中,较高的MTV和TLG值对PFS和OS具有显著的不良预后影响。在多因素分析中,只有TLG升高对OS和PFS均保持统计学意义。因此,基线PET扫描中的TLG似乎是一个强有力的PMBCL预后预测因子。
此外,在 IELSG26 研究中,基线TLG与治疗结束时的 Deauville 评分相结合,其阳性预测值优于单独使用 TLG。TLG >5814且中期 Deauville 4-5 分的患者预后明显较差。
R/R PMBCL的挽救治疗
R/R PMBCL是一个重大的医疗难题,主要是因为疾病进展时预后不佳,这与一线治疗通常效果良好形成鲜明对比。在一线治疗后的前 18 个月内,约 15% 至 20% 的PMBCL患者会出现复发。复发主要发生在纵隔外部位,如肾上腺、肾脏、卵巢和肝脏,而CNS或骨髓受累则较为罕见。
对于可能存在疾病进展的情况,建议进行全面活检,这不仅是为了排除PET的假阳性结果,也是为了通过免疫组化检查 PDL1 是否过度表达(前提是初次诊断时未进行此项检查)。此外,还建议重新评估 CD19 和 CD20 的表达情况,并检查是否存在符合MGZL或cHL特征的复合型或序贯型淋巴瘤。
不同国家以及获批药物之间的治疗标准存在差异。在已批准将CAR-T疗法作为二线治疗的国家,CAR-T 疗法已成为标准治疗方案,而在尚未批准将 CAR-T 疗法用于二线治疗的国家,标准治疗方案仍是大剂量化疗方案,如 R-DHAP、R-ICE 或等效方案,并辅以ASCT。然而,R/R PMBCL对大剂量化疗的耐药性常常导致挽救治疗失败,从而无法进行ASCT,或在移植后早期复发,最终导致预后极差,复发或进展后的 2 年总生存率仅为 15%。
CAR-T 细胞免疫疗法
3 期 TRANSFORM 研究在多种LBCL亚型中比较了liso-cel 与标准治疗,其中包括 18 例PMBCL患者(liso-cel 组 8 例,标准治疗组 10 例)。该研究促使 liso-cel 获批用于一线免疫化疗后难治或 12 个月内复发的 PMBCL 患者。
在 CAR-T 细胞免疫疗法尚未作为二线治疗手段的国家,可将其作为三线治疗选择。在注册研究的背景下,基于 ZUMA-1 研究的结果,axi-cel已获批用于R/R PMBCL患者的三线治疗。但该研究仅纳入 8 例 R/R PMBCL 患者;此外 TRANSCEND NHL 001 研究中仅有 15 例 R/R PMBCL 患者接受 liso-cel 治疗。
tisa-cel尚未获得用于PMBCL,因为关键 JULIET 研究中并未纳入相关组织学类型。
临床实践进一步提供了有关 CAR-T 细胞三线治疗PMBCL的实际疗效的更多数据。Crombie 等报告了 2018 年至 2019 年期间,在美国 5 个中心接受 axi-cel 治疗的 33 例 R/R PMBCL 患者(既往中位3线治疗)的结局,结果ORR为 76%,CR率为 67%,24 个月PFS为 64%,24 个月OS为 78%。19 例患者在 axi-cel 输注前(14 例)、后(4 例)或前后(1 例)接受了抗 PD1 治疗,对于axi-cel 治疗前或治疗后进行免疫检查点阻断治疗的患者,在 axi-cel 的疗效和毒性方面没有明显差异。
在真实世界研究的背景下,意大利 CART-SIE 注册中心关于 axi-cel 治疗的经验也值得一提。该研究旨在评估 axi-cel 在 70 例PMBCL患者中的疗效,并将其与 190 例其他DLBCL患者(意大利前瞻性观察性 CART-SIE 研究)进行比较。中位随访 12.17 个月,PMBCL 患者的 12 个月PFS率为 62%,而其他 DLBCL 患者为 48%(p=0.0386);12 个月OS率为 86%和71%(p=0.0034)。总之,接受 CAR-T 细胞治疗的R/R PMBCL 患者的预后明显优于其他 DLBCL 患者。
新药和检查点抑制剂
由于PMBCL具有表达 PDL1 和 CD30 等生物学特性,近年来开展了针对新药的研究,包括帕博利珠单抗和纳武利尤单抗(抗 PD1 检查点抑制剂)以及维布妥昔单抗(BV)(抗 CD30 抗体药物偶联物)。PMBCL 核型中 9p24.1 位点的频繁扩增或重排导致淋巴瘤细胞中 PDL1 和 PDL2 的过度表达,为使用抗 PD-1 阻断剂提供了依据。
关键 2 期 KEYNOTE-170 研究评估了帕博利珠单抗在至少接受过 2 次治疗且不适合ASCT的R/R PMBCL患者中的应用。53 例患者接受了每 3 周 200mg帕博利珠单抗输注,最多持续 35 个周期(2 年),直至出现疾病进展或不可接受的毒性反应。ORR为 41.5%(20.8%达到CR,20.8%达到PR)。帕博利珠单抗的中位至缓解时间为 2.7 个月。中位随访 4 年,中位PFS和OS分别为 4.3 个月和 22.3 个月,4 年 PFS 和 OS 率分别为 33%和 45.3%。
1/2 期开放标签、多中心 Checkmate 436 研究纳入R/R PMBCL患者,评估了纳武利尤单抗和维布妥昔单抗。30 例重度经治的 R/R PMBCL 患者每 3 周接受一次维布妥昔单抗1.8mg/Kg和固定剂量 240mg纳武利尤单抗治疗,直至疾病进展或出现不可接受的毒性反应。ORR为 73.3%,CR和PR分别为 40.0% 和 33.3%。中位至缓解时间为 1.3 个月。中位随访 39.6 个月,中位PFS为 26.0 个月,中位OS尚未达到,24 个月 PFS 和 OS 率分别为 55.5% 和 75.5%。12 例(40%)缓解患者根据研究者判断接受了后续巩固性自体(6 例患者)或异基因(6 例患者)移植,100 天完全缓解率为 100.0%。目前尚不清楚接受含抗 PD-1 药物治疗方案后达到CMR的患者是否应接受进一步的巩固治疗(如自体或异基因移植或 CAR-T 细胞免疫治疗),还是仅需观察即可。
鉴于 Zinzani 等报告的一项 2 期研究中,BV作为单药的ORR非常低(13%),因此纳武利尤单抗联合BV的疗效很可能是由生物学协同效应所介导的。
总之,帕博利珠单抗或那武利尤单抗联合 BV等检查点抑制剂方案可改善难治性疾病的极差预后,应取代挽救性化疗,并作为 CAR-T 细胞免疫疗法的桥接治疗手段。
双特异性抗体
在双特异性抗体注册研究中,有关PMBCL患者的数据有限。在epcoritamab的关键 EPCORE NHL-1 研究中,157 例患者中仅有 4例 PMBCL。在这些患者中,ORR为 100%,CR率为 50%。在格菲妥单抗2 期研究中也仅有 6 例 PMBCL 患者。
尽管接受双特异性抗体治疗的PMBCL患者数量仍较少,但现有数据颇具前景,在CAR-T免疫疗法失败的情况下,双特异性抗体仍具有潜在价值。
总结
近 80%的PMBCL病例可治愈,含蒽环类药物和利妥昔单抗的方案是一线治疗的主要手段。R-CHOP14/21、DA-EPOCH-R 和 R-V/MACOP-B 方案的长期疗效相似。然而由于缺乏对现有化疗方案进行高质量随机比较的数据,R-CHOP21 方案可能并非 PMBCL 初始治疗的最佳选择。
治疗结束时的PET扫描(Deauville评分1-3)显示完全代谢缓解与更好的生存率相关。随机IELSG37研究的最终结果表明,根据PET引导的方法,在诱导治疗后达到完全代谢缓解的患者中,可以安全地省略放疗。
在批准CAR-T疗法作为二线治疗的国家,CAR-T细胞免疫疗法目前是最佳选择。
抗PD-1抗体(如帕博利珠单抗)以及纳武利尤单抗联合维布妥昔单抗可改善难治性疾病的极差预后。在尚未将CAR-T细胞免疫疗法作为二线治疗选择的国家,这些疗法已经取代了挽救化疗,并应视为CAR-T细胞免疫疗法的桥接治疗。
最后,作者为原发性纵隔大 B 细胞淋巴瘤患者提出了治疗原则,见图 4。

参考文献
Donzelli L,et al.Primary mediastinal large B-cell Lymphoma: Biological features, clinical characteristics and current treatment strategies.Cancer Treat Rev. 2025 Feb 6:134:102898. doi: 10.1016/j.ctrv.2025.102898.


