Nat Commun 安徽医科大学谢峻团队/浙江大学徐清波团队合作开发靶向CD248的T细胞免疫疗法,精准治疗心梗后心肌纤维化
时间:2025-04-01 12:08:33 热度:37.1℃ 作者:网络
急性心肌梗死是我国致死致残的重要疾病,随着急诊介入治疗的普及,心梗急性期死亡率显著下降,但仍有大量患者因心肌纤维化进展为心力衰竭,面临生活质量下降和预后不良的困境。成纤维细胞在疤痕成熟后的异常活化是心梗后组织修复障碍的关键病因。传统药物治疗仅能延缓症状,无法逆转纤维化进程;而靶向成纤维细胞活化蛋白(FAP)的CAR-T疗法因对成纤维细胞的无差别攻击,可能破坏疤痕的形成和稳定,临床安全性存疑。如何精准干预致病成纤维细胞,成为治疗心梗后心肌纤维化亟待突破的瓶颈。
2025年3月27日,安徽医科大学第一附属医院谢峻教授团队、浙江大学医学院附属第一医院徐清波教授团队合作在Nature Communications发表了题为“CD248-targeted BBIR-T cell therapy against late-activated fibroblasts in cardiac repair after myocardial infarction”的文章,筛选并鉴定出心梗后组织修复过程中的关键致病成纤维细胞F-Act亚群及其特征性表面抗原CD248,开发靶向CD248的生物可控型生物素结合免疫受体(BBIR) T细胞免疫疗法,于心梗疤痕成熟后精准清除损伤心肌中的F-Act亚群,有效抑制心肌纤维化扩张,改善心室重构并延缓心功能的恶化。

本研究通过整合单细胞RNA测序(scRNA-seq)与空间转录组测序(stereo-seq)技术,系统解析小鼠梗死心脏间质细胞,成功鉴定出具有显著致病特征的成纤维细胞亚群—F-Act。在心梗疤痕成熟后,F-Act亚群在梗死周围区聚集和活化,驱动病理性纤维化扩张和组织修复障碍。研究确定跨膜糖蛋白CD248作为F-Act亚群的特异性分子标志物,其正常成年组织中呈低表达,而在心梗后的F-Act亚群中特异性高表达,这一特性使其成为CAR-T细胞治疗的理想靶点,可有效降低脱靶效应风险。值得关注的是,在人类缺血性心肌病患者的心脏组织中也能观察到CD248阳性细胞,该跨物种保守性特征为靶向CD248的抗纤维化治疗策略提供了关键转化医学证据,提示通过干预F-Act亚群活性调控心脏重构进程的可行性。
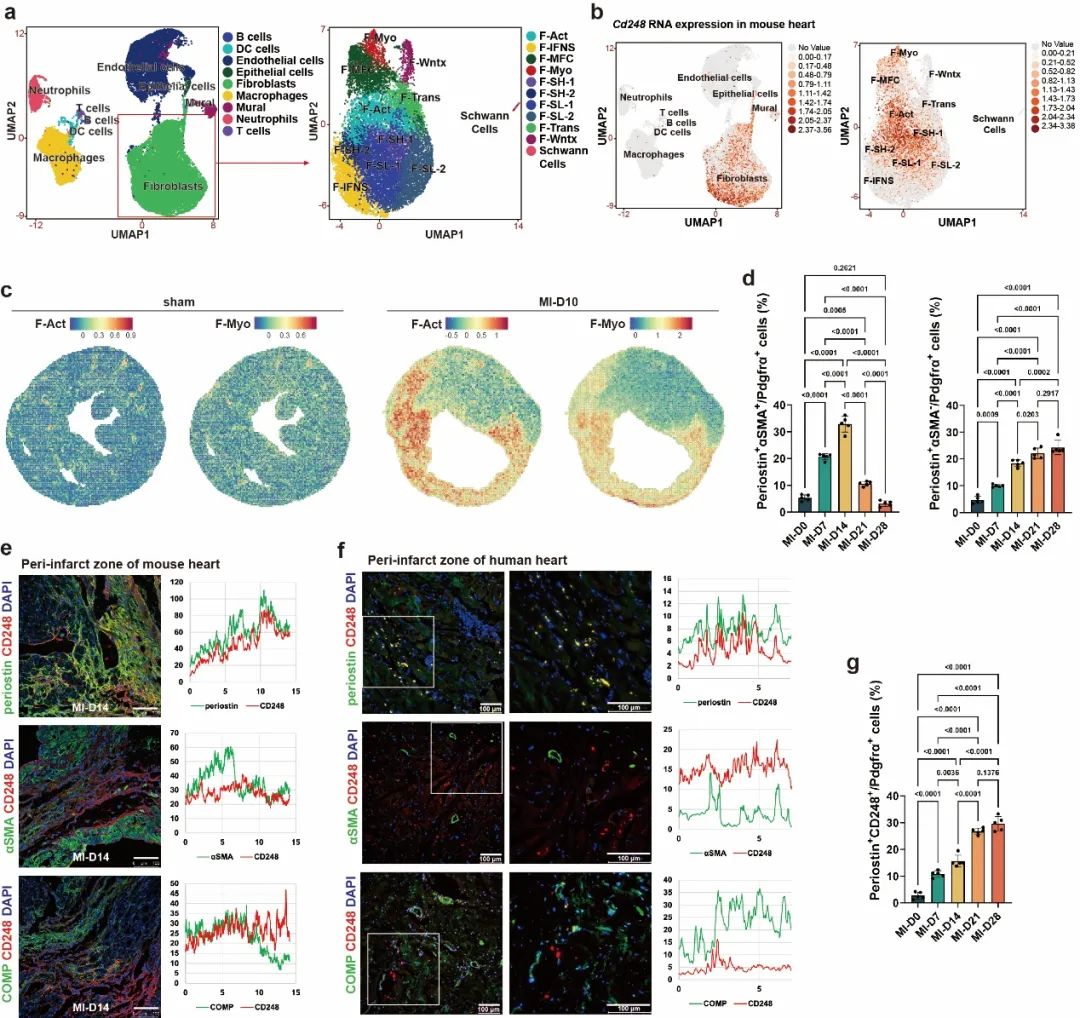
基于以上发现,研究团队创新性地开发了靶向CD248的BBIR-T细胞免疫疗法。通过将双链亲和素(dcAv)与T细胞信号转导结构域偶联构建BBIR-T细胞,利用“生物素-亲和素”的分子开关实现精准靶向。治疗策略采用两步法:首先在心梗后即刻心肌内注射生物素化抗CD248 F(ab')2,标记损伤心肌中的CD248阳性细胞;待梗死疤痕成熟后,静脉输注BBIR-T细胞,使其精准募集至损伤部位并清除F-Act亚群。体外实验证实,该疗法可选择性清除CD248阳性细胞而不损伤阴性细胞。在小鼠心梗模型中,该疗法可清除至少2/3的靶细胞,显著抑制纤维化扩张和心肌细胞肥大,改善心室重构和心功能,且未引发细胞因子风暴或其他器官损害。
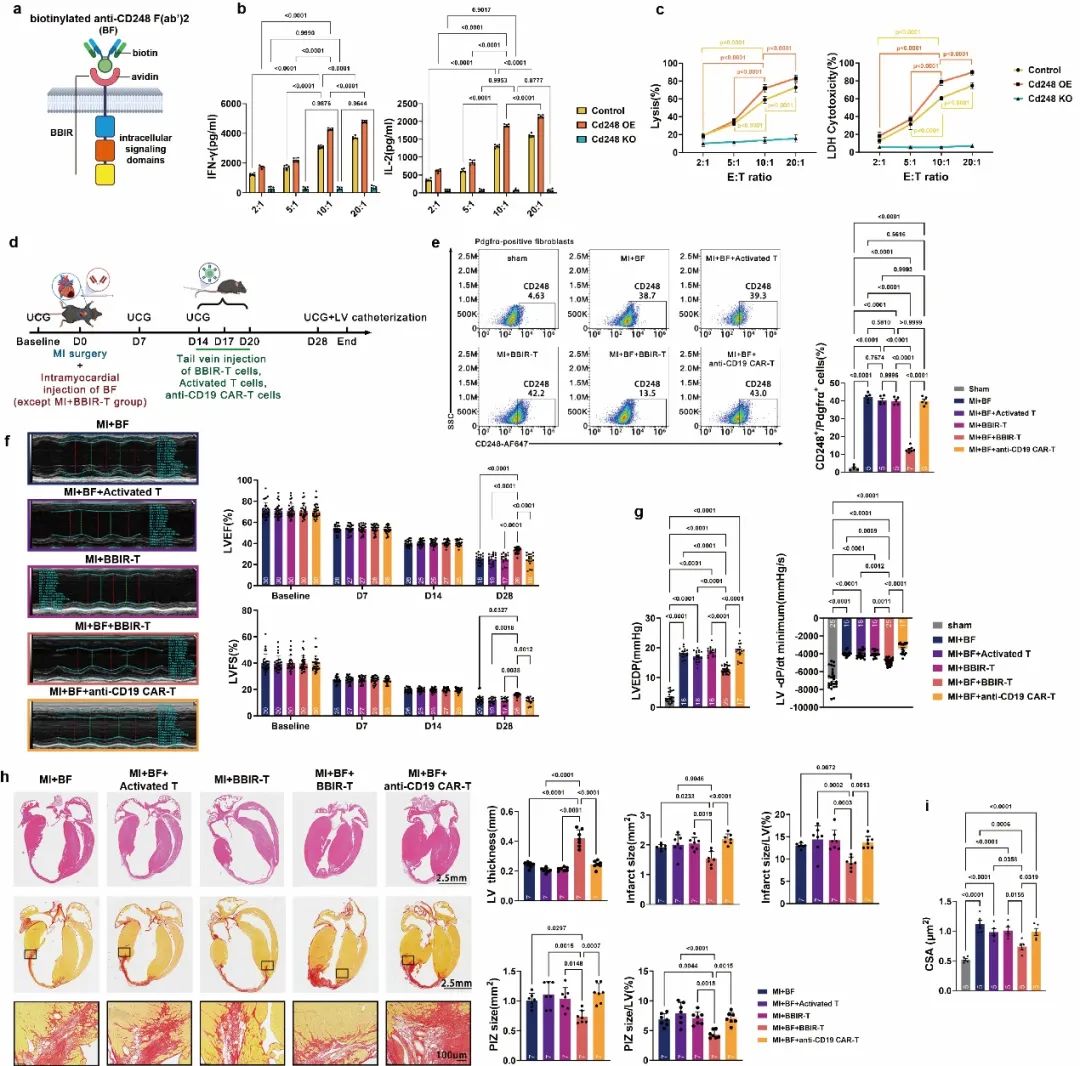
综上,该方案创新性地实现了在特定时间(瘢痕成熟期)对特定部位(损伤心肌)的特定细胞群(F-Act亚群)的精准干预,突破传统抗纤维化治疗的非特异性局限,为心肌修复提供了时空调控的靶向治疗范式。
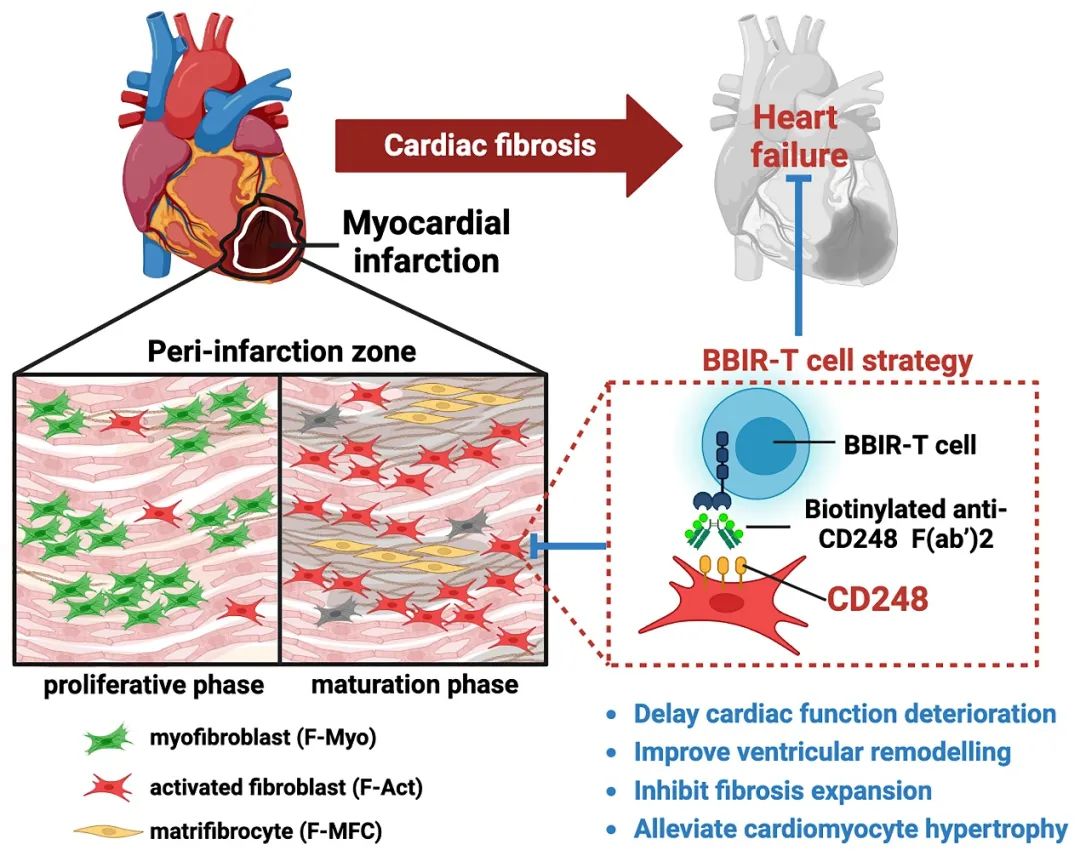
安徽医科大学第一附属医院/北京安贞医院安徽医院谢峻教授、浙江大学医学院附属第一医院徐清波教授为本文共同通讯作者,安徽医科大学第一附属医院/北京安贞医院安徽医院陈海婷博士、胡柯硕士以及南京医科大学“国家卫健委抗体技术重点实验室”唐奇副研究员为本文共同第一作者。该研究工作得到了国家自然科学基金重大研发计划、江苏省杰出青年基金、中央高校基金等项目的资助。
原文链接:
https://www.nature.com/articles/s41467-025-56703-2


