肝星状细胞激活和MASH纤维化
时间:2025-02-28 12:12:08 热度:37.1℃ 作者:网络
【导语】
肝纤维化是MASH患者死亡率和不良肝脏事件的主要预测因素。静息肝星状细胞(HSC)被激活转变为肌成纤维细胞,进而分泌大量细胞外基质,导致肝脏纤维化瘢痕形成,是其主要发病机制。因此,抑制HSC活化对于预防和减少MASH纤维化至关重要。
“脂肪肝学苑”第36期,特别推荐美国加州大学Jerrold M. Olefsky团队2024年5月在Cell Metabolism期刊发表的一项研究“TM7SF3 controls TEAD1 splicing to prevent MASH-induced liver fibrosis”。该研究提出了一种全新的TM7SF3-hnRNPU-TEAD1信号通路通过调控TEAD1剪接在HSC激活和MASH相关纤维化中的作用,并展示了使用特定反义寡核苷酸(ASO)干预的潜在应用,为慢性肝病的治疗提供了新思路。
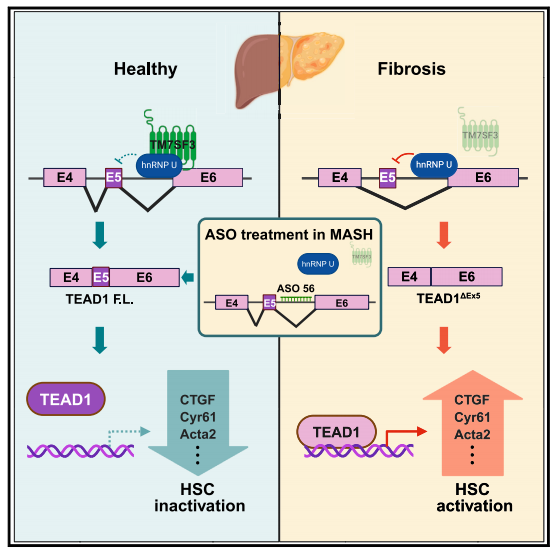
全文地址:https://pubmed.ncbi.nlm.nih.gov/38670107/
· 研究背景 ·
Hippo信号通路和TEAD1与炎症、纤维化和癌症等多种疾病密切相关。然而,TEAD1在HSC中的作用尚未深入研究。本研究通过揭示核内七跨膜蛋白TM7SF3对TEAD1剪接的调控机制,探索其在MASH诱导的肝纤维化中的关键作用。
· 研究结果 ·
1. TM7SF3缺失促进HSC活化和纤维化
研究者发现,U2-OS细胞中TM7SF3敲低(KD)导致基因表达谱与肝纤维化/HSC激活谱高度相似。CCl4处理或MASH饮食诱导的活化HSC中,Tm7sf3 mRNA表达降低(图1A)。构建肝脏类器官模型,使用脂肪酸混合物模拟MASH过程,发现TM7SF3 KO-HSC的纤维化和炎症相关基因(如Tgfb1、Col1a1、Timp1和Mcp1)及ECM蛋白表达显著增加(图1C-E)。siRNA沉默小鼠和人原代HSC中的Tm7sf3基因后,纤维化基因表达显著升高(图1F-G),HSC增殖增加(图1H-I)。结果表明,TM7SF3抑制HSC的活化,减少纤维化和炎症。
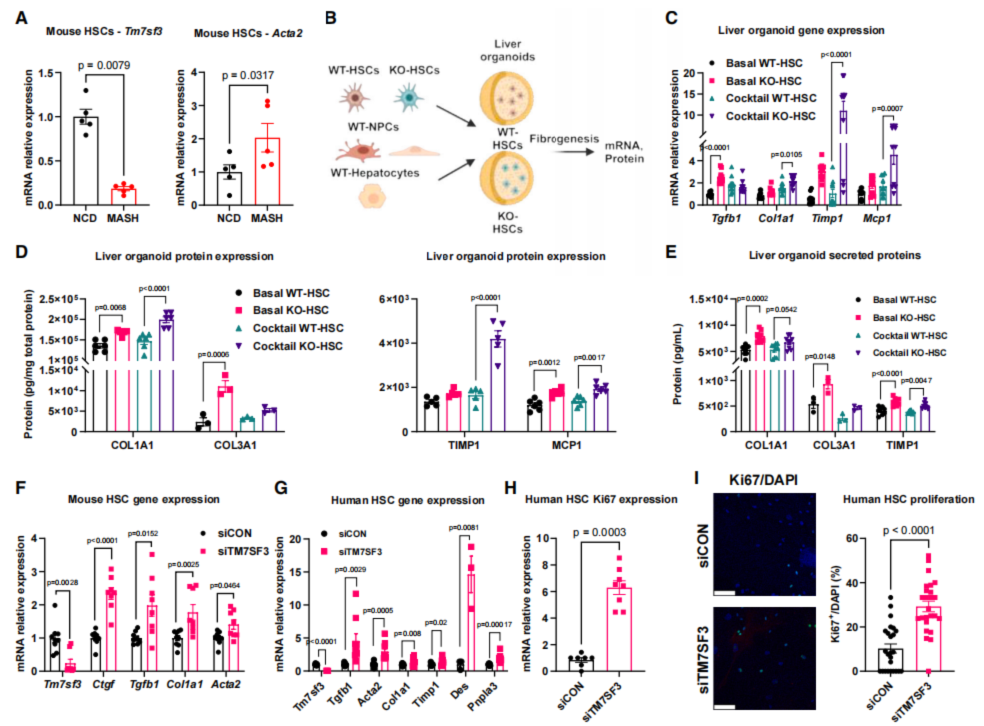
图1 TM7SF3 KO通过促进HSC活化和细胞增殖诱导肝脏类器官和HSC的纤维化
2. HSC特异性TM7SF3敲除加重MASH诱导的肝纤维化
为进一步评估TM7SF3 KO对HSC活化和肝纤维化的影响,研究者构建HSC特异性TM7SF3敲除小鼠(HSC-TM7SF3KO),西方饮食(WD)喂养6周后,HSC-TM7SF3KO小鼠肝脏羟脯氨酸含量升高;16周后,α-SMA免疫染色和COL1A1、TIMP1蛋白表达显著增加(图2A-C),炎症标志物表达升高(图2D-E),血清ALT水平显著上升(图2F)。TM7SF3缺失加重了MASH诱导的肝纤维化。
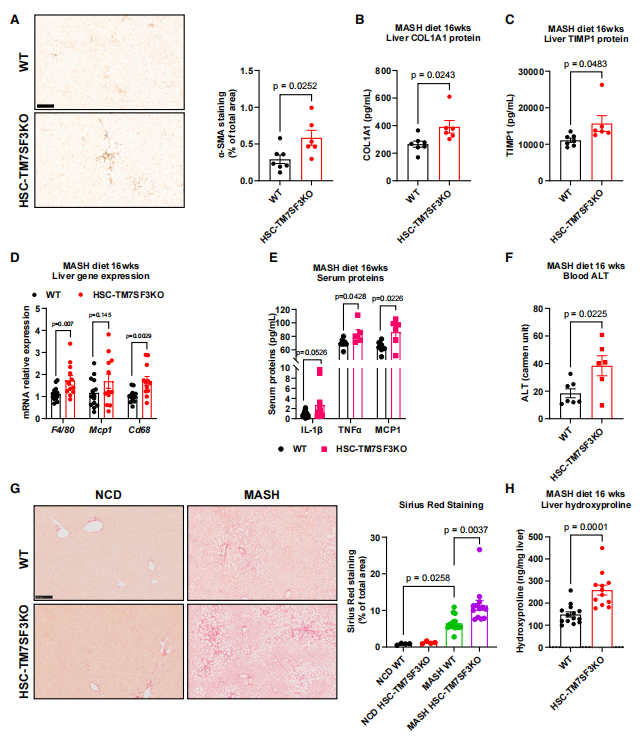
图2 HSC特异性TM7SF3 KO加重MASH诱导的肝纤维化
3. TM7SF3通过调控TEAD1剪接调节HSC活化
TEAD1在肝损伤后会发生选择性剪接(AS),从而调节其活性。研究发现,MASH患者肝脏中TEAD1表达显著升高(图3A),MASH小鼠HSC中TEAD1选择性剪接(AS)增加(图3B)。TM7SF3 KD促进TEAD1外显子5跳跃,产生更活跃的TEAD1△Ex5形式(图3C-D)。设计siRNA抑制外显子5跳跃(siTEAD1△Ex5),显著降低了TEAD1靶基因(如Ctgf和Cyr61)及HSC活化标志物(如ACTA2和Il-6)的表达(图3F-K)。在肝脏类器官中,siTEAD1△Ex5显著降低纤维化基因和蛋白表达(图3L-M)。TM7SF3通过调控TEAD1剪接抑制HSC活化。
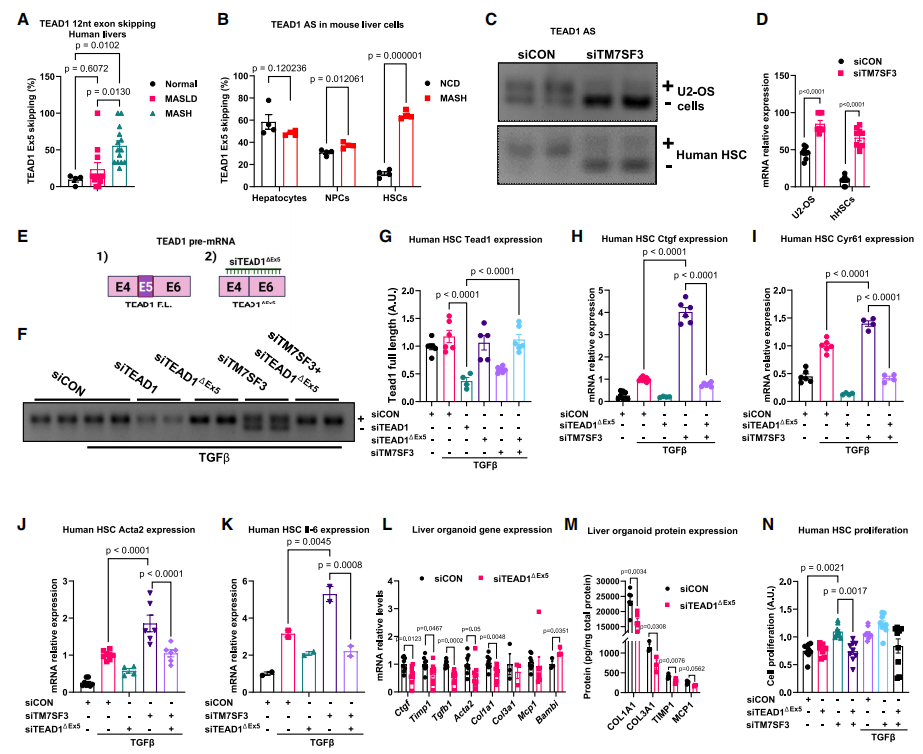
图3 TM7SF3通过调节TEAD1选择性剪接来调节HSC活化
4. TM7SF3通过hnRNPU调控TEAD1剪接
AS的调节通常是通过剪接因子与前体mRNA序列的相互作用来实现的。为鉴定TM7SF3 KD诱导TEAD1 AS的直接作用剪接因子,研究者分析与TM7SF3结合的蛋白质列表,寻找可能含有位于TEAD1外显子5上游或下游100 bp的RNA结合基序序列的剪接因子。异质核核糖核蛋白U(hnRNPU)是唯一具有接近TEAD1外显子5邻近结合基序的剪接因子。RNA免疫沉淀(RIP)实验显示,hnRNPU与TEAD1前体mRNA结合,促进外显子5跳跃(图4A-E)。hnRNPU KD降低了TM7SF3 KD诱导的TEAD1剪接活性(图4F-G),并抑制HSC活化(图4H-I)。TM7SF3通过hnRNPU调控TEAD1剪接,抑制HSC活化。
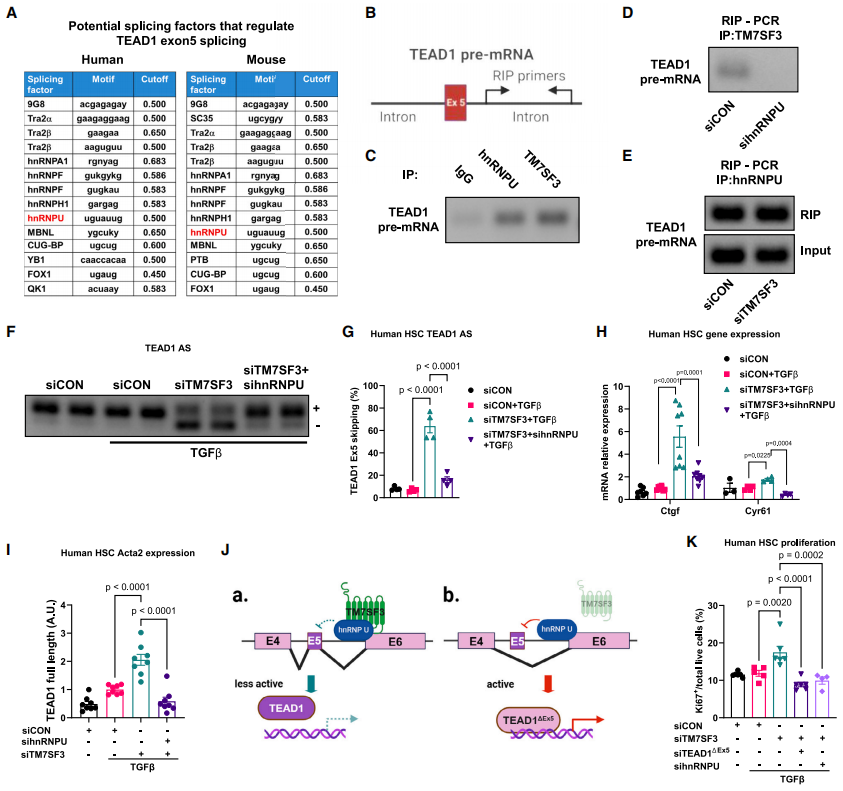
图4 TM7SF3通过结合hnRNPU剪接因子抑制TEAD1选择性剪接
5. 靶向TEAD1前体mRNA的ASO抑制HSC活化
为进一步评估TEAD1 AS对HSC活化和MASH进展的影响,研究者设计ASO 56靶向hnRNPU结合基序,可显著降低TGFβ处理的HSC中TEAD1△Ex5及纤维化基因(如TGFB1、ACTA2、TIMP1)的表达(图5B)。在肝脏类器官中,ASO 56抑制了纤维化基因和蛋白表达(图5C-E)。小鼠体内实验显示,ASO 56减少了HSC中TEAD1△Ex5的表达(图5F),并抑制了Acta2和Col1a1的表达(图5H)。ASO 56通过抑制TEAD1剪接减少HSC活化。
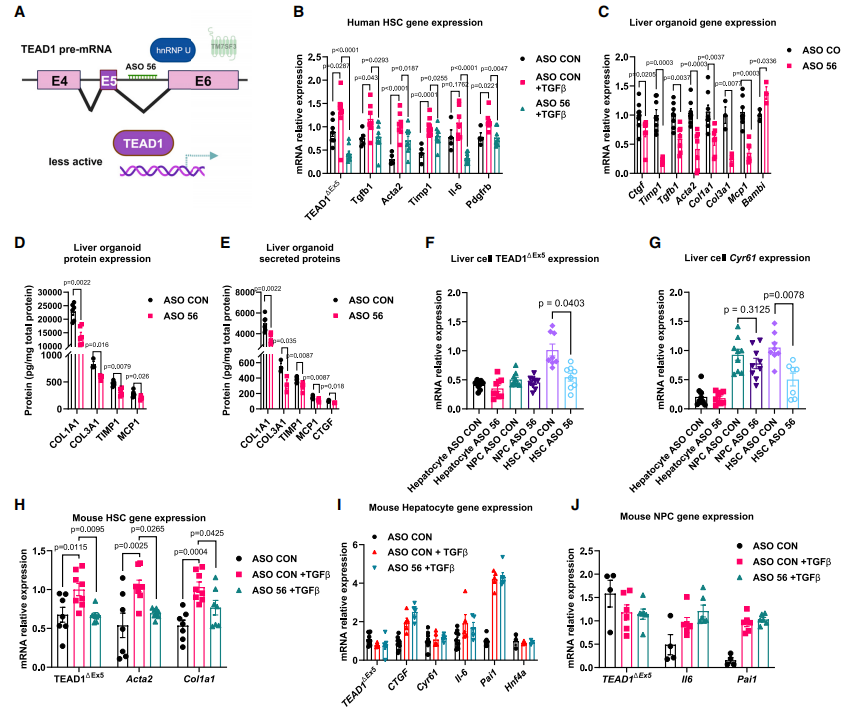
图5 靶向TEAD1前体mRNA的ASO使HSC失活
6. ASO 56改善MASH小鼠表型
最后,研究者评估ASO 56体内改善小鼠MASH表型的能力。ASO 56降低了MASH小鼠肝脏中Ctgf和Birc5的表达(图6B-D),减少了炎症因子和纤维化水平(图6E-F),降低了血清ALT水平(图6J),并减少了肝细胞衰老(图6K)。天狼星红染色和羟脯氨酸含量测量显示,ASO 56显著降低了胶原蛋白沉积(图6L-M)。ASO 56通过抑制HSC活化改善MASH表型。
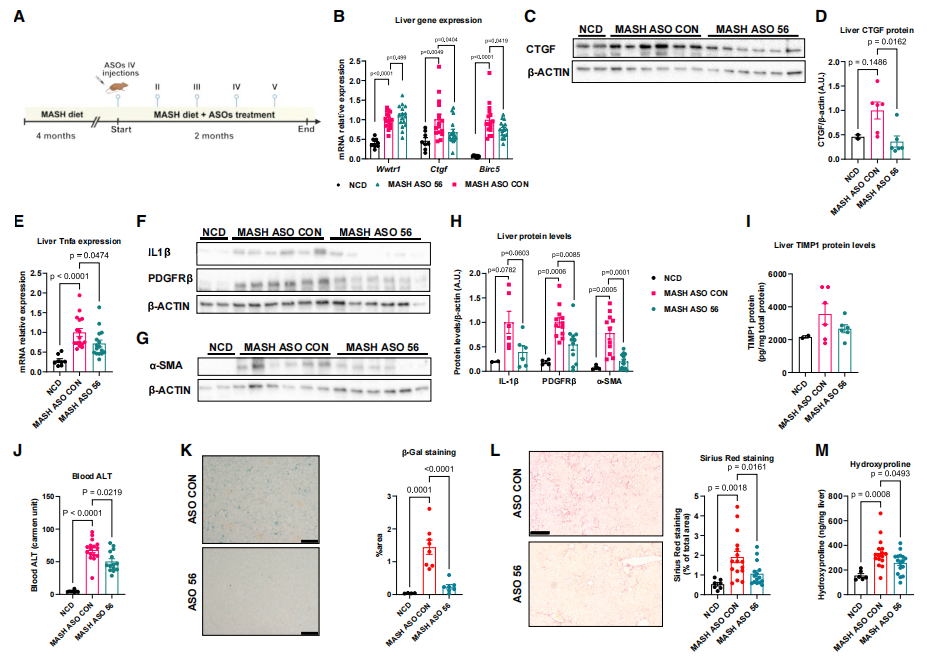
图6 靶向TEAD1前体mRNA的ASO体内促使HSC失活
· 研究结论 ·
本研究揭示了TM7SF3通过hnRNPU调控TEAD1剪接,抑制HSC活化和MASH相关纤维化的新机制。TM7SF3缺失导致TEAD1外显子5跳跃,产生更活跃的TEAD1△Ex5形式,加速HSC活化和纤维化。靶向TEAD1前体mRNA的ASO疗法在抑制HSC活化和改善MASH表型方面展现出潜在应用价值,为MASH诱导的肝纤维化治疗提供了新策略。


