JAMA:瑞莎珠单抗治疗溃疡性结肠炎
时间:2025-02-19 12:08:45 热度:37.1℃ 作者:网络
溃疡性结肠炎是一种慢性、免疫介导的炎症性肠病,与腹泻、直肠出血和肠急症有关。溃疡性结肠炎症状与生活质量下降、社会和心理功能受损以及卫生保健费用增加有关。目前的治疗方法,包括皮质类固醇和免疫调节剂,由于缺乏初始反应、反应丧失和潜在的不良事件(如感染或恶性肿瘤风险增加)而受到限制。肿瘤坏死因子抑制剂,如英夫利昔单抗和阿达木单抗,是溃疡性结肠炎的一线治疗药物;然而,大约三分之一的患者对肿瘤坏死因子抑制剂的初始治疗没有反应。细胞因子IL-23与肠道炎症和溃疡性结肠炎的发病有关,它刺激炎症细胞群的增殖,并支持其他细胞因子的激活。瑞莎珠单抗(一种选择性靶向IL-23 p19亚基的单克隆抗体)用于治疗溃疡性结肠炎的临床效果尚不明确。这项研究评估了瑞莎珠单抗作为诱导和维持治疗对溃疡性结肠炎患者的疗效和安全性。

诱导试验在41个国家的261个临床中心进行,从2020年11月5日至2022年8月4日招募了977名患者(最终随访时间为2023年5月16日)。维持试验在37个国家的238个临床中心进行,从2018年8月28日至2022年3月30日招募了754名患者(最终随访时间为2023年4月11日)。符合条件的患者为中重度活动性溃疡性结肠炎患者;对1种或多种常规疗法、先进疗法或两种疗法均存在不耐受或反应不足的病史;且既往未接受过瑞莎珠单抗治疗。在诱导试验中,患者按2:1的比例随机分配接受1200 mg瑞莎珠单抗或安慰剂,分别在第0、4和8周静脉注射。在维持试验中,静脉注射瑞莎珠单抗后出现临床反应(根据改良Mayo评分确定)的患者按1:1:1的比例随机分配接受180 mg或360 mg瑞莎珠单抗或安慰剂(不再接受瑞莎珠单抗)皮下治疗,每8周一次,持续52周。主要结局为诱导试验第12周和维持试验第52周的临床缓解(排便频率评分≤1且不高于基线,直肠出血评分为0,内镜评分≤1且无脆性)。
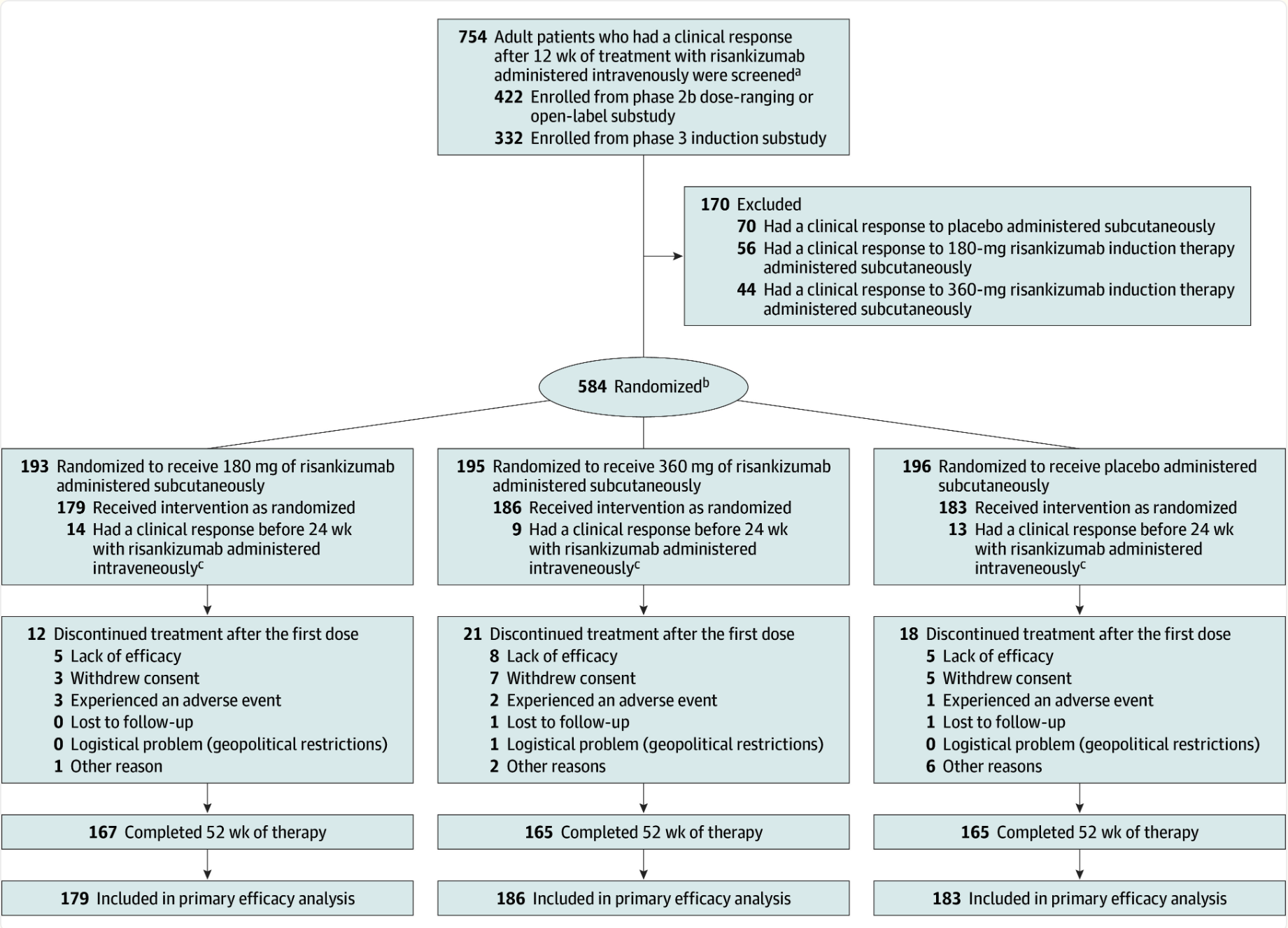
在诱导试验中分析的975名患者中,第12周的临床缓解率为1200 mg瑞莎珠单抗组132/650(20.3%)和安慰剂组20/325(6.2%)。在维持试验中分析的548名患者中,第52周的临床缓解率为180 mg瑞莎珠单抗组72/179(40.2%)、360 mg瑞莎珠单抗组70/186(37.6%)和安慰剂组46/183(25.1%)(180 mg瑞莎珠单抗组与安慰剂组的组间调整差异为16.3%;360 mg瑞莎珠单抗组与安慰剂组的组间调整差异为14.2%。治疗组中未发现新的安全风险。
这项研究的结果表明,与安慰剂相比,瑞莎珠单抗在中重度活动性溃疡性结肠炎患者的诱导试验和维持试验中提高了临床缓解率。需要进一步研究以确定52周随访后的获益。
原文出处:
Louis E, Schreiber S, Panaccione R, Bossuyt P, Biedermann L, Colombel JF, Parkes G, Peyrin-Biroulet L, D'Haens G, Hisamatsu T, Siegmund B, Wu K, Boland BS, Melmed GY, Armuzzi A, Levine P, Kalabic J, Chen S, Cheng L, Shu L, Duan WR, Pivorunas V, Sanchez Gonzalez Y, D'Cunha R, Neimark E, Wallace K, Atreya R, Ferrante M, Loftus EV Jr; INSPIRE and COMMAND Study Group. Risankizumab for Ulcerative Colitis: Two Randomized Clinical Trials. JAMA. 2024 Sep 17;332(11):881-897. doi: 10.1001/jama.2024.12414. Erratum in: JAMA. 2024 Nov 19;332(19):1676. doi: 10.1001/jama.2024.21794. PMID: 39037800; PMCID: PMC11264075.


