神奇发现!中国药大揭示人参皂苷如何通过肠道菌群和催产素信号改善抑郁症状
时间:2024-12-08 20:01:35 热度:37.1℃ 作者:网络
抑郁症是一种全球范围内广泛存在的精神障碍,该病发病率持续攀升,成因复杂,通常涉及社会心理、环境及遗传因素的相互作用。此外,胃肠道的紊乱可能引发肠-脑轴的代谢、免疫和神经异常,这些因素与抑郁症的发病机制存在因果联系。然而,现行的抗抑郁药物并未专门针对这些系统性信号。因此,在探索新的治疗靶点和方法时,必须考虑大脑定位以及调节抑郁症相关行为表现的系统性机制。
人参自古以来即被广泛应用于多种传统抗抑郁药方,人参及其相关制品被普遍采纳为促进精神健康之药物成分及营养补充剂。尽管人参皂苷作为主要活性成分已广为人知,但其抗抑郁作用的具体机制可能涉及多种成分,目前尚未完全明了。
近日,一篇名为“Ginsenoside Rg1 enriches gut microbial indole-3-acetic acid to alleviate depression-like behavior in mice via oxytocin signaling”的论文从肠道微生物到大脑信号传导的角度阐明人参皂苷Rg1(Rg1)的抗抑郁机制。

图1 论文首页
Rg1在不可预知温和应激小鼠中产生抗抑郁作用
该研究探讨了低剂量与高剂量Rg1(分别为20mg/kg和40mg/kg)在已建立的UMS抑郁模型中的作用(图2B)。Rg1给药14天后埋珠实验(MBT)结果显示,与UMS组相比,低剂量和高剂量Rg1组(20mg/kg和40mg/kg)的埋珠数量显著减少(图2C)。此外,在悬尾实验(TST)和强迫游泳(FST)中,UMS组的不动时间有所增加,而Rg1则有效减少了这一时间(图2D,E)。在社交互动测试(SIT)中,Rg1以剂量依赖的方式改善了UMS小鼠的社交回避行为(图2F)。这些数据共同证明,Rg1能够改善UMS小鼠的行为异常,尤其是社交回避行为。
神经发生障碍是抑郁症的一个典型特征。研究进一步发现UMS小鼠海马齿状回(DG)中双皮层蛋白(DCX)阳性细胞的数量显著减少,而Rg1显著逆转了这一变化(图2G,H)。因此,研究进一步研究了Rg1对海马神经营养因子的影响,发现UMS模型降低了Gdnf和Ngf的表达,但Rg1处理对这两个因素没有显著影响(图2I)。研究还比较了海马突触蛋白的mRNA表达。UMS模型降低了GluA2和CamkIIα的表达,而Rg1有效地逆转了CamkIIβ的减少(图2J)。综上所述,Rg1对UMS小鼠的抗抑郁作用伴随着海马神经可塑性的改善。
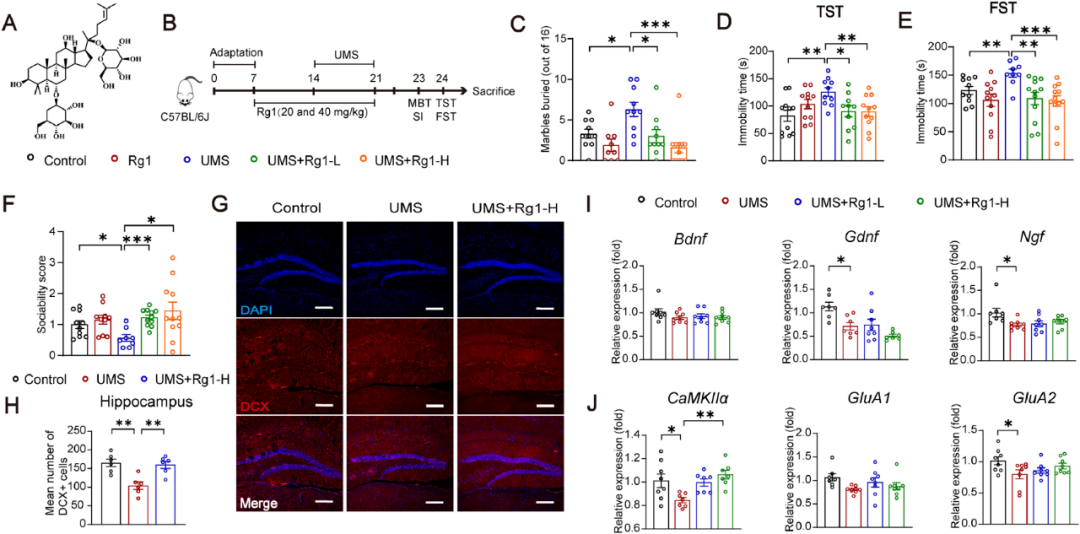
图2 Rg1对UMS小鼠产生抗抑郁作用
Rg1选择性地增加血清和脑组织中的IAA水平
该研究对血清进行了非靶向代谢组学分析,旨在识别潜在的肠脑信号。结果显示,UMS与Rg1处理组之间存在多种代谢物差异(图3A)。通路富集分析揭示,Rg1诱导了代谢途径的转变,主要涉及不饱和脂肪酸合成及色氨酸(Trp)代谢(图3B)。色氨酸由宿主与肠道微生物共同代谢,产生多种信号代谢物,这些代谢物已被证实为肠脑相互作用及行为调节的关键因素。为深入探讨人参皂苷与肠道微生物组的相互作用,研究采用一种经过验证的方法对色氨酸代谢途径进行了靶向分析。结果显示,在USM小鼠血清中,细菌衍生的吲哚代谢物,包括IAA(脑吲哚-3-乙酸)、IAld(吲哚-3-甲醛)、ILA(吲哚-3-乳酸)、IA(吲哚-3-丙烯酸)、IPA(吲哚-3-丙酸)显著减少。Rg1持续提升血清及海马中的IAA水平,并在下丘脑中呈现上升趋势(图3C-I),这暗示IAA水平的调节可能是Rg1作用机制的关键环节。
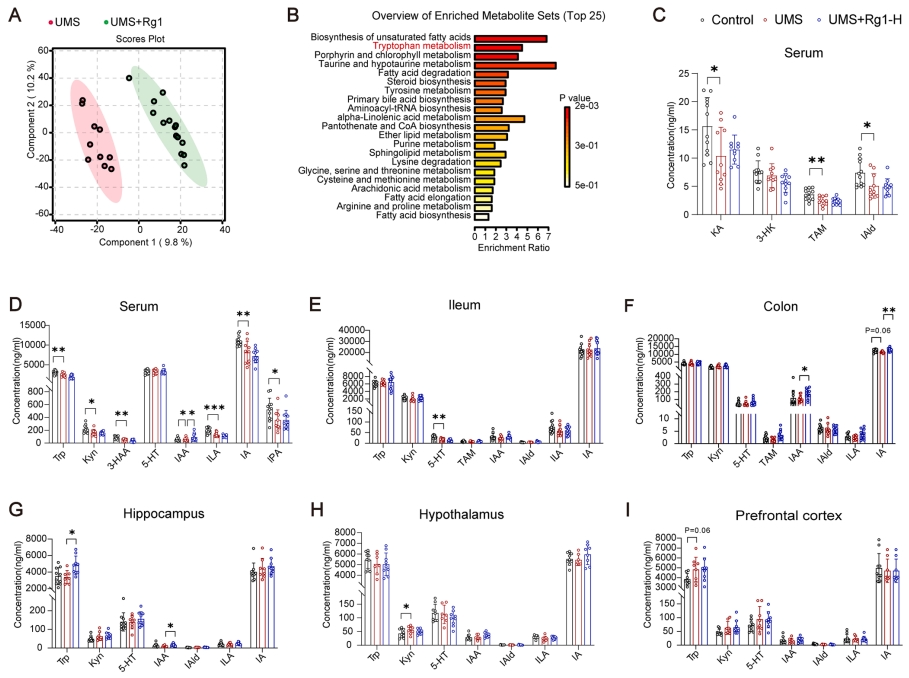
图3 Rg1通过细菌色氨酸代谢途径增加IAA
催产素信号介导Rg1的抗抑郁作用
研究旨在探究OXT信号是否参与了Rg1的抗抑郁效应。在UMS小鼠的室旁核(PVN)中,OXT阳性细胞的数量显著减少,而高剂量的Rg1显著恢复了该区域的OXT阳性细胞数量(图4A,B)。这一发现暗示Rg1可能通过影响UMS小鼠下丘脑-海马OXT信号来发挥其抗抑郁作用。为进一步探究这一作用的功能相关性,研究采用了可穿透血脑屏障的OXTR抑制剂L-368899来阻断OXT信号传导(图4C)。
在开放场测试(OFT)中,L-368899逆转了高剂量Rg1在UMS小鼠中引起的中心区域进入和停留时间的增加(图4D,E)。与仅接受Rg1处理的组相比,经过OXTR抑制剂处理后,小鼠埋藏的珠子数量显著增加(图4F),表明Rg1对小鼠社交回避行为的缓解作用被消除(图4G)。在TST和FST测试中,OXTR抑制剂同样消除了Rg1对UMS小鼠静止时间的保护作用(图4H,I)。综合上述结果,研究指出Rg1的抗抑郁机制在功能上依赖于OXT信号传导。
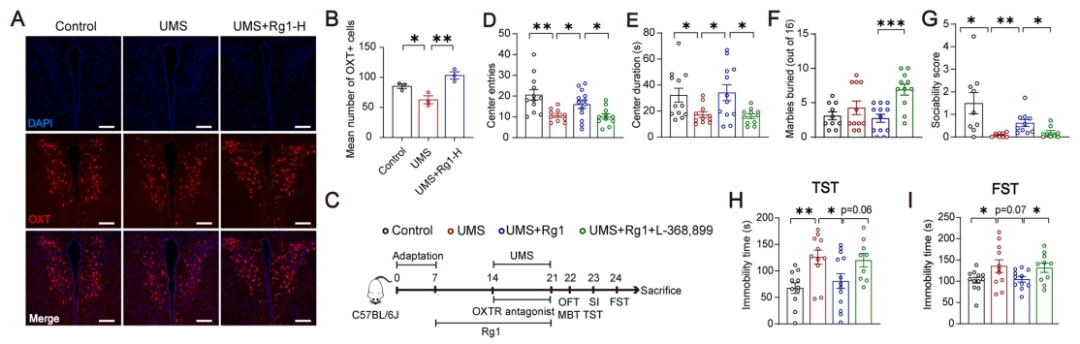
图4 下丘脑中的催产素信号介导Rg1的抗抑郁作用
IAA对UMS小鼠产生抗抑郁作用
通过生物分布的测定,研究观察到口服IAA后,该物质在小鼠海马和下丘脑等脑区有良好的分布(图5A),这提升了Rg1调节的微生物IAA可能通过脑部作用影响行为的假设。为了进一步验证这一假设,研究对UMS小鼠进行了IAA的口服处理,并对其行为结果进行了检测(图5B)。结果正如预期,IAA显著提升了UMS小鼠在开放场测试(OFT)中进入中心区域的次数及停留时间(图5C、D)。在MBT中,与UMS组相比,IAA处理组的埋藏珠子数量明显减少(图5E)。此外,IAA显著改善了UMS小鼠的社交回避行为(图5F),并缩短了小鼠在TST和FST中的不动时间(图5G、H)。这表明IAA对小鼠具有直接的抗抑郁效果。
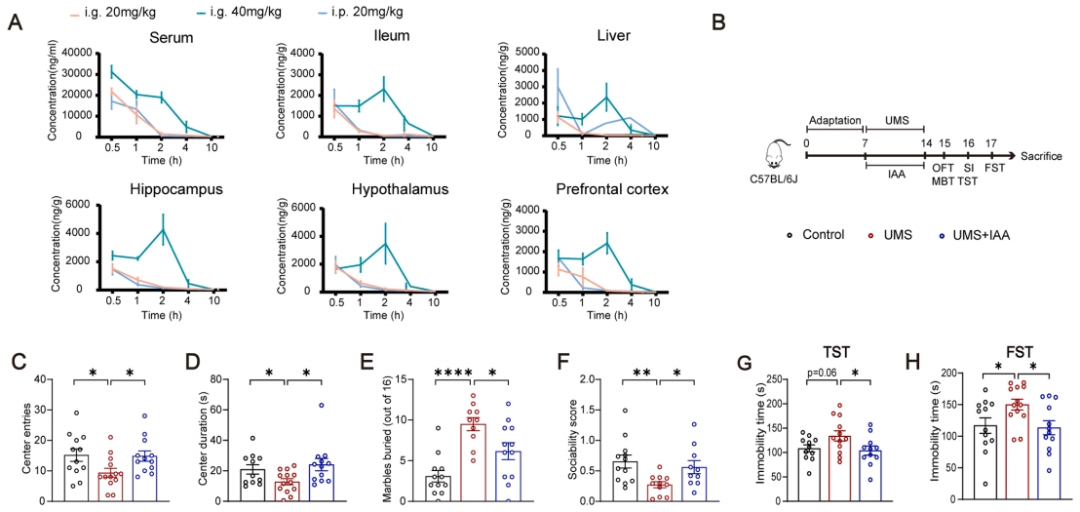
图5 IAA对UMS小鼠具有抗抑郁作用
IAA通过催产素信号发挥抗抑郁作用
研究进一步探讨了催产素信号是否对IAA的作用至关重要;为此,在应用IAA之前,预先给予了催产素受体抑制剂L-368,899(图6A)。结果显示,与Rg1的效果类似,IAA对大脑中催产素阳性神经元具有保护作用,这包括在下丘脑室旁核(PVN)中催产素表达的显著恢复(图6B-C),以及在海马区中双皮质素阳性细胞数量的显著增加(图6D-E)。L-368,899逆转了IAA对催产素信号传导的保护作用,并且阻断了IAA对OFT测试(图6F,G)、SIT测试(图6H)、TST测试(图6I)和FST测试(图6E)中抑郁样行为的改善作用。这些结果表明下丘脑-海马催产素信号传导在IAA的抗抑郁作用中扮演了关键角色。
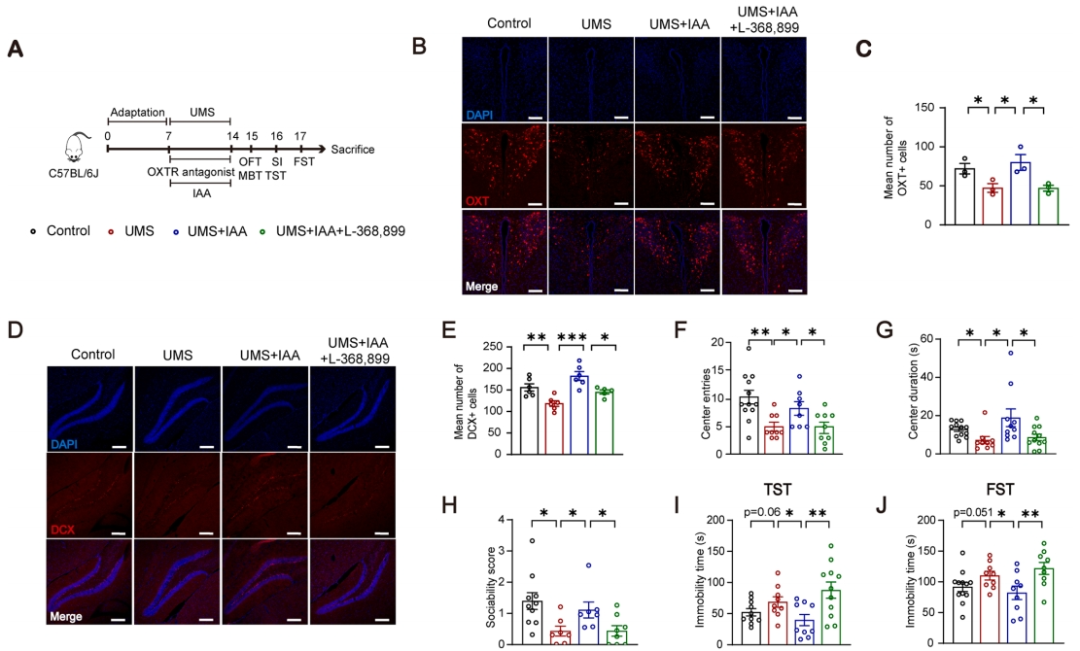
图6 IAA以催产素受体依赖的方式产生抗抑郁作用
结论
总之,该研究揭示了Rg1抗抑郁效应一种新的肠道-大脑轴机制,亦加深了对微生物群与行为之间代谢信号联系的理解,并为通过肠道-大脑相互作用产生抗抑郁效果提供了新的潜在治疗途径。
参考文献:
Yu S, Yin Z, Ling M, Chen Z, Zhang Y, Pan Y, Zhang Y, Cai X, Chen Z, Hao H, Zheng X. Ginsenoside Rg1 enriches gut microbial indole-3-acetic acid to alleviate depression-like behavior in mice via oxytocin signaling. Phytomedicine. 2024 Dec;135:156186. doi: 10.1016/j.phymed.2024.156186


