EMM:天津医科大学张丽荣等团队发现常染色体显性遗传性多囊肾病的潜在治疗新策略
时间:2024-11-27 12:01:08 热度:37.1℃ 作者:网络
黑色素样纳米颗粒(MNP)因其出色的生物相容性和清除各种活性氧(ROS)的能力,成为有效的抗氧化治疗药物。然而,已有研究主要集中在急性ROS相关疾病上,仍不清楚其在慢性病中的治疗潜力。此外,除了其公认的抗氧化作用外,尚未探索MNP是否靶向其他细胞内分子途径。
2024年11月20日,天津医科大学张丽荣、孙少凯、陈宇鹏共同通讯在EMBO Molecular Medicine 在线发表题为 “Melanin-like nanoparticles slow cyst growth in ADPKD by dual inhibition of oxidative stress and CREB” 的研究论文,该研究合成了Mn2+螯合的的超小聚乙二醇MNP(MMPP),发现MMPP穿过肾小球滤过屏障,并特异性地积聚在肾小管中。
常染色体显性遗传性多囊肾病(ADPKD)是一种慢性遗传性疾病,与氧化应激增加密切相关,其特征是肾小管各个节段的囊肿进行性增大。MMPP治疗显著减轻了氧化应激水平,抑制了囊肿生长,从而改善了肾功能。有趣的是,我们发现MMPP有效抑制cAMP-CREB通路下游的囊肿促进基因,这是与ADPKD进展有关的关键信号通路。从机制上讲, MMPP直接与CREB的bZIPDNA结合结构域结合,导致CREB的DNA结合竞争性抑制,随后CREB靶基因表达降低。总之,该研究确定了MMPP的细胞内靶标,并通过同时靶向氧化应激和CREB转录活性证明了其治疗ADPKD的潜力。

常染色体显性遗传性多囊肾病(ADPKD)是一种危及生命的单基因疾病,影响着全球超过1200万人。ADPKD主要由PKD1或PKD2基因突变引起,PKD1或PKD2基因编码多囊蛋白1或多囊蛋白2。疾病特征是肾脏中充满液体的囊肿数量增加,随着时间的推移而扩大,导致肾功能进行性下降,超过50%的患者在60岁时发生肾功能衰竭。
最近的研究表明,信号通路异常与ADPKD进展有关,包括环磷酸腺苷(cAMP)水平异常升高、活性氧(ROS)积累、细胞内钙失衡、细胞复杂性和RNA异常。cAMP可以结合并激活PKA激酶活性,从而磷酸化CREB等底物。磷酸化的CREB与其靶基因上的CRE序列结合并激活其表达。有研究发现,抑制CREB可减少体外囊肿扩张。该团队已有研究发现CREB靶基因在囊性上皮细胞中的表达与ADPKD的进展有关。此外,抑制CREB转录活性有效抑制了体内囊肿生长。上述研究强调了靶向抑制cAMP-CREB通路是治疗ADPKD的潜在策略。
ADPKD的另一个关键特征是线粒体功能障碍和ROS过度积累。ROS稳态对于维持生理细胞功能至关重要。然而,过高的ROS水平可能对细胞有害。线粒体是ROS生产和清除的主要场所。线粒体功能障碍会导致ROS过度积累,从而诱导氧化应激和损伤细胞。该团队已有研究已经确定了ADPKD患者肾脏中ROS水平与疾病严重程度之间的正相关关系。此外,作者发现激活抗氧化转录因子Nrf2可以有效降低ROS水平,延迟ADPKD进展。上述发现表明,提高ROS清除率有望减缓ADPKD进展。
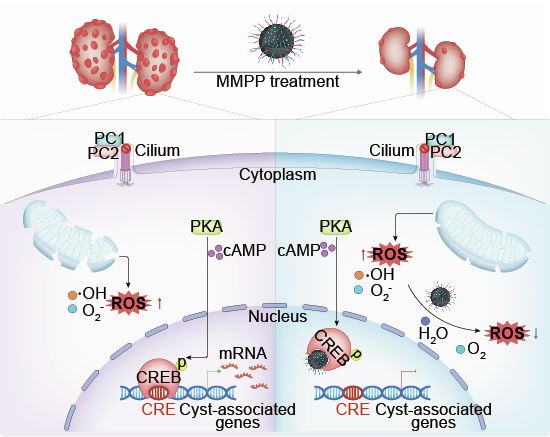
类黑色素纳米颗粒通过氧化应激和CREB的双重抑制来减缓ADPKD的囊肿生长(图源自 EMBO Molecular Medicine )
黑色素是一种内源性生物聚合物,具有显著的抗氧化性能、生物相容性和生物降解性,副作用最小。为了利用黑色素的抗氧化能力,已经开发了类黑色素纳米颗粒(MNP)。先前的研究表明MNP在治疗与ROS升高相关的各种疾病方面效果显著,包括缺血性中风、牙周病、急性肺损伤、急性肾损伤、败血症引起的心肌损伤和伤口愈合。值得注意的是,由于表面存在酚羟基和胺基,MNP还表现出对各种金属离子的优异螯合能力,从而赋予MNP成像能力。有研究合成了聚乙二醇修饰的Mn2+-螯合黑色素(MMPP)纳米颗粒。这些纳米颗粒具备超小的流体动力学尺寸、良好的生理稳定性、对各种有害ROS的显著抗氧化特性等特征,能够有效治疗急性肾损伤和败血症诱导的心肌损伤。虽然MMPP等MNP有望成为治疗各种急性ROS相关疾病的ROS清除剂,但其在治疗慢性疾病方面的潜力仍然未知。此外,与小分子药物类似,了解MNP的分子靶点以最大限度地提高其治疗效果并确保其安全性至关重要。虽然MNP的抗氧化特性已得到广泛研究,但尚不清楚其靶向其他细胞内信号通路和分子的能力。
该研究旨在通过探索MMPP在ADPKD中的治疗潜力。作者证明了体外实验中MMPP对囊肿生长的抑制作用,以及ADPKD小鼠静脉内给药时抑制囊肿生成的功效。从机制上讲,MMPP通过减少氧化应激和维持氧化还原稳态来发挥其治疗作用。重要的是,作者发现MMPP通过bZIPDNA结合结构域直接与CREB相互作用,导致CREB-DNA复合物的破坏并随后抑制CREB的转录活性。
参考消息:
https://www.embopress.org/doi/full/10.1038/s44321-024-00167-2


