Cell子刊:中山大学彭穗/王骥揭示成红细胞岛在肝母细胞瘤中发挥免疫抑制功能
时间:2023-05-19 09:48:34 热度:37.1℃ 作者:网络
成红细胞岛是红系细胞成熟发育的重要细胞结构,在红细胞正常分化及贫血、感染等疾病中均发挥重要作用,但其在肿瘤中发挥的功能还尚未被详细探索。
2023年5月16日,中山大学附属第一医院精准医学研究与小儿外科合作在Cell Reports Medicine 上发表了题为“Intratumoral erythroblastic islands restrain anti-tumor immunity in hepatoblastoma”的研究论文,该研究首次从单细胞水平描绘了HB的免疫微环境组成,报道了成红细胞岛在瘤内的富集,并揭示其通过Galectin-9/TIM-3轴抑制树突状细胞的成熟和抗原递呈功能,诱导免疫抑制微环境的机制,为HB患者的免疫治疗提供潜在靶点和研究新思路。

肝母细胞瘤(HB)是最常见的儿童肝脏恶性肿瘤,标准治疗是手术联合化疗。但是部分HB患儿化疗耐药、预后极差,且大剂量化疗会诱发可能影响患儿生长发育的严重不良反应,需要寻找新的有效且安全的治疗方式,因此要全面了解HB的肿瘤免疫微环境以探索新的治疗靶点。
研究人员对13例原发初治的HB患儿的肿瘤、癌旁及外周血进行单细胞测序,首先对肿瘤免疫细胞组成进行了剖析,发现HB瘤内的B细胞、T细胞等免疫细胞多处于幼稚状态,并存在较多造血祖细胞。其中红系前体细胞特异性的在HB瘤内富集,且增殖更加活跃。为了明确HB内红系前体细胞的来源,研究人员利用外周血、胎肝及骨髓的单细胞数据进行比较,发现HB瘤内的红系前体细胞具有与胎肝内红系前体细胞的相似转录特征,而与外周血及骨髓来源的细胞差异较大,提示HB瘤内的红系前体细胞可能由胎肝期间分化并驻留于瘤内,该发现间接为HB的胚胎起源提供了证据。同时,研究人员在多个队列中发现瘤内红系前体细胞富集越多,HB患儿的长期预后越差,提示红系前体细胞在HB的微环境中可能发挥抑制功能。那么红系前体细胞是如何在患儿肿瘤中存留下来并扩增发挥免疫抑制功能的呢?
研究人员进一步利用细胞互作分析发现红系前体细胞在HB瘤内与VCAM1+巨噬细胞互作密切,并通过VCAM1-ITGA4轴粘附形成成红细胞岛,促进了红系细胞在瘤内的驻留和成熟。进一步分析红系前体细胞的功能发现其在瘤内高表达LGASL9,可通过分泌Galectin-9与树突状细胞(Dendritic cell, DC)上的TIM-3结合,抑制DC的成熟及其共刺激分子(CD80、CD86)与MHC分子的表达。体外细胞实验发现,抗TIM-3抗体可以显著逆转红系前体细胞对DCs的抑制功能,提示TIM-3可作为HB免疫疗法的潜在目标。另一方面,在红系细胞浸润较多的患儿瘤内CD8+T细胞的激活水平和杀伤功能更低,提示红系前体细胞可能通过抑制DC的抗原递呈,抑制瘤内CD8+T细胞的激活从而诱导形成免疫抑制微环境,导致患者预后更差。
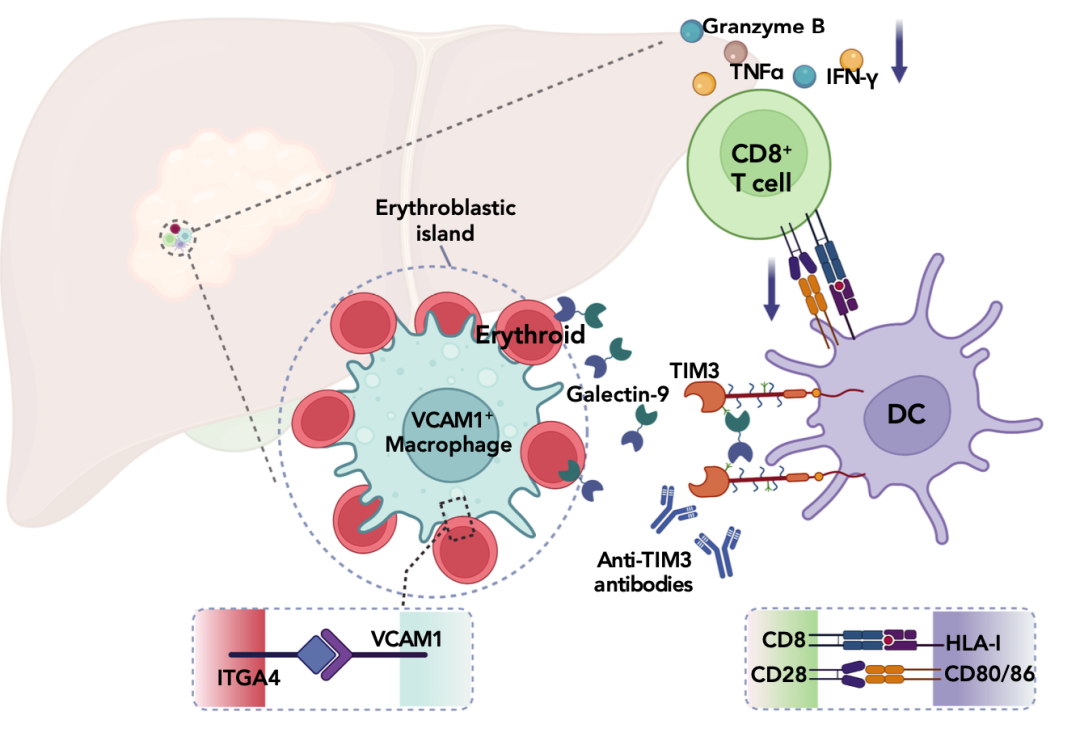
图注:红系前体细胞与VCAM1+巨噬细胞在肝母细胞瘤内形成成红细胞岛,分泌Galectin-9,通过TIM-3抑制DC细胞的成熟,导致CD8+T细胞的功能缺陷。
该研究首次从单细胞水平对原发初治的HB免疫微环境组成进行剖析,发现了红系前体细胞诱导HB微环境幼稚化的机制,为HB患儿提供了药物研发的方向。
中山大学附属第一医院博士后王瑗琪、向骁,小儿外科陈华东医生和超声介入科周路遥教是该文共同第一作者,精准医学研究院彭穗教授、王骥研究员和小儿外科蒋宏副主任医师是共同通讯作者。
原文链接:
https://doi.org/10.1016/j.xcrm.2023.101044


