『脊髓电刺激』—难治性慢性疼痛的治疗新手段
时间:2023-07-18 23:16:16 热度:37.1℃ 作者:网络
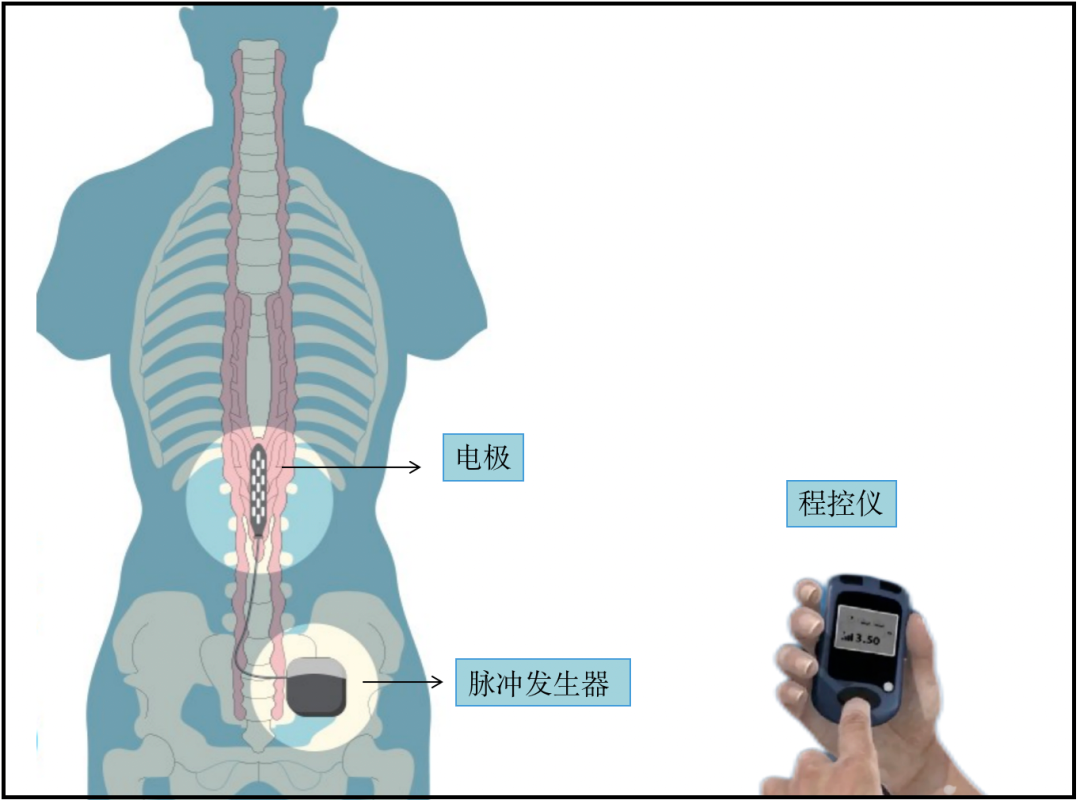
『脊髓电刺激』(SCS)是指将刺激电极置入椎管硬膜外腔,通过电流刺激脊髓后角的感觉神经元及后传导束,阻断疼痛信号,以达到治疗疼痛的一种神经调控方法。
历史沿革
1965年
Melzack和Wall提出了疼痛“门控理论”,成为SCS的理论基础;
1967年
SCS首次应用于疼痛治疗
1970年
诞生了完全植入式SCS系统
1989年
美国食品药品管理局批准SCS用于疼痛治疗
2003年
中日友好医院采用完全植入式SCS成功治疗臂丛损伤所致的慢性疼痛,开国内SCS治疗慢性疼痛之先河。
2019年
清华大学神经调控技术国家工程实验室自主研发的全植入式SCS系统进入临床试验(CITRIP study),开启了SCS系统的国产化进程。
经过数十年的发展,SCS逐渐成为临床治疗慢性疼痛的重要手段。目前认为,对常规治疗无效的慢性疼痛病人,在充分考虑适应证和禁忌证的前提下,越早植入SCS,病人获益越大。
另外临床中发现,部分病人在试用短期SCS治疗后,即使未植入SCS也能获得较长时间的疼痛缓解,由此开启了SCS短时程刺激治疗模式。
作用机制
SCS的作用机制目前尚未完全明了且十分复杂,不仅在脊髓节段性机制和脊髓上机制方面存在着协同作用,而且各种神经递质系统在SCS作用中的关系也极为密切。
1、闸门控制学说
“闸门控制学说”被认为是SCS镇痛作用的『理论基础』。该学说认为:与疼痛相关的神经冲动的传导由脊髓—大脑痛觉传导通路中一种类似闸门作用的特殊结构调节,该机制受粗神经纤维和细神经纤维的活性平衡影响,小直径细纤维促进传导过程,而大直径粗纤维则抑制传导过程。
2、γ-氨基丁酸能机制
在分子水平上,SCS通过调节GABA神经递质(γ-氨基丁酸)的相关的氨基酸来镇痛,同时文献证据表明GABA-B受体似乎特别受电刺激的影响,即SCS通过诱导脊髓背角GABA释放,激活GABA-B受体,从而抑制脊髓背角兴奋性氨基酸谷氨酸和天冬氨酸的释放,最终抑制神经元的痛觉传递。
3、5-羟色胺机制、胆碱能和肾上腺素能机制
文献证据表明SCS通过激活脊髓5-HT受体,增加5-HT的释放,它们对疼痛信号的传递具有抑制作用。此外,一些数据表明,SCS可使脊髓中乙酰胆碱和去甲肾上腺素的水平升高,同时参与了一个去甲肾上腺素能脊髓下行疼痛抑制通路。
4、阿片能系统及内源性大麻素系统机制。
最近一项大鼠神经病理性疼痛损伤模型的研究表明,2Hz的镇痛效果被μ或κ阿片受体拮抗剂所阻断,100Hz的镇痛效果被κ受体拮抗剂所阻断,10kHz的镇痛效果可被任何一种μ、δ或κ受体拮抗剂所阻断,这表明不同频率的SCS的镇痛效果是由不同的内啡肽和阿片受体所介导的,提示阿片能系统参与了SCS的镇痛。
同时有研究表明大麻素1型受体在SCS诱导的痛觉过敏的持久和增量逆转中起着关键的作用,脊髓背角外周神经末梢上的瞬时感受器电位香草酸受体1(TRPV1)受体参与了SCS对脊髓背角浅层伤害性信息传递的抑制,提示内源性大麻素系统参与了SCS的镇痛。
适用范围
1、适应证
腰椎术后疼痛综合征(FBSS)、复杂性区域疼痛综合征(CRPS)、周围神经损伤性疼痛、慢性神经根性疼痛、交感神经相关性疼痛、带状疱疹后神经痛、痛性糖尿病周围神经病变、周围血管性疾病、顽固性心绞痛(经规范内外科治疗无法缓解)、内脏痛、多发性硬化引起的神经痛、放化疗引起的痛性神经病变、脑卒中后疼痛、脊髓损伤后疼痛、神经根(丛)性撕脱伤、癌性疼痛等。近年来,SCS被用于脏器功能保护、改善胃肠功能、中枢催醒并取得了一定效果。
2、禁忌证
-
绝对禁忌证
包括病人有凝血功能异常、手术部位感染、精神心理疾病、躯体形式障碍、不具备使用SCS装置的能力、特殊排异体质等。
-
相对禁忌证
包括病人药物(如阿片类)滥用、全身感染、妊娠、免疫抑制、体内已植入心脏起搏器或除颤器(脉冲发生器可能会损害这些设备的功能)。
操作方法
1、术前评估
SCS的疼痛治疗效果会受到抑郁、焦虑、躯体化等因素的影响,故术前应评估病人的心理状态。术前应针对性进行实验室和影像学检查(MRI、CT和X线等),了解病人的血常规、尿常规、血生化、凝血功能等,明确手术相关节段的椎板间隙、硬膜外腔、脊髓情况等,排除椎管内肿瘤。
2、电极选择
电极的选择取决于病人的情况,以平衡风险和获益。穿刺电极侵入性小,可减轻或避免与神经根压迫相关的潜在风险,但其较易移位。对电极移位风险较高的病人(如青壮年、运动员等),可考虑采用外科电极,或借助良好的固定技术降低移位风险。
对患有严重脊柱相关疾病并接受过脊柱手术的病人,以及存在严重椎管狭窄、黄韧带肥厚或手术瘢痕的病人,穿刺电极在硬膜外腔的行进容易受阻,可考虑采用外科电极。
3、手术操作
SCS手术分测试期和植入期两期进行。
测试期进行1~2周的体验性治疗,观察镇痛疗效和病人对电刺激的耐受程度。若病人疼痛缓解≥50%或总体功能(包括疼痛、睡眠、行走等)改善≥50%和/或病人对测试效果满意,则视为测试合格,可以植入植入式脉冲发生器(IPG);若测试效果不满意,则手术取出电极。
SCS短时程刺激可参照测试期体验性治疗。将电极准确放置到目标脊髓节段,是SCS手术成功的关键。穿刺电极通常采用局部麻醉,经皮穿刺放置,术中通过X线透视和病人对刺激的反馈确认电极位置。外科电极需局部麻醉或全身麻醉放置,术中借助X线透视确认电极位置,也可借助体感诱发电位或肌电图辅助电极位置确认。
IPG植入一般在局部麻醉下进行,术中建立皮下囊袋,将电极经皮下隧道与IPG连接。如电极长度不足可加用延伸导线。IPG植入部位以不影响病人功能为原则,如臀上、锁骨下、腹部等。
长期管理
不同于其他外科操作,SCS术后需要程控来获得及维持良好的疗效。随着远程程控技术的发展,未来术后程控可采用远程方式,以获得更高效、更经济的长期疾病管理。现在有些厂商也开展了患者自我调控的简便方法,但还未广泛使用。
展 望
近年来SCS治疗慢性疼痛已取得几项重大进展。高质量的临床研究已证明SCS能够带来更好的疗效。
高频脊髓电刺激、高密度脊髓电刺激、暴发式脊髓电刺激及背根神经节电刺激等新型SCS模式提高了疗效,减少感觉异常的发生,无线新技术、电极置入引导的新方法、新型电极以及更优程控算法的开发进一步巩固了SCS疗法在慢性疼痛管理中地位。这些新型SCS模式的作用机制逐渐揭开,但还需继续深入探究。
关于SCS疗效影响因素的研究也在不断完善中,有关安全性和有效性的远期随访始终是研究热点。尽管技术在不断进步,但严格的病人筛选仍然是SCS成功干预疼痛至关重要的因素。
参考文献:
[1]罗裕辉,巴茜远,孙武平等.脊髓电刺激对神经病理性疼痛镇痛作用及相关机制研究[J].中国疼痛医学杂志,2019,25(06):414-419.
[2]刘竟,鄢建勤,罗剑刚.脊髓电刺激治疗带状疱疹相关性疼痛研究进展[J].中国疼痛医学杂志,2021,27(12):923-925.


